ANALISIS DE VARIABILIDAD DE SEÑALES CARDIOVASCULARES ... · Empieza al final de la onda S y...
Transcript of ANALISIS DE VARIABILIDAD DE SEÑALES CARDIOVASCULARES ... · Empieza al final de la onda S y...

ANALISIS DE VARIABILIDAD DE SEÑALES CARDIOVASCULARES UTILIZANDO TÉCNICAS DE
PROCESAMIENTO DIGITAL DE SEÑALES
JULIO ENRIQUE RAMIREZ HERNANDEZ
MARIA ISABEL GUAPACHA GARCIA
UNIVERSIDAD TECNOLOGICA DE PEREIRA FACULTAD DE INGENIERIAS ELÉCTRICA, ELÉCTRONICA,
FÍSICA Y CIENCIAS DE LA COMPUTACIÓN PROGRA DE INGENIERIA ELÉCTRICA
PEREIRA

ANALISIS DE VARIABILIDAD EN SEÑALES CARDIOVASCULARES UTILIZANDO TÉCNICAS DE
PROCESAMIENTO DIGITAL DE SEÑALES
JULIO ENRIQUE RAMIREZ HERNANDEZ MARIA ISABEL GUAPACHA GARCIA
Trabajo de grado para optar a el título de ingenieros electricistas
DIRECTOR:
ING. EDUARDO GIRALDO
UNIVERSIDAD TECNOLOGICA DE PEREIRA FACULTAD DE INGENIERIAS ELÉCTRICA, ELÉCTRONICA,
FÍSICA Y CIENCIAS DE LA COMPUTACIÓN PROGRAMA DE INGENIERIA ELÉCTRCA
PEREIRA

La elaboración de este proyecto va dedicad a todos aquellos que colaboraron en su realización en especial
a mis dos hermosos hijos y a mi compañero de aventura por todo su cariño y apoyo.

CAPITULO 1
VARIACIÓN EN SEÑALES ELECTROCARDIOGRÁFICAS
1.1 INTRODUCCIÓN.
En este capitulo daremos una visión básica acerca de: Que es un electrocardiograma, las
ondas que lo conforman, las patologías más conocidas asociadas al electrocardiograma
(ECG) y la variabilidad del ECG en presencia de estas patologías.
1.2 ¿QUE ES UN ELECTROCARDIOGRAMA?
Un electrocardiograma conocido como ECG es un registro visible de la actividad
eléctrica del corazón, inscrito por un estilete que traza dicha actividad en una tira de
papel (Fig. 1.0), la cual se desplaza en forma continua, dando forma a una onda que nos
indicaran la transmisión del impulso eléctrico que contrae al músculo cardiaco y por
tanto, lo hace realizar su trabajo (expulsar sangre por una parte especifica).
(a) (b)
Fig. 1.1. (a) Electrocardiógrafo digital. [1] (b) Papel utilizado para la toma de
electrocardiograma
1.3 ANALISIS DEL SISTEMA CARDIACO.
Lo que se pretende con este análisis es conocer un poco sobre la anatomía del corazón
y el origen de su actividad eléctrica, lo cual da principio a este trabajo.

1.3.1 ANATOMIA DEL CORAZÓN
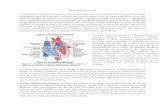
Fig. 1.2. El corazón y fisiología [2].
En la figura 2 podemos observar la anatomía del corazón humano, conformado
básicamente por cuatro cavidades: la aurícula derecha e izquierda y los ventrículos
derecho e izquierdo. En su parte superior esta ubicada la vena cava superior, cayado de
la aorta, la válvula pulmonar; en su lado derecho se observa la vena pulmonar derecha,
músculo papilar, válvula tricúspide y la vena cava inferior; al lado izquierdo tiene, vena
pulmonar izquierda, válvula mitral, válvula aórtica, tabique interventricular y la aorta.
Conociendo la distribución fisiológica del corazón podemos ya empezar a comprender
el sistema de conducción cardíaco, el cual comienza en el nodo sinusal y se extiende
hasta el miocardio auricular y ventricular [2].

1.3.2 SISTEMA DE CONDUCCIÓN CARDIACO
Figura 1.3. Sistema de conducción cardiaco [3].
1.3.2.1 NODO SINUSAL (SENOAURICULAR SA)
Nodo SA, esta situado en la parte superior de la aurícula derecha, ligeramente lateral a
la unión de la orejuela correspondiente a este lado y la vena cava superior, en
condiciones normales, este nódulo genera un estímulo eléctrico cada vez que el corazón
late, el cual viaja a través de las vías de conducción y hacen que las cavidades bajas del
corazón se contraigan y bombeen la sangre hacia fuera. Ver Figura 3 [3].
1.3.2.2 NODO AURICULO-VENTRICULAR (AV) El Nodo AV, Localizado en la aurícula derecha en su parte baja, al lado derecho del
septo ínter auricular y el anillo fibroso central exactamente encima de los ventrículos,
aquí llega el impulso eléctrico proveniente del nodo SA, es aquí en el nodo AV donde
se retrasan los impulsos durante unos breves instantes para continuar por la vía de
conducción a través del Haz de His hacia los ventrículos. Este es conocido también
como el marcapaso fisiológico. Ver Figura 3 [3].
1.3.2.3 CONDUCCIÓN A NIVEL AURICULAR El modo de conducción de los impulsos a las aurículas ha sido un tema de bastante
controversia. A nivel de aurículas no existe un “verdadero” tejido de conducción (a
diferencia de los ventrículos que si cuentan con tejido conductivo: el Haz de His y fibras
de Purkinje).El impulso se transmite en forma radial y sincitial (la mas rápida) desde el
nodo SA al nodo AV, de manera que se admite que hay tres áreas de fibras musculares

de conducción más rápida llamadas: 1)
internodal media de Wenckebach
1.3.2.4 HAZ DE HIS Pequeña banda de fibras miocá
proveniente de las aurículas a los
parte posterior inferior del septo membranoso y se dirige en dirección anterior y medial.
Tiene una longitud aproximada de 1cm, antes de dividirse siendo el
ramificado” [4].
1.3.2.5 RAMAS Y FIBRAS DE PURKINJE La porción ramificada, comienza con las fibras que
“cascada”. La rama izquierda se divide en dos ramas principales:
1) La rama antero-superior, que se dirige hacia arriba y adelante terminando en el
músculo papilar anterior.
2) Rama postero-inferior, que se dirige hacia atrá
papilar posterior.
Después de dar las ramas para formar “la rama izquierda” el Haz continua como “la
rama derecha”. Tanto la ra
trayecto “no ramificado”, para final
conectaran con el endocardio ventricular
1.4 ECG NORMAL Y ANATOMIA CARDIACA CORRELATIVA
El electrocardiograma como ya se
actividad eléctrica del corazón,
evaluar dicha actividad, el ECG esta compuesto por varias ondas e “intervalos” que
representan el comportamiento del
numerales.
1.4.1 ECG Normal:
Todos los latidos cardiacos aparecen con morfologías similares, separados por espacios
iguales; cada uno esta formado por tres unidades principales: Onda P, complejo QRS y
onda T. Aunque para muchas aplicaciones se hace necesario estudiar el compl
como ondas separadas tomando segmentos y
Figura
de conducción más rápida llamadas: 1) Vía internodal anterior de Bachmann
Wenckebach y 3) Vía internodal posterior de Thorel
miocárdicas especializadas que conduce la onda de contracción
de las aurículas a los ventrículos. Cruza el triangulo fibroso pasando por la
inferior del septo membranoso y se dirige en dirección anterior y medial.
Tiene una longitud aproximada de 1cm, antes de dividirse siendo el
RAMAS Y FIBRAS DE PURKINJE
La porción ramificada, comienza con las fibras que forman la rama izquierda en
. La rama izquierda se divide en dos ramas principales:
superior, que se dirige hacia arriba y adelante terminando en el
inferior, que se dirige hacia atrás y abajo, terminando en el músculo
Después de dar las ramas para formar “la rama izquierda” el Haz continua como “la
rama derecha”. Tanto la rama izquierda y derecha están “aisladas” durante todo su
trayecto “no ramificado”, para finalmente ramificarse en fibras de Purkinje que se
conectaran con el endocardio ventricular [5].
ECG NORMAL Y ANATOMIA CARDIACA CORRELATIVA
como ya se había mencionado es un registro relativo de la
del corazón, además es el procedimiento más sencillo y
evaluar dicha actividad, el ECG esta compuesto por varias ondas e “intervalos” que
representan el comportamiento del corazón de las cuales se hablará en los
Todos los latidos cardiacos aparecen con morfologías similares, separados por espacios
iguales; cada uno esta formado por tres unidades principales: Onda P, complejo QRS y
Aunque para muchas aplicaciones se hace necesario estudiar el compl
como ondas separadas tomando segmentos y analizando sus características
Figura 1.4. Esquema de una señal electrocardiográfica.
de Bachmann 2) Vía
3) Vía internodal posterior de Thorel [4].
especializadas que conduce la onda de contracción
Cruza el triangulo fibroso pasando por la
inferior del septo membranoso y se dirige en dirección anterior y medial.
Tiene una longitud aproximada de 1cm, antes de dividirse siendo el “Haz no
forman la rama izquierda en
superior, que se dirige hacia arriba y adelante terminando en el
s y abajo, terminando en el músculo
Después de dar las ramas para formar “la rama izquierda” el Haz continua como “la
aisladas” durante todo su
mente ramificarse en fibras de Purkinje que se
ECG NORMAL Y ANATOMIA CARDIACA CORRELATIVA
es un registro relativo de la
s sencillo y rápido para
evaluar dicha actividad, el ECG esta compuesto por varias ondas e “intervalos” que
en los próximos
Todos los latidos cardiacos aparecen con morfologías similares, separados por espacios
iguales; cada uno esta formado por tres unidades principales: Onda P, complejo QRS y
Aunque para muchas aplicaciones se hace necesario estudiar el complejo QRS
características.
4. Esquema de una señal electrocardiográfica.

1.4.2 LATIDO CARDIACO AISLADO NORMAL
Figura 1.
Cada latido se manifiesta por cinco ondas fundamentales: P, Q, R, S, T. Las ondas Q, R
y S representan la activación ventricular. Suel
complejo QRS [7]”.
1.4.2.1 EL CORAZÓN CON
Cada onda representa la transmisión de un impulso eléctrico que contrae al músculo
cardiaco y por lo tanto lo hace expulsar sangre por una parte específica del corazón.
LATIDO CARDIACO AISLADO NORMAL:
1.5. Ondas de un latido normal del corazón.
latido se manifiesta por cinco ondas fundamentales: P, Q, R, S, T. Las ondas Q, R
y S representan la activación ventricular. Suelen considerarse como una unidad
CON RELACIÓN AL ECG:
Cada onda representa la transmisión de un impulso eléctrico que contrae al músculo
cardiaco y por lo tanto lo hace expulsar sangre por una parte específica del corazón.
(a)
(b)
latido se manifiesta por cinco ondas fundamentales: P, Q, R, S, T. Las ondas Q, R
en considerarse como una unidad “El
Cada onda representa la transmisión de un impulso eléctrico que contrae al músculo
cardiaco y por lo tanto lo hace expulsar sangre por una parte específica del corazón.

(c)
Figura 1.6. (a) La onda P representa el impulso que atraviesa las aurículas (parte
superior del corazón). (b) El complejo QRS representa el impulso que atraviesa los
ventrículos, situados por debajo de las aurículas. (c) La onda T es originada por la
recuperación eléctrica (repolarización) de los ventrículos, momento en el cual no hay
contracciones cardiacas.
De estas características y definiciones de las ondas hablaremos más adelante.
1.4.2.2 VÍA ELÉCTRICA NORMAL:
La onda P (onda auricular) empieza en el nodo SA (marcapaso fisiológico normal),
localizado en la parte alta de la aurícula derecha. El complejo QRS (onda ventricular),
empieza en el nodo AV, localizado en la parte superior de los ventrículos. Ambos nodos
están inervados por el sistema simpático, que aumenta la frecuencia cardiaca, y por el
sistema parasimpático (nervio vago) que disminuye la frecuencia cardiaca.
Ya conocidas las medidas básicas, estamos familiarizados con la relación entre las
ondas del ECG y la anatomía del corazón, veamos cual es el significado de cada onda e
intervalo.
a. ONDA P
Esta onda representa la contracción auricular, su ensanchamiento indica agrandamiento
de la aurícula, como puede producirse en la estenosis mitral (la aurícula crece porque la
abertura del orificio valvular mitral, entre la aurícula y el ventrículo izquierdo, es
pequeña, obligando a la sangre a estancarse y a la pared auricular a expandirse). La
onda P suele considerarse aumentada si se tiene una altura mayor de dos y medio
pequeños cuadros, una anchura mayor de tres pequeños cuadros o ambas características.
b. INTERVALO PR
Este se extiende desde el comienzo de la onda P al de la onda Q. Tiene importancia
principalmente porque este intervalo aumenta de duración en la cardiopatía
arterioesclerosa y en la fiebre reumática. Este alargamiento se produce porque el tejido
cardiaco, cuya actividad está representada por el intervalo PR (aurícula y zona del nodo
AV), está inflamado o es cicatrizal, y el impulso se propaga con menor velocidad. En
términos general es, el intervalo PR normal no dura más de de 0,20s [7].

Figura 1.7. Intervalo PR
c. COMPLEJO QRS:
Esta formado por tres deflexiones: onda Q, el primer desplazamiento hacia abajo; onda
R, en el desplazamiento hacia arriba, y onda S, el ultimo desplazamiento hacia abajo.
Una onda Q grande puede indicar infarto de miocardio antiguo. Una onda R alta suele
indicar crecimiento ventricular. La onda S tiene poca significación para la actual
exposición. Aunque no siempre se registren complejos QRS con onda Q y con onda S,
es costumbre usar la denominación compleja QRS para indicar que es un impulso
ventricular [7].
d. SEGMENTO ST:
Empieza al final de la onda S y finaliza al principio de la onda T. Esta elevado cuando
hay infarto de miocardio agudo. Está hundido cuando: a) El músculo cardiaco no recibe
su provisión normal de oxigeno, b) El paciente recibe digital.
Figura 1.8. Segmento ST
e. ONDA T: Representa la recuperación eléctrica de la contracción ventricular. (Los electrones se
desplazan para recuperar sus posición normal, el reposo). La onda T se aplana cuando
el corazón no recibe suficiente oxigeno, como en la cardiopatía arterioesclerosa.
Puede ser alta cuando la concentración sérica de potasio es elevada. La onda T
normal no excede de 5 cuadrados pequeños (5mm).

En la siguiente tabla se describirá la relación entre las diferentes ondas y segmentos, su
duración (ms) y su amplitud (mV) representativas en el ECG.
Inscripción
Amplitud (mV)
Duración (ms)
Onda P < 2,5 < 100
Intervalo PR - 120 – 220
Complejo QRS < 25 en V5 60 – 120
Onda T < 6 -
Intervalo QT - 350 – 440
Intervalo RR - 600 - 1000
Segmento ST A 80 ms de J<-1 50 – 150
Tabla 1.1. Relación entre ondas y segmentos [11].
1.5 ARRITMIAS FRECUENTES Ahora que ya conocemos algo de la electrocardiografía básica vamos a considerar varias
arritmias que se observan con frecuencia; aquí nos referimos a tres, que se originan en el
nodo SA, luego veremos las nacidas fuera de esté. Pero primero hemos de explicar
como se determina la frecuencia cardiaca, porque el ritmo y la irregularidad de los
impulsos eléctricos se utilizan para identificar las arritmias.
1.5.1 DETERMINACION DE LA FRECUENCIA CARDIACA
Como ya se ha indicado cada cuadrado grande en el papel del ECG representa 0.20s.
Por tanto 300 representa un minuto (0,20*300 = 60s). Para determinar en forma rápida
pero aproximada la frecuencia cardiaca hay que contar el número de cuadrados grandes
entre una y otra onda R (complejo QRS) del ECG y dividir 300 por esta cifra. Por
ejemplo, si en una muestra hay tres cuadrados grandes entre dos onda R. Dividiendo por
300 por tres nos da una frecuencia de cien latidos por segundo (si hubiera dos
cuadrados, la frecuencia seria de 150 latidos, y si hubiera 4, seria de 75).
1.5.2 RUTA DE ESTIMULO EN LOS RITMOS SINUSALES
Figura 1.9. Ruta de estímulo del SA

Las tres arritmias que se originan en el nodo SA son: La arritmia sinusal, la taquicardia
sinusal y la bradicardia sinusal. La vía que siguen sus impulsos eléctricos es
exactamente la de un ritmo sinusal normal (ECG normal), según se indica, En
consecuencia, la onda P (auricular) y el complejo QRS (ventricular) tienen la misma
configuración que en el ritmo normal. La diferencia estriba en la frecuencia y
regularidad de los impulsos [9].
1.5.2.1 ARRITMIA SINUSAL
Figura 1.10. ECG de arritmia sinusal
Todos los complejos son normales, pero la frecuencia cardiaca es irregular.
Aumentar con la inspiración y disminuye con la espiración. Esta irregularidad es
frecuente en niños. Es debida a impulsos nerviosos que provienen de los pulmones y
llegan al centro cardiaco del cerebro; esté a su vez, estimula el nodo sinusal que varia
su frecuencia con la respiración. Al tomar el pulso del niño hay que tener presente que
la arritmia sinusal es normal y que la frecuencia cardiaca aumenta con la inspiración y
disminuirá con la espiración.
1.5.2.1.1 TAQUICARDIA SINUSAL
Figura 1.11. ECG de taquicardia sinusal
Se define como una frecuencia mayor de 100. En otras palabras, todos los complejos
son normales, pero la frecuencia cardiaca es mayor de 100 por minuto (raramente
excede los 140) [9]. La estimulación nerviosa excesiva es la que provoca ese aumento,
y la causa mas frecuente son ansiedad, fiebre y choque. Como la taquicardia sinusal
suele ser secundaria a factores extra cardiacos, el tratamiento debe dirigirse hacia la
causa subyacente.

1.5.2.1.2 BRADICARDIA SINUSAL
Figura
Esta arritmia se diagnostica cuando la frecuencia cardiaca es menor de 60 por minuto,
conservando todos los complejos su configuración normal. Puede observarse
comúnmente en atletas bien entrenados y en pacientes bajo acción de digital
morfina, o aminas presoras
no suele necesitarse tratamiento con medicamentos.
Cuando se presenta en el infarto de miocardio, la bradicardia sinusal puede provocar
perdidas de conocimiento (síndrome de Sto
congestiva [9]. Si aparecen síntomas, el tratamiento debe empezarse inmediatamente
tratando de inhibir el nervio vago (que hace más lenta la frecuencia cardiaca), con lo
cual el corazón se acelera.
Ya habiendo dado una explicación gen
taquicardia sinusal y bradicardia
SA, sitio normal de origen del impulso eléctrico del corazón.
más: las arritmias auriculares las cuales empiezan fuera del nodo SA, pero
limitadas a la aurícula. Como la patología que provoca bloqueo auriculoventricular se
encuentra en esta zona general, también nos ocuparemos de ello.
1.5.3 IMPULSOS ELECTRICOS
Como ya se dijo, el impulso eléctrico para: El ritmo normal, la arritmia sinusal, la
taquicardia y la bradicardia sinusal, se originan en el nodo seno auricular (SA),
localizado en la parte alta de la aurícula derecha. El impulso eléctrico hace que el
músculo cardiaco se contraiga y por tanto, expulse sangre contenida en las aurículas.
Como el nodo SA controla la frecuencia cardiaca, se dice que hay un marcapaso
fisiológico normal.
El impulso eléctrico que genera las arritmias
del nodo SA, pero todavía dentro de la aurícula.
BRADICARDIA SINUSAL
Figura 1.12. ECG de bradicardia sinusal
a se diagnostica cuando la frecuencia cardiaca es menor de 60 por minuto,
conservando todos los complejos su configuración normal. Puede observarse
comúnmente en atletas bien entrenados y en pacientes bajo acción de digital
o aminas presoras (para tratamiento de la presión arterial baja)
no suele necesitarse tratamiento con medicamentos.
Cuando se presenta en el infarto de miocardio, la bradicardia sinusal puede provocar
perdidas de conocimiento (síndrome de Stokes_Adams) o insuficiencia cardiaca
. Si aparecen síntomas, el tratamiento debe empezarse inmediatamente
tratando de inhibir el nervio vago (que hace más lenta la frecuencia cardiaca), con lo
Ya habiendo dado una explicación general y básica de tres arritmias (arritmia
y bradicardia sinusal), recordemos que estas comienza
SA, sitio normal de origen del impulso eléctrico del corazón. Nos ocuparemos de tres
las arritmias auriculares las cuales empiezan fuera del nodo SA, pero
a la aurícula. Como la patología que provoca bloqueo auriculoventricular se
encuentra en esta zona general, también nos ocuparemos de ello.
IMPULSOS ELECTRICOS NORMALES
Como ya se dijo, el impulso eléctrico para: El ritmo normal, la arritmia sinusal, la
taquicardia y la bradicardia sinusal, se originan en el nodo seno auricular (SA),
localizado en la parte alta de la aurícula derecha. El impulso eléctrico hace que el
ulo cardiaco se contraiga y por tanto, expulse sangre contenida en las aurículas.
Como el nodo SA controla la frecuencia cardiaca, se dice que hay un marcapaso
El impulso eléctrico que genera las arritmias a continuación estudiadas se
del nodo SA, pero todavía dentro de la aurícula.
a se diagnostica cuando la frecuencia cardiaca es menor de 60 por minuto,
conservando todos los complejos su configuración normal. Puede observarse
comúnmente en atletas bien entrenados y en pacientes bajo acción de digital, de
baja). En tales casos
Cuando se presenta en el infarto de miocardio, la bradicardia sinusal puede provocar
uficiencia cardiaca
. Si aparecen síntomas, el tratamiento debe empezarse inmediatamente
tratando de inhibir el nervio vago (que hace más lenta la frecuencia cardiaca), con lo
(arritmia sinusal,
comienzan en el nodo
Nos ocuparemos de tres
las arritmias auriculares las cuales empiezan fuera del nodo SA, pero se conservan
a la aurícula. Como la patología que provoca bloqueo auriculoventricular se
Como ya se dijo, el impulso eléctrico para: El ritmo normal, la arritmia sinusal, la
taquicardia y la bradicardia sinusal, se originan en el nodo seno auricular (SA),
localizado en la parte alta de la aurícula derecha. El impulso eléctrico hace que el
ulo cardiaco se contraiga y por tanto, expulse sangre contenida en las aurículas.
Como el nodo SA controla la frecuencia cardiaca, se dice que hay un marcapaso
estudiadas se origina fuera

1.5.3.1 TAQUICARDIA PAROXISTICA AURICULAR (TPA)
Figura 1.13. Impulso eléctrico generado fuera del nodo SA
Se trata de una arritmia frecuente. Suele observarse en el adulto relativamente joven con
corazón normal, pero que probablemente ya ha tenido varios síntomas previos al
trastorno. El paciente suele quejarse de un golpeteo o tremulaciones bruscas en el
pecho, acompañada de lasitud o dificultad para respirar. La frecuencia cardiaca suele
estar entre 140 y 250 por minuto, como promedio es de aproximadamente180.
1.5.3.1.1 Vías normales de la TPA: Un impulso que sigue a lo largo de la vía normal
produce un ECG normal. Un impulso que sigue la vía anormal del TPA, produce una
onda P anormal. Sin embargo, el complejo QRS es normal (representa el impulso
ventricular), ya que no necesariamente hay trastornos en los ventrículos.
1.5.3.1.2 ECG DE LA TPA: La onda P es de forma anormal y muchas veces resulta
difícil de distinguir, porque se halla superpuesta a la onda T precedente, como
consecuencia de la gran frecuencia cardiaca (una frecuencia cardiaca rápida tiende a
superponer ondas en un ECG). La onda P es anormal porque el impulso comienza fuera
del nodo SA. Como dichas ondas P suelen ser pequeñas, muchas veces resulta
imposible distinguir las variaciones en su configuración.
Figura 1.14. ECG de la TPA
En resumen, la TPA se caracteriza en el ECG por:
1. Frecuencia mayor a la de la taquicardia sinusal (mas de 140 por minuto),
2. Complejo QRS normales, y
3. Ondas P de forma anormal que en muchos casos no se distinguen por quedar
camufladas dentro de ondas T precedentes [9].

1.5.3.2 LATIDO FUERTE (FLÚTTER) AURICULAR
Como su nombre lo indica es una tremulación auricular regular rápida de la aurícula.
Suele producirse en un corazón enfermo (generalmente arterioescleroso o reumático),
en contraste con la TPA que se suele observar en corazones normales. Las ondas P, que
están arrítmicas se denominan F, se suceden de tal forma que el registro cobra aspecto
de dientes de sierra porque provienen de un foco distinto al sinusal, y a una frecuencia
muy alta. Como en la TPA, el impulso proviene de un foco ectópico auricular. A
diferencia de la TPA cuya frecuencia auricular es de 180, como termino medio (no el
pulso o la frecuencia ventricular), el flútter tiene una frecuencia de 250 a 350 por
minuto. Aunque las reglas que damos a continuación sean muy simples, resultan muy
útiles para distinguir las arritmias auriculares [8]:
1. La frecuencia auricular en la taquicardia sinusal llegan hasta 140 por minuto,
2. La frecuencia auricular en la TPA se halla entre 140 y 250 por minuto y
3. La frecuencia auricular en el flútter se halla entre 250 y 350 por minuto.
VIA NORMAL VIA DEL FLUTTER AURICULAR
(a) (b)
Figura 1.15. (a) Vía normal del impulso. (b) Vía del impulso en el flútter auricular
1.5.3.2.1 Vías normal y del flútter auricular: Estos son los mismos esquemas
utilizados para demostrar la vía de la TPA, porque esta vía es ectópica es la misma del
flútter auricular que para TPA. Obsérvese que si bien el impulso del flútter auricular se
origina fuera del nodo sinusal, nace en la aurícula.
1.5.3.2.2 ECG del flútter auricular: Las flechas indican las ondas F que provienen del
foco ectópico rápido en la aurícula. Obsérvese que no todas las ondas estimulantes van
seguidas de un complejo QRS (onda ventricular). Como la anomalía que existe en el
corazón se halla por encima del nodo AV, los complejos QRS son de configuración
normal.

Figura 1.16. ECG de Flútter auricular
Dado que las ondas F se suceden rápidamente, el nodo AV no puede conducirlas todas;
por tanto, se produce cierto grado de bloqueo a nivel del nodo. Por ejemplo, si la
frecuencia auricular es de 300, la ventricular (igual a la del pulso) puede ser de 150.
Entonces se dice que el bloque es de 2:1 puesto que hay dos impulsos auriculares por
cada respuesta ventricular. La proporción 2:1 es de bloqueo mas frecuente en el flútter
auricular. La mayor parte de los casos TPA no presenta bloqueo y todos los impulsos
son trasmitidos por el nodo AV a los ventrículos.
1.5.3.3 FIBRILACIÓN AURICULAR
Suele observarse en pacientes de edad avanzada con enfermedad arteriosclerótica del
corazón. La arteriosclerosis origina cicatrices en la aurícula y, por tanto dificulta el
curso normal de la onda auricular. El complejo QRS (onda ventricular) es de
configuración normal porque el tejido de conducción mas allá del nodo AV no ha sido
afectado en forma critica.
Como implica la palabra “fibrilación”, las ondas P normales quedan sustituidas por
otras rápidas irregulares, cada una de configuración diferente. Estas llamadas
frecuentemente ondas de fibrilación, representan formas diferentes, porque provienen de
focos diversos en el territorio auricular, en contraste con las ondas P del flútter
auricular, que se suceden regularmente y son uniformes, por originarse el estimulo en
un mismo foco [9].
1.5.3.3.1 Vías normal y de la fibrilación auricular: Existen varios focos ectópicos en
la aurícula. Como cada pequeña onda auricular proviene de un foco diferente y sigue un
trayecto también diferente, la forma de cada onda auricular es distinta.
VIA NORMAL VIA DE LA FIBRILACIÓN AURICULAR

(a) (b)
Figura 1.17. (a) Vía normal del impulso. (b) Vía del impulso en la fibrilación auricular
Como las ondas P se presentan con intervalos variab
un ritmo irregular, igual que el pulso del paciente. Las ondas P llegan tan rápido, que no
todas atraviesan hacia los ventrículos, debido al periodo refractario normal en el nodo
AV; por tanto la frecuencia auricular suele
Figura
1.5.3.3.2 ECG de fibrilación auricular: respuesta ventricular, esto es, de un complejo QRS
presentan con intervalos irregulares, cuando hay fibrilación auricular el ritmo
ventricular es irregular.
En ocasiones el ritmo ventricular es muy rápido porque el nodo AV bloquea un número
de latidos relativamente menor de lo normal. En este caso la actividad a
no se manifieste en el ECG y hay dificultad para definir arritmia. Muchas veces resulta
útil la siguiente regla: Si se observa complejos QRS normales con ritmo tan rápido que
no puede verse la actividad auricular y si el ritmo es irregular
fibrilación auricular.
1.5.3.4 BLOQUEO AV
En esta arritmia, el nodo AV esta enfermo y hay dificultad para que trasmita la onda p
hacia los ventrículos. Las causas más comunes son la arteriosclerosis y su sucedáneo, el
infarto de miocardio.
Una cicatriz, la inflamación o el edema, impiden o hacen más lenta la transmisión del
impulso eléctrico por el nodo A
clasifica como bloqueo de primer grado, segundo grado o tercer grado.
(a) (b)
7. (a) Vía normal del impulso. (b) Vía del impulso en la fibrilación auricular
Como las ondas P se presentan con intervalos variables, los complejos QRS presentan
un ritmo irregular, igual que el pulso del paciente. Las ondas P llegan tan rápido, que no
todas atraviesan hacia los ventrículos, debido al periodo refractario normal en el nodo
AV; por tanto la frecuencia auricular suele ser más rápida que la ventricular.
Figura 1.18. ECG de fibrilación auricular
ECG de fibrilación auricular: sólo algunas de las ondas P van seguidas de
, esto es, de un complejo QRS. Pero como estos complejos se
an con intervalos irregulares, cuando hay fibrilación auricular el ritmo
En ocasiones el ritmo ventricular es muy rápido porque el nodo AV bloquea un número
de latidos relativamente menor de lo normal. En este caso la actividad a
no se manifieste en el ECG y hay dificultad para definir arritmia. Muchas veces resulta
útil la siguiente regla: Si se observa complejos QRS normales con ritmo tan rápido que
no puede verse la actividad auricular y si el ritmo es irregular, probablemente existe
En esta arritmia, el nodo AV esta enfermo y hay dificultad para que trasmita la onda p
hacia los ventrículos. Las causas más comunes son la arteriosclerosis y su sucedáneo, el
Figura 1.19. Bloqueo AV
cicatriz, la inflamación o el edema, impiden o hacen más lenta la transmisión del
impulso eléctrico por el nodo AV. El bloqueo varia, desde muy ligero a completo, y se
clasifica como bloqueo de primer grado, segundo grado o tercer grado.
7. (a) Vía normal del impulso. (b) Vía del impulso en la fibrilación auricular
les, los complejos QRS presentan
un ritmo irregular, igual que el pulso del paciente. Las ondas P llegan tan rápido, que no
todas atraviesan hacia los ventrículos, debido al periodo refractario normal en el nodo
ser más rápida que la ventricular.
algunas de las ondas P van seguidas de
Pero como estos complejos se
an con intervalos irregulares, cuando hay fibrilación auricular el ritmo
En ocasiones el ritmo ventricular es muy rápido porque el nodo AV bloquea un número
de latidos relativamente menor de lo normal. En este caso la actividad auricular quizá
no se manifieste en el ECG y hay dificultad para definir arritmia. Muchas veces resulta
útil la siguiente regla: Si se observa complejos QRS normales con ritmo tan rápido que
, probablemente existe
En esta arritmia, el nodo AV esta enfermo y hay dificultad para que trasmita la onda p
hacia los ventrículos. Las causas más comunes son la arteriosclerosis y su sucedáneo, el
cicatriz, la inflamación o el edema, impiden o hacen más lenta la transmisión del
varia, desde muy ligero a completo, y se

1.5.3.4.1 Bloqueo AV de primer grado: como el tejido alrededor del nodo AV es
anormal, el impulso toma mayor tiempo para atravesar la zona. Esto se traduce en un
aumento de la duración del intervalo PR en el ECG (el intervalo PR representa el
impulso que atraviesa las aurículas y la zona del nodo AV). En contraste con los
bloqueos de segundo y tercer grados, en el primer grado todas las ondas auriculares (P)
llegan al ventrículo y dan lugar a complejos QRS. Cuando la conducción es normal, el
intervalo no es mayor de 0,20s (5 cuadros de 0,04s cada uno, sobre el papel del ECG).
CONDUCCION NORMAL AV BLOQUEO AV GRADO 1
(a) (b)
Figura 1.20. (a) ECG de un impulso normal. (b) ECG de un Bloqueo grado 1
1.5.3.4.2 Bloqueo AV de segundo grado: Algunas ondas P no pasan a los ventrículos,
pero otras si. Se pueden observar bloqueos del tipo 2:1; esto significa que cada segunda
onda P sí va seguida de un complejo QRS. Este bloqueo de segundo grado también
puede ser de tipo 3:1 o cualquiera de estas combinaciones. Lo esencial para distinguirlo
del bloqueo de primer grado, es que sólo algunas ondas auriculares P se conducen y dan
lugar a complejos QRS, otras no se conducen.
Figura 1.21. Bloqueo AV de segundo grado
1.5.3.4.3 Bloqueo AV de tercer grado: También se llama bloqueo AV completo. Las
ondas auriculares P no atraviesan el nodo AV hacia los ventrículos; por tanto, éstas y
los complejos QRS son independientes.

Figura 1.22. Bloqueo AV de tercer grado
Las ondas P se observan en el ECG antes de los complejos QRS. Obsérvese que no hay
relación constante entre las ondas P y los complejos QRS lo cual se observa fielmente
en las graficas de un ECG. La frecuencia del pulso es lenta, porque los ventrículos laten
independientemente y la frecuencia es de unos 40 latidos por minuto.
1.5.3.5 INFARTO DEL MIOCARDIO (IM):
Un punto importante para recordar, en relación con la interpretación del ECG de un
infarto del miocardio, es que aproximadamente 15% de los infartos no se manifiestan
en el trazado inicial. Por tanto, si una persona tiene síntomas compatibles con un ataque
coronario, aunque su ECG sea normal, debe ingresar en el hospital para que sea
observada y tomar electrocardiograma aleatoriamente.
El primer signo de infarto suele ser la elevación del segmento ST. Esta va seguida de
inversión de la onda T y mas tarde aparece una onda Q prominente. Cuando el infarto
ha cicatrizado, la onda Q puede quedar como el único estigma de una antigua oclusión
coronaria [9].
En las siguientes figuras del ECG se puede observar el comportamiento del ECG
después del infarto del miocardio.
Figura 1.23. ECG en un IM el segmento ST se encuentra elevado.
1 Aquí (figura 1.23) observamos unas horas después del infarto el segmento ST esta
elevado. 2. Unas horas después incluso días mas tarde hay inversión de la onda T y la
onda Q se hace mayor. 3. Unos días o semanas después la onda T recupera su dirección
hacia arriba, pero la onda Q puede seguir prominente.
1.5.3.5.1 Onda Q anormal: Como una onda Q prominente muchas veces indica infarto
antiguo (excepto en AVR, en donde una onda grande es normal) muchas veces se
pregunta que dimensiones puede tener la onda Q antes de considerarla anormal. Se

puede considerar anormal si tiene una anchura mayor de 0,04s (un pequeño cuadro del
papel de ECG), o si su profundidad es mayor de la tercera parte de la magnitud del
complejo QRS.
Figura 1.24. Un infarto del miocardio se caracteriza por elevación de ST e inversión de
T. Una Q grande puede indicar infarto antiguo.
1.5.4 AFECCIONES EN LOS VENTRICULOS 1.5.4.1 CONTRACCIONES VENTRICULARES PREMATURAS (EXTRASISTOLES) (CVP)
Se observa en la mayoría de pacientes con infarto del miocardio y constituye el
trastorno de ritmo más frecuente y fácil de reconocer en el ECG. También puede
presentarse en personas normales, causado muchas veces por fumar, tomar café o
alcohol. Cuando extrañas patologías, se observan, sobre todo en pacientes con
enfermedades cardiacas arterioscleróticas.
VÍAS NORMALES VIAS DE LA CVP
(a) (b)
Figura 1.25. (a) Vía normal del impulso. (b) Vía del impulso de la CVP

1.5.4.1.1 Vías normales y de la CVP (extrasístole):contracciones ventriculares prematuras se originan en el ventrículo por debajo del nodo
AV (el complejo ventricular normal QRS empieza en el nodo AV). Puesto que las
contracciones prematuras no siguen la vía de conducción normal en el ventrículo,
muestran una configuración de QRS distinta y abigarrada en el ECG.
1.5.4.1.2 ECG de la CVP (extrasístole): aparecen en etapa temprana del ciclo (prematuras) y son más anchas que el latido
normal.
En el paciente con infarto, las contracciones ventriculares prematuras suelen recibir
tratamiento enérgico, porque pueden desencadenar la fibrilación ventricular si coinciden
con una onda T, son especialmente peligrosas cuando:
1. Son más de una por cada 10 latidos.
2. Ocurren en grupos de dos o tres.
3. Se producen cerca de la onda T.
4. Toman configuraciones diversas.
1.5.4.2 BIGEMINY VENTRICULAR
En esta arritmia, se presentan contracciones ventriculares prematuras CVP’s
intercaladas con latidos normales
1.5.4.3 TRIGEMINY VENTRICULAR Esta arritmia se presenta en el ECG, como una secuencia de un CVP por
latidos normales.
1.5.4.4 TAQUICARDIA VENTRICULAR:
Esta temida complicación del infarto del miocardio puede definirse como una serie de
contracciones ventriculares prematuras consecutivas (tres o mas), de una frecuencia
generalmente de 150 a 200 por minuto. La taquicardia ventricular es muy peligrosa
porque origina disminución de la actividad cardiaca, y muchas veces acaba en
fibrilación ventricular [9].
Vías normales y de la CVP (extrasístole): Como lo indica su nombre, las
contracciones ventriculares prematuras se originan en el ventrículo por debajo del nodo
AV (el complejo ventricular normal QRS empieza en el nodo AV). Puesto que las
aturas no siguen la vía de conducción normal en el ventrículo,
muestran una configuración de QRS distinta y abigarrada en el ECG.
P (extrasístole): Obsérvese que las contracciones prematuras
aparecen en etapa temprana del ciclo (prematuras) y son más anchas que el latido
Figura 1.26. ECG de la CVP
En el paciente con infarto, las contracciones ventriculares prematuras suelen recibir
amiento enérgico, porque pueden desencadenar la fibrilación ventricular si coinciden
con una onda T, son especialmente peligrosas cuando:
Son más de una por cada 10 latidos.
Ocurren en grupos de dos o tres.
Se producen cerca de la onda T.
iones diversas.
BIGEMINY VENTRICULAR
En esta arritmia, se presentan contracciones ventriculares prematuras CVP’s
intercaladas con latidos normales.
TRIGEMINY VENTRICULAR
sta arritmia se presenta en el ECG, como una secuencia de un CVP por
VENTRICULAR:
Esta temida complicación del infarto del miocardio puede definirse como una serie de
contracciones ventriculares prematuras consecutivas (tres o mas), de una frecuencia
200 por minuto. La taquicardia ventricular es muy peligrosa
porque origina disminución de la actividad cardiaca, y muchas veces acaba en
Como lo indica su nombre, las
contracciones ventriculares prematuras se originan en el ventrículo por debajo del nodo
AV (el complejo ventricular normal QRS empieza en el nodo AV). Puesto que las
aturas no siguen la vía de conducción normal en el ventrículo,
Obsérvese que las contracciones prematuras
aparecen en etapa temprana del ciclo (prematuras) y son más anchas que el latido
En el paciente con infarto, las contracciones ventriculares prematuras suelen recibir
amiento enérgico, porque pueden desencadenar la fibrilación ventricular si coinciden
En esta arritmia, se presentan contracciones ventriculares prematuras CVP’s
sta arritmia se presenta en el ECG, como una secuencia de un CVP por cada dos
Esta temida complicación del infarto del miocardio puede definirse como una serie de
contracciones ventriculares prematuras consecutivas (tres o mas), de una frecuencia
200 por minuto. La taquicardia ventricular es muy peligrosa
porque origina disminución de la actividad cardiaca, y muchas veces acaba en

1.5.4.4.1 Vías normales y vías de la taquicardia ventricularesquemas utilizados para indicar la vía de la CVP, ya que la taquicardia ventricular
puede considerarse como una serie de CPV. Como éstos, la taquicardia muestra una
configuración abigarrada en el ECG.
VÍAS NORMALES
(a) (b)
Figura 1.27. (a) Vía normal del impulso. (b) Vía del impulso en la taquicardia
1.5.4.4.2 ECG de la taquicardia la frecuencia es rápida y que el QRS es ancho (una anchura de tres o más pequeños
cuadros se considera anormal). Como las aurículas laten independientemente, en 20%
de los casos en que la frecuencia ventricular no es ex
ventriculares no son muy anchos, pueden verse ondas P independientes de los
complejos QRS.
Figura
1.5.4.5 FIBRILACIÓN VENTRICULAR:
Es muy importante saber reconocer este ritmo, pues e
paciente debe intuir de inmediato el tratamiento adecuado. Si la arritmia no se corrige,
el enfermo morirá en pocos minutos.
1.5.4.5.1 Vías normales y vías de fibrilación ventricular:puede considerarse que están originándose estímulos simultáneamente en gran número
de focos ectópicos ventriculares. Por tanto, no se produce una contracción eficaz del
músculo cardiaco y el paciente no tiene pulso.
Vías normales y vías de la taquicardia ventricular: estos
uemas utilizados para indicar la vía de la CVP, ya que la taquicardia ventricular
puede considerarse como una serie de CPV. Como éstos, la taquicardia muestra una
configuración abigarrada en el ECG.
VIAS DE LA TAQUICARDIA VENTRIULAR
(a) (b)
27. (a) Vía normal del impulso. (b) Vía del impulso en la taquicardia
ventricular
ECG de la taquicardia ventricular: se pude observar en esta patología que
la frecuencia es rápida y que el QRS es ancho (una anchura de tres o más pequeños
cuadros se considera anormal). Como las aurículas laten independientemente, en 20%
de los casos en que la frecuencia ventricular no es excesiva y los complejos
ventriculares no son muy anchos, pueden verse ondas P independientes de los
Figura 1.28. ECG de la taquicardia ventricular
FIBRILACIÓN VENTRICULAR:
Es muy importante saber reconocer este ritmo, pues el primer especialista que vea el
paciente debe intuir de inmediato el tratamiento adecuado. Si la arritmia no se corrige,
pocos minutos.
Vías normales y vías de fibrilación ventricular: En el corazón que fibrila,
iderarse que están originándose estímulos simultáneamente en gran número
de focos ectópicos ventriculares. Por tanto, no se produce una contracción eficaz del
músculo cardiaco y el paciente no tiene pulso.
son los mismos
uemas utilizados para indicar la vía de la CVP, ya que la taquicardia ventricular
puede considerarse como una serie de CPV. Como éstos, la taquicardia muestra una
VIAS DE LA TAQUICARDIA
27. (a) Vía normal del impulso. (b) Vía del impulso en la taquicardia
pude observar en esta patología que
la frecuencia es rápida y que el QRS es ancho (una anchura de tres o más pequeños
cuadros se considera anormal). Como las aurículas laten independientemente, en 20%
cesiva y los complejos
ventriculares no son muy anchos, pueden verse ondas P independientes de los
l primer especialista que vea el
paciente debe intuir de inmediato el tratamiento adecuado. Si la arritmia no se corrige,
En el corazón que fibrila,
iderarse que están originándose estímulos simultáneamente en gran número
de focos ectópicos ventriculares. Por tanto, no se produce una contracción eficaz del

VÍAS NORMALES
(a) (b)
Figura 1.29. (a) Vía normal del impulso. (b) Vía del impulso en la fibrilación
1.5.4.5.2 ECG de la fibrilación ventricularla irregularidad de los complejos. Una distorsión similar puede producirse también por
movimiento del paciente o de los alambres del monitor; por tanto, es necesario excluir
estas posibilidades. Si el paciente esta despier
es de fibrilación ventricular.
Figura
1.5.4.5.3 CPV que produce fibrilación cerca del vértice de la onda T (periodo vulnerable), puede desencadenarse la fibrilación
que aquí presentamos [8].
desfibrilación eléctrica y no la cardioversión, que puede emplea
otras arritmias. En la cardioversión, un choque eléctrico se sincroniza de manera que no
afecta la onda T, pues en tal caso el corazón pudiera entrar en fibrilación ventricular. En
la desfibrilación, el choque eléctrico es inmediato,
VIAS DE LA FIBRILACIONVENTRIULAR
(a) (b)
29. (a) Vía normal del impulso. (b) Vía del impulso en la fibrilación
ventricular
ECG de la fibrilación ventricular: se debe observar la distorsión completa
la irregularidad de los complejos. Una distorsión similar puede producirse también por
movimiento del paciente o de los alambres del monitor; por tanto, es necesario excluir
estas posibilidades. Si el paciente esta despierto, o si no lo esta y tiene pulso, el ritmo no
es de fibrilación ventricular.
Figura 1.30. ECG de la fibrilación ventricular
CPV que produce fibrilación ventricular: cuando una CPV se produce
cerca del vértice de la onda T (periodo vulnerable), puede desencadenarse la fibrilación
. Este ECG también explica por que motivo es necesaria la
brilación eléctrica y no la cardioversión, que puede emplearse para interrumpir
En la cardioversión, un choque eléctrico se sincroniza de manera que no
afecta la onda T, pues en tal caso el corazón pudiera entrar en fibrilación ventricular. En
la desfibrilación, el choque eléctrico es inmediato, pues no hay onda T en la fibrilación.
FIBRILACION
29. (a) Vía normal del impulso. (b) Vía del impulso en la fibrilación
observar la distorsión completa y
la irregularidad de los complejos. Una distorsión similar puede producirse también por
movimiento del paciente o de los alambres del monitor; por tanto, es necesario excluir
to, o si no lo esta y tiene pulso, el ritmo no
una CPV se produce
cerca del vértice de la onda T (periodo vulnerable), puede desencadenarse la fibrilación
Este ECG también explica por que motivo es necesaria la
rse para interrumpir
En la cardioversión, un choque eléctrico se sincroniza de manera que no
afecta la onda T, pues en tal caso el corazón pudiera entrar en fibrilación ventricular. En
pues no hay onda T en la fibrilación.

CAPITULO 2
ANALISIS DE VARIABILIDAD DE SEÑALES
La variabilidad en la actividad cardiaca vascular tal como el intervalo RR y la duración
de la repolarización ventricular (VRD) han sido ampliamente usadas como una medida
de la función cardiovascular. Esto es típico para esas señales que fluctúan en una base
pulso a pulso alrededor de su valor medio y las fluctuaciones son asociadas con la
regulación automática del corazón monitoreando las fluctuaciones observadas en la
fluctuación del corazón y el VRD que provee información concerniente a su regulación
automática y disturbios.
Para predecir un riesgo de eventos cardiovasculares adversos la medición analítica
primaria ha sido la variabilidad de la rata del corazón y el análisis QT. Anormalidades
en la fluctuación de la rata del corazón han sido mostradas para anteceder taquiarritmias
ventriculares espontáneas. Por ejemplo la baja variabilidad de la rata del corazón
predice el incremento de la mortalidad después de un infarto agudo al miocardio (IMA).
Datos clínicos y experimentales han mostrado que la prolongación del intervalo QT es
un factor de riesgo para arritmia ventricular y muerte cardiaca repentina en pacientes
con o sin IMA previos. El riesgo se incrementa debido a que la prolongación QT es
independiente de la edad, historia de IMA, rata del corazón y uso de droga. La
variabilidad de intervalos consecutivos RR ha sido usada tradicionalmente para acceder
al riesgo en pacientes en términos de mortalidad futura. Recientemente se ha hecho
énfasis en proteger la asimilación de los cambios dinámicos en la fase de repolarización
del corazón.
El sistema nervioso autonómico (ANS) regula el funcionamiento del corazón a través de
sus partes simpática y parasimpática. Esto es de interés para cuantificar la cantidad de
la fluctuación de la señal relacionada a esas dos partes del ANS separadamente y
también su balance en la rata del corazón entonces es afectada por factores tales como la
respiración, el sistema termo-regulador y el mecanismo regulador de la presión de la
sangre.

La variabilidad de la rata del corazón (HVR) ha sido estudiada extensivamente durante
los últimos años. El análisis del espectro de frecuencia de la señal de la rata del corazón
ha atraído la atención principalmente debido a su habilidad para exponer diferentes
fuentes de fluctuaciones y su poder para ilustrar el balance de la regulación autonómica
neural. Allí también existen varios parámetros ampliamente usados en el dominio del
tiempo que representan fluctuaciones en la rata y han puesto más énfasis en el análisis
no lineal de la variabilidad de la rata del corazón.
2.1 CAMBIOS DE VARIABILIDAD DE LA SEÑAL CONECTADOS A
EMFERMEDADES ESPECÍFICAS
Una disminución en la actividad neural vagal en el corazón puede resultar en un HRV
disminuido después del infarto del miocardio IM conducente al predominio de la
regulación neural simpática y a la inestabilidad eléctrica. La reducción de la
variabilidad de la rata del corazón es también asociado con un incremento del riesgo de
fibrilación ventricular y muerte cardiaca repentina. HUIKURI [10] concluyó que
cambios en las dinámicas del intervalo RR de periodo largo con intervalos RR alternos
pulso a pulso son probables para el inicio espontáneo de taquiarritmias ventriculares
sostenidas.
Enfermedades cardiacas tales como falla obstructiva del corazón, enfermedad de la
arteria coronaria y una hipertensión sencilla son también asociadas a un vagal reducido
y un mejorado tono simpático, el cual cambia las dinámicas de la variabilidad de la rata
del corazón. Porque el análisis HRV puede ser estimado como no invasivo,
reproducible y un método fácil de usar para reflectar los grados de control autonómico
del corazón, esto ha sido ampliamente usado para diagnosticar la disfunción autonómica
debido a neuropatía diabética.
Aunque el HRV es usado en un amplio rango de aplicaciones clínicas, el HRV
disminuido solo ha sido generalmente aceptado como un pronosticador de riesgo
después de un infarto del miocardio agudo y de una temprana neuropatía diabética. El
HRV disminuido pude pronosticar mortalidad y eventos de arritmia independientemente
de otros factores de riesgo y después de un infarto agudo del miocardio y el termino

largo análisis HRV ha admitido ser el más certero pronosticador comparado con un
análisis de corto termino. La variabilidad de la rata del corazón podría también ser
unida a otros factores de riesgo así como a mejoras del uso predictivo.
Cualquier enfermedad del corazón (hipertrofia ventricular izquierda, falla del corazón)
puede modificar la duración de la repolarización. Anomalías en la duración de la
repolarización son signos de la inestabilidad eléctrica en el corazón y pueden conducir a
arritmias malignas tales como fibrilación ventricular. Análisis de las dinámicas de la
duración de la repolarización ventricular proveen información esencial en una
predisposición de arritmias ventriculares, porque algunas arritmias son una amenaza
para la vida pues aumentan el tejido miocardial. Dinámicas alteradas del VRD y los
eventos de amplitud de la onda T alternante particularmente en pacientes con el
síndrome de QT largo como también con la enfermedad estructural del corazón en ratas
del corazón rápidas, sugieren que el análisis de las dinámicas de la repolarización
ventricular puede proveer una importante herramienta clínica.
2.2 SERIES DE TIEMPO EN INTERVALOS RR
El procedimiento básico usado para determinar la rata del corazón y sus fluctuaciones es
descrito a continuación. Un electrocardiograma (ECG) es medido, usando equipo
apropiado de adquisición de datos, el tiempo transcurrido entre los pulsos consecutivos
del corazón es definido entre 2 ondas P, donde una onda P describe la fase de
despolarización auricular. En la práctica, este es el complejo QRS que es usado para
obtener el periodo de tiempo entre los pulsos del corazón. Este complejo es detectado
en la onda R, pues esta tiene una amplitud muy clara y mejor resolución de frecuencia
que la onda P, y una mejor proporción señal-ruido. El intervalo de tiempo entre las
ondas P y R puede ser asumido constante.
Definiendo las veces de ocurrencia de 2 ondas R consecutivas como s (t) y s (t+1), con
t = 1,2,...,N, la expresión x(t)= s(t+1)-s(t) es obtenida para un periodo de tiempo en
milisegundos. X(t) es llamada la serie de tiempo del intervalo RR o los tiempo a los
cuales esta se refiere son simplemente llamados intervalos RR. Una serie de tiempo de
la rata del corazón (min-1
) puede ser obtenida por y(t)= 1000*(60/x(t)) y la rata media
del corazón es simplemente

,
Esta fórmula (1) indica una relación no lineal entre los valores de una serie de tiempo
dada, la cual debería ser tomada en cuenta cuando se comparan los resultados obtenidos
para aproximaciones del dominio tiempo-frecuencia. En el momento, los intervalos
RR parecen ser la serie de tiempo más frecuentemente usada en el análisis de
variabilidad de la rata del corazón (HRV). Para una discusión de la elección entre
diferentes series de tiempo (tacograma) ver Janssen (1993) [6].
2.3 SERIES DE TIEMPO VRD
El intervalo de tiempo QT en señales electrocardiográficas ha sido usado para ejecutar
tanto análisis estático como dinámico de la duración de la repolarización ventricular.
Allí existen dificultades en la detección del inicio (onset) de la onda Q y la
compensación (offset) de la onda T debido a la escasa proporción señal-ruido y diversas
morfologías ECG. Por esas razones otros estimados, tales como el intervalo RTmax, han
sido ampliamente usados. Además, este provee una motivación para investigar y
comparar la sensibilidad del ruido de diferentes intervalos QT estimados. Porque el
intervalo de tiempo Q-S es resultado del periodo de despolarización de los ventrículos,
está es actualmente más correcta para medir el intervalo de tiempo entre las ondas R y T
como un interés en los cambios ocurridos dentro del periodo de repolarización
ventricular. La onda R ha sido usada para estimar el inicio del periodo de
repolarización porque buscar la compensación (offset) de la onda S puede ser difícil. El
máximo (pico) de la onda T ha sido con frecuencia estimado como confiable para el fin
del periodo de repolarización que la compensación (offset) de la onda T. La duración
de la repolarización total, es el intervalo de tiempo entre las compensaciones (offsets) de
las ondas S y T.
El ECG ambulatorio es usualmente adquirido con una frecuencia de muestreo de 128
Hz dando una resolución de tiempo de 7.81ms por cada muestra, la cual es demasiado
baja para medidas de variabilidad del intervalo T. Esto ha sugerido que el intervalo QT

debería ser determinado con mínimo una resolución de 1 ms, lo cual podría requerir una
frecuencia de muestreo de 1 kHz para una señal ECG.
2.4 DETECCION DE LA FORMA DE ONDA DEL ECG
Los intervalos RR y QT adquiridos fueron basados en una implementación de un
algoritmo descrito previamente y el esquema de detección será repasado brevemente en
este documento. El concepto básico del algoritmo es observar los puntos que cruzan
por cero, los cruces de valores umbral son determinados experimentalmente como
también los valores máximo o mínimo de la señal ECG diferenciada d(t) y su versión
filtrada pasa bajo f(t).
El diagrama de flujo del procedimiento de detección de la forma de onda implementada
es el siguiente: El primer paso es calcular las señales de d(t) y f(t), lo cual está hecho
para el periodo completo del ECG seleccionado para el análisis. El procedimiento de
detección de la forma de onda continúa por determinar el valor inicial del valor umbral
Hn usado para buscar el valor máximo absoluto del QRS en la señal f(t). El valor de
umbral Hn + 1 es continuamente actualizado durante la detección de la forma de onda
usando la ecuación (2):
Hn+1 = 0,8*Hn + (0,16*│f (PKn) │) , (2)
Donde │f (PKn) │ es el valor absoluto de la señal f(t) en la posición de la onda R
fiduciaria obtenida del pulso n.
La inicialización del promedio de los intervalos RR y RRav y el primer valor del
intervalo RR son obtenidos. El valor RRav es usado después para chequear el valor
calculado de un nuevo intervalo RR y así proveer unas bases para identificar el
complejo QRS.
La posición inicial del complejo QRS es detectada usando un método de umbral
adaptable determinado por el valor promedio del intervalo RR. Después de esto, el
algoritmo continúa buscando la posición de la onda R. En la presente aproximación, el
punto fiduciario de la onda R fue detectado usando 3 métodos: la máxima amplitud
arriba o debajo de la línea base, o el punto de cruce por cero de la señal f (t) durante el

complejo QRS. La última técnica nos dice que en algunos casos una definición más
exacta se puede obtener si el punto ficticio de la onda R puede ser definido en la
máxima amplitud positiva de QRS con este algoritmo una determinación exacta de la
onda R es una condición absolutamente necesaria para una detección de la onda Q
confiable.
Después de detectar la posición de la onda R y actualizar un umbral de la onda Hn y
RRav, el onset de la onda Q es buscado manteniendo la posición de la onda R como
punto de referencia. Aquí se debe mencionar que el examen del patrón de la onda Q es
hecho por el análisis de la señal diferenciada d (t) y no de la señal f (t) porque la señal
d (t) contiene componentes de alta frecuencia de la onda Q.
A continuación el máximo de la onda T y el final de la misma son detectados de la
señal f(t). La siguiente definición para los límites de una ventana de búsqueda
calculada de la posición de onda R que fue usada es (3):
(bwind, ewind) = (a * RRav, b * RRav) , (3)
Donde a y b son valores de parámetros en el procedimiento. Esta definición es una
ligera diferencia de lo dado por Laguna [11]. Como el umbral para el fin de la onda T
fue usado para valores Hs = f(Ti)/2, Ti denota la posición de la máxima pendiente
descendente o ascendente después del máximo de la onda T.
Finalmente un valor del intervalo QT es calculado usando la relación
QT(n) = Tend(n) - QTonset(n), donde Tend y QTonset son las posiciones del fin de la onda
T y el onset del intervalo de tiempo de la onda QT durante el pulso n. El análisis del
próximo pulso cardiaco es iniciado 150 ms después de que el último fin de onda fuera
fijado.
2.4.1 CAMBIOS NO PERIODICOS EN EL INTERVALO RR
Métodos de análisis matemático convencional tal como desviación estándar, correlación
y análisis del espectro de frecuencia suponen que los datos son estacionarios en un
amplio sentido. Esto significa que en el caso del análisis el ritmo sinus del corazón

puede ser aproximadamente estable. Esta aproximación se cumple mejor en periodos
cortos y bajo condiciones de estado estable. Cambios no periódicos en el ritmo del
corazón pueden deteriorar la estacionariedad de la señal y tener efectos adversos en
índices HRV.
2.4.2 CORRECCION DE INTERVALOS RR ANORMALES
La decisión de como una variación del intervalo podría ser corregida o no, forma el
paso más difícil en los intervalos anormales eliminados. Un segmento de una serie de
tiempo del intervalo RR es aceptado para análisis precisos si el número de intervalos
calificados excede un porcentaje de tolerancia programado los cuales varían
ampliamente de acuerdo a la aplicación y clase de paciente.
Figura 2.1. Series de tiempo. Arriba muestra un cambio abrupto de los intervalos RR.
Abajo a la izquierda un espectro de energía hallado con el método de covarianza
modificada con un modelo de orden 20. Abajo a la derecha diferencia de orden 1
dibujada de los intervalos RR. [12]

2.5 ANALISIS EN EL DOMINIO DEL TIEMPO
Análisis en el dominio del tiempo de series de tiempo del intervalo RR cubren
histogramas y análisis de scattergrama (diagramas de dispersión), y el cálculo de varios
índices estadísticos comunes.
Cuando se trabaja con la interpretación de parámetros tales como histogramas, se
deberían apuntar aquellos que en general no tienen alguna información en fluctuaciones
periódicas en los intervalos RR. La frecuencia respiratoria, por ejemplo, no puede ser
observada en las bases de esos parámetros, la varianza relacionada a una especifica
frecuencia de banda (componente espectral) no puede ser medida por sus índices, sin
intervalos RR cualquier filtro pasa banda es considerado. Los índices de dominio de
tiempo pueden tender a medir el cambio de la variabilidad del promedio en series de
tiempo o amplitud máxima de la variabilidad dependiendo de la naturaleza del índice
considerado.
2.5.1 INDICES DEL DOMINIO DEL TIEMPO
Hay varios índices estadísticos los cuales han sido usados para describir la variabilidad
de la rata del corazón, por ejemplo, promedio medida proporcional, desviación entre
valores máximo y mínimo (rango), de desviación estándar (SD) y la raíz media
cuadrada de diferencias sucesivas (RMSSD). La formulación de eso es bien conocida y
ellos no requieren cálculos complejos.
Las propiedades estadísticas de una serie de tiempo x(t) son a menudo índices básicos
tales como medio y desviación estándar Sx los cuales pueden ser obtenidos de datos
dados como sigue en (4):
(4)

La varianza es el cuadrado de la desviación estándar, var(x(t)) = sx2. El coeficiente de
variación y el rango, estos son la desviación entre los valores máximo y mínimo en una
serie de tiempo formulados como (5) y (6):
El promedio cuadrado de diferencias sucesivas (RMSSD) es calculado para los
propósitos de análisis HRV por (7):
2.5.2 ANALISIS DE DISTRIBUCIÓN
La distribución de intervalos RR puede ser analizada en términos de un histograma de
la serie de tiempo en la cual las "frecuencias" en el histograma depositadas pueden ser
expresadas en números absolutos o como "frecuencias" relativas de valores de serie de
tiempo, el histograma también ha sido presentado dibujando una línea entre los
contenedores (Bin) depositados dando las porciones de valores de series de tiempo
numéricamente.
Pocos parámetros generados por el análisis de histograma del intervalo RR son
introducidos en Baevskij (1984)[13]. El Bin teniendo la más larga "frecuencia" es
llamado modo de histograma y la "amplitud" de este modo también ha sido cerrada. El
ancho del histograma de la desviación máxima en valores de serie de tiempo fue
propuesto como otra medida básica de la variabilidad del intervalo RR, varios
parámetros pueden ser construidos de esas tres medidas elementales.
CASOLO (1989) [14] uso el ancho del histograma base como una medida de la
variabilidad total, y fijo el ancho en niveles de 10% y 50% de la altura máxima del
histograma. Odemuyiwa (1991) [15] aproximó la forma del histograma como un
triángulo para reducir el efecto de menos variabilidad marcada.

Los resultados producidos por el histograma naturalmente dependen del ancho del
contenedor (Bin) usado. Si un contenedor (Bin) grande es escogido, el histograma será
impreso en su forma. Mientras que un contenedor (Bin) de ancho corto acentuara
detalles poco importantes. Es notorio que el ancho del bin de un histograma debería
permanecer constante en virtud de permitir comparaciones racionales de resultados
absolutos. Un simple estimado para un ancho de bin es dado por (8):
hN = 3.49 * sx / N3 , (8)
Donde Sx es la desviación estándar de valores de N series de tiempo. El estimado toma
la variabilidad en series de t en cuanto es usada la desviación estándar. Esta expresión
puede ser usada exitosamente con datos de aproximación Gaussiana.
2.6 ANALISIS EN EL DOMINIO DE LA FRECUENCIA
2.6.1 INTERPRETACIÓN DE LA ESTIMACIÓN ESPECTRAL
Estimados espectrales pueden ser estudiados integrando sobre una frecuencia de banda
dada por descomposición del espectro en componentes. La primera aproximación puede
ser ejecutada con Fourier y técnicas auto regresivas (AR), pero la ultima es posible solo
con técnicas AR.
Un problema que afecta la integración del espectro es la definición de las bandas de
frecuencia. Haciendo esto las señales podrían ser realmente una tarea fabulosa, porque
esto chequeara el promedio de todos los estimados manualmente. Los rangos de
frecuencia pueden ser definidos por un procedimiento experimental y obtenidas desde
una literatura y observación constante pero problemas se originan cuando la
localización de los componentes varía entre las señales [16].
El uso del procedimiento de descomposición del espectro da estimados para los
componentes del espectro de energía. En adición las frecuencias centrales también
como la energía estimada pueden ser utilizadas para la búsqueda de los componentes
apropiados. Se usa el máximo del espectro de componentes y el ancho de banda del
componente para detectar fluctuaciones periódicas [17]. El promedio, frecuencia

mediana y central han sido usados para obtener la frecuencia característica de una banda
específica [18]. Varias definiciones existen para las frecuencias de los componentes en
un espectro de series de tiempo del intervalo RR, como resumimos en la siguiente
descripción corta:
- Los componentes de muy baja frecuencia (VLF) son encontrados en frecuencias
f < 0,04 Hz [19]. Estas fluctuaciones en intervalos RR son debidos a
mecanismos de termorregulación. Algunas bajas frecuencias tendientes o no
estacionarias también pueden existir, lo cual puede ser observado en la forma de
energía aumentada en bajas frecuencias en el espectro.
- El componente de baja frecuencia (LF) es usualmente observado encontrando
f = 0,1 Hz. Esto es principalmente debido al sistema regulatorio de la presión de
la sangre y refleja el tono simpático autonómico de la regulación de la rata del
corazón, aunque esto también ha sugerido que la regulación parasimpática toca
algún papel en este [20].
- El componente de alta frecuencia (HF) será encontrado a menudo en la banda de
frecuencia 0,15 < f < 0,4 Hz, el cual es relacionado a la frecuencia de respiración
(por ejemplo duración del ciclo T = 4s, f = 0,25 Hz). La amplitud y frecuencia
de este componente están estrechamente relacionados al volumen de la
respiración y frecuencia. El componente HF ha sido considerado una medida de
regulación neural parasimpática de la rata del corazón [21].
Algunas veces una ultra baja frecuencia (ULF) es definida con una banda de frecuencia
de f < 0,0033 Hz [19]. El balance entre la regulación neural simpática y parasimpática
es a menudo medido por la proporción de la energía estimada para los componentes LF
y HF [21]. Una serie de tiempo RR para un sujeto joven saludable se muestra en la
figura 3.1, conjuntamente con un espectro estimado usando un modelo AR, mostrando
los componentes de fluctuaciones RR espontáneas descritas anteriormente y un
diagrama de polos del modelo paramétrico en el complejo plano Z. En este ejemplo, el
orden del modelo fue seleccionado por inspección visual del espectro, cuando el orden
16 dio un resultado razonable el espectro de potencia estimado representa la suma del

espectro (línea sólida) y el espectro de los componentes separados relacionados a
respectivos polos pares (líneas fracasadas).
Figura 2.2. (Arriba)Serie de tiempo RR obtenida de un joven sano en condición pasiva.
(Abajo izquierda) Espectro de energía estimado por el método de covarianza
modificada con un modelo de orden 16. (Abajo derecha) El correspondiente diagrama
de polos.
2.6.2 EN EL USO DEL ANÁLISIS ESPECTRAL
El uso del análisis del dominio de la frecuencia en diferentes circunstancias clínicas ha
sido ampliamente revisado [19]. El análisis espectral ha sido a menudo efectuado para
series de tiempo del intervalo RR incluyendo 256 o 512 valores. Análisis de esta clase
pueden proveer información en fluctuaciones de periodo corto en intervalos RR.
Fluctuaciones de periodo corto y sus cambios pueden ser estudiados con grabaciones
ambulatorias, en una grabación larga siendo distribuida en series de tiempo de muy
cortos intervalos de 512 valores [22]. Tales series de corto tiempo pueden ser asumidas

para confirmar mejor el requerimiento estacionario para la estimación del espectro
relevante.
2.6.3 PROCESO MATEMÁTICO DEL ANÁLISIS ESPECTRAL.
Las series de tiempo del intervalo RR incluyen información de origen amplio y su
naturaleza permitirá apenas una suposición de amplio sentido estacionario en el estricto
sentido, bajo cualquier condición. Los intervalos RR deberían ser comprendidos como
aproximadamente estacionarios o más, con lo cual el análisis podría dar resultados
relevantes en un sentido médico. Pueden existir secciones las cuales sean muy bien
asumidas para ser estacionarias (casi), y también secciones que están lejos de permitir
tales suposiciones. Esto es a menudo necesario para dividir una grabación en
secuencias estacionarias más cortas. No estacionariedades incluyen fenómenos
transitorios y los cambios varían lentamente (tendencia), la identificación de la cual es
más difícil. La teoría de muchas aproximaciones es no obstante basada en la suposición
de la señal estacionaria. En este contexto un espectro calculado para series de tiempo
del intervalo RR, por ejemplo, es comprendido como un “modelo” para fluctuaciones
periódicas, más bien que como espectro “real”.
Dejar a x (t) ser un proceso estacionario definido en valores discretos t = 0, ±±±±1, ±±±±2,....
La función autocovarianza se escribirá como en (9) [23]:
r(k) = E{ (x(t) – µ) (x(t+k) – µ) } , k = 0, ±1, ±2, … (9)
Y la función de autocorrelación será entonces ρ(k) = r(k) / r(0). Aquí el valor
promedio del proceso x(t) es definido usando el operador de expectación µ = E{x(t)} .
Para un sentido amplio del proceso estacionario, el valor promedio es constante y la
autocorrelación satisface la propiedad p(n1,n2) = p(n1- n2) = p(k).
Dejándonos entonces asumir que x(t) es un cero promedio del proceso estacionario.
Allí debe entonces existir un proceso ortogonal Z(s) tal que (10) [23]:

Y E{ ІdZ(ω) І2} = dH(ω), donde dH(ω) = h(ω)dω, -π ≤ ω ≤ π y ω = 2πf. Esta
es llamada la representación espectral de un proceso estacionario discreto. La secuencia
de autocovarianza es como (11):
Y la densidad de potencia espectral es (12):
2.6.4 ESTIMACION DEL ESPECTRO USANDO UN PERIODOGRAMA
Se dejan dividir los N puntos del proceso x(t) en segmentos K no traslapados, cada uno
teniendo M puntos. La transformada de Fourier del segmento p: th se puede escribir
como en (13):
El periodograma estimado de la función de densidad espectral de un simple dato de
segmento es dado por (14):
Si los periodogramas de segmentos K son promediados el estimado es llamado un
periodograma promediado Bartlett. El periodograma es solo una forma de estimar el
espectro del proceso y no significa una “definición” del espectro.
Modificaciones del periodograma promediado también existen, en medio de las cuales
los periodogramas Welch son introducidos. En este método, los datos de segmentos son
permitidos a traslapar por 50% o 70% por ejemplo, y cada dato del segmento será
cargado con una función ventana antes de calcular el periodograma. Como resultado,
uno tiene para el periodograma de cada segmento a (15):

El factor es un factor de normalización para la energía en la
t = 1 función ventana ω(t). El periodograma Welch estimado será entonces un
promedio de esos periodogramas en (16) [23]:
Algunas veces uno puede necesitar aproximar un periodograma más cerradamente, el
cual puede ser hecho usando el procedimiento de zero padding (amortiguado en cero)
[24]. Este es ejecutado por extensión del conjunto de datos con ceros y tomando la
transformada de Fourier del conjunto de datos completo. Esta operación no consigue
mejor resolución en el espectro, sin embargo, aunque la frecuencia de espaciado será
densa, el zero padding actualmente interpola los valores del espectro de medida en más
frecuencias, produciendo un espectro suave.
2.6.5 MODELAMIENTO PARAMETRICO DE SERIES DE TIEMPO
El modelamiento paramétrico de las series de tiempo tiene algunas ventajas sobre
métodos no paramétricos (Fourier). Aquí solo son examinados modelos autorregresivos
(AR) y el foco está en la estimación espectral, la cual ha sido el principal objeto de
interés en el análisis HRV. Hay muchos algoritmos para obtener estimados para
parámetros AR, por ejemplo, métodos basados en estimación de la secuencia de
autocorrelación, el algoritmo burgo, y algoritmos de predicción lineal del mínimo
cuadrado (incluyendo el método de covarianza modificada) [24]. Hay también
algoritmos adaptables tales como el mínimo medio cuadrado (LMS) y el recursivo
mínimo cuadrado (RLS), el cual actualiza los parámetros estimados como un nuevo
dato de muestreo llegando a ser posible [25].

2.7 ANALISIS TIEMPO FRECUENCIA
2.7.1 REPRESENTACION TIEMPO-FRECUENCIA
Allí puede estar una necesidad para monitorear las propiedades espectrales de la señal
como tiempo transcurrido, especialmente, cuando periodos de tiempo “largos” están
bajo consideración. La ubicación temporal de los componentes espectrales puede dar
más información que un espectro simple. La transformada de Fourier de tiempo corto
(STFT) es una representación lineal tiempo-frecuencia (TFR) usada para presentar
cambios en la señal que varía con el tiempo. La transformada de Fourier no muestra
explícitamente la ubicación en el tiempo de los componentes de frecuencia, pero alguna
forma de ubicación en el tiempo puede ser obtenida usando una pre-ventana adecuada
[26]. El STFT puede ser definido para x(t) como en (17):
es un espectro local de la señal X(s) alrededor del análisis de tiempo S. Las
propiedades de la ventana g*(s) también tienen un efecto en el cálculo STFT [26].
La resolución tiempo-frecuencia es limitada por el producto tiempo-frecuencia, esto es,
tener una resolución de corto tiempo significa resolución de frecuencia mala, o
viceversa. La resolución es también constante como una función de la frecuencia la
cual es debida a la ventana elegida para el STFT [27].
2.7.2 ANALISIS ESPECTRAL TIEMPO-VARIANTE
Técnicas han sido desarrolladas recientemente y permiten el rastreo de parámetros
espectrales como el tiempo transcurrido. Aproximaciones de este tipo han sido
llamadas análisis espectral tiempo-variante o análisis tiempo-frecuencia [28 – 22 – 29].
Las ventajas de esas metodologías son asociadas principalmente con la reducción de
influencias no estacionarias.

Un procedimiento de arreglos espectrales comprimidos (CSA) puede reducir el dato
espectral obtenido de grabaciones ECG [22]. El método se basa en el cálculo de
estimados espectrales AR para segmentos sucesivos de intervalos RR, y chequea si un
nuevo espectro difiere significativamente desde el anterior.
En el análisis espectral tiempo-variante los parámetros AR son estimados por la
aproximación del cuadrado mínimo recursivo (RLS), y el espectro de potencia tiempo-
variante es dado como (18) [29]:
Con y t denota el índice de tiempo.
Mainardi et al. (1994) [30] introdujo 2 algoritmos para rastreo recursivo de los
desplazamientos de polos de un modelo AR estimado. Los algoritmos fueron basados
en la aproximación de linealidad básica y cálculo recursivo de las raíces de un
polinomio.
La transformada de Fourier autorregresiva y representación tiempo-frecuencia (TFR)
[31], basada en estimadores de potencia espectral aplicada a series de tiempo no
estacionarias muestra que TFRs tales que SPWD (distribución suavizada falsa pseudo
Wigner) y RWED (distribución exponencial de ventaneo que fluye) debería ser utilizada
cuando una buena resolución del tiempo o la presentación de la potencia instantánea es
esencial. El RWED ha podido ser eficiente en la reducción de amplitudes de periodo-
cross, pero el SPWD es más capaz de evaluar la energía promedio en el plano tiempo-
frecuencia. Puede también concluirse que un problema detallado en las estimaciones
clásicas es la dependencia de la resolución del tiempo para las oscilaciones observadas
en series de tiempo cardiovasculares.
Está siendo mostrado un aumentado interés en el análisis espectral tiempo-variante o el
monitoreo de parámetros espectrales como una función del tiempo. Esas técnicas
parecen ofrecer aproximaciones para superar el requerimiento de la señal estacionaria.

2.8 ANALISIS WAVELET
La transformada Wavelet (WT) es una aproximación bastante nueva en el campo del
análisis de las series de tiempo biomédicas, y solo unos pocos artículos publicados
existen en el uso de análisis HRV, esto casi parece poseer algunas ventajas obvias sobre
el método de análisis clásico tiempo-frecuencia [32]. La motivación para explicar la
transformada wavelet en el análisis de la señal ECG y series de tiempo del intervalo RR
yace principalmente en el monitoreo de señales no estacionarias y la evolución del
periodo largo del espectro de potencia.
La WT fue una herramienta en la aproximación del análisis espectral tiempo-dependiente para
procesos estocásticos, especialmente el término “frecuencia”· en conexión de series de tiempo
no estacionarias. Debido a que los métodos explicados anteriormente son muy limitados
en cuanto a la robustez frente al ruido, artefactos y desviaciones de la línea base, la WT
es la más usada y segura en la detección de ondas del ECG [32, 33].
2.8.1 TRANSFORMADA WAVELET DISCRETA
Por elección de valores fijos, a = a0m y b = nb0a0
m, m,n = 0, ±1, ±2, . . . , nosotros
obtenemos para la transformada wavelet discreta (DWT) (19) [34]:
Los valores a0 = 2 y b0 = 1 construyen wavelets discretos ψm,n(t) = 2-m/2ψ(2-mt – n)
usado en análisis multirresolución constituyendo bases normales para L2 (R).
Para obtener una caracterización completa de x(t) usando wavelets discretizados
ψm,n(t), y más aún, a recobrar x(t) desde la transformada discreta en una manera
numéricamente estable, la función wavelet podría constituir un marco. La transformada
entre la señal y la función wavelet será saltada encima y debajo

con A>0 y B<∝∝∝∝ si el marco de salto A y B son iguales entonces el marco es llamado
apretado.
2.8.2 ANALISIS WAVELET MULTIRESOLUCION
En el análisis multiresolución sucesivas aproximaciones de subespacios cumplen la
propiedad Vj C Vj+1 con (21):
el aspecto multirresolución cumple la condición de que todos los espacios son versiones
escaladas del espacio central V0 (22):
x(t) ∈∈∈∈ Vj ⇔ x (2j .) ∈∈∈∈ V0 .
El espacio Vo tiene que ser variante bajo una traslación completa en (23):
x(t) ∈∈∈∈ V0 ⇔ x(. – n) ∈∈∈∈ V0
para todo n ∈∈∈∈ ZZZZ. Una función escalamiento φφφφm,n(t) ∈∈∈∈ V0 es también requerido el cual es
una base normal en Vo, donde φφφφm,n(t) = 2-m/2φφφφ((((2-mt-n).... Bajo esas suposiciones el
esquema multiresolución implica unas bases wavelet normales L2(R).
ψψψψm,n(t) = 2-m/2 ψψψψ((((2-mt-n), así que (24):
donde Pm es la proyección normal en el espacio Vm. La señal x(t) es obtenida
consecuentemente por (25):

La descomposición de la señal x(t) usando funciones ψψψψj,k(t) del análisis wavelet discreto
y funciones φφφφK,k(t) escalares discretas pueden ser dadas en diferentes escalas como
sigue en (26):
donde dj(k) son coeficientes wavelet (señales detalladas) en escala 2j y aK(k) son los
coeficientes escalares (señal aproximada) en la escala 2K. En la figura 2.3, la idea del
análisis wavelet discreto es presentada por medio de una descomposición de árbol
(ramificada) de wavelet. Una descomposición sobre escalas diádicas asociadas al
contenido de la señal y escalas como (27):
2-j ππππ ≤ ΔωΔωΔωΔωj j j j ≤≤≤≤ 21-j ππππ
para j = 1, 2, .... El espectro de señal incluye el rango 0 - ππππ rad y ΔωΔωΔωΔωjjjj es la banda
de frecuencia correspondiente al nivel j.
2.8.3 FILTRADO SUBBANDA
Análisis multiresolución comprenden un esquema jerárquico y rápido para computar los
coeficientes wavelet de una señal analizada. El esquema involucra la computación de
aproximaciones secuenciales bruscas x(t) y la diferencia de señales de dos niveles
consecutivos. En la aproximación del filtrado sub-banda la computación consiste de los
análisis y de las síntesis de los pasos los cuales corresponden a las etapas de
reconstrucción y descomposición en análisis wavelet [35]. La transformada de wavelet
discreta puede ser implementada por el escalamiento (pasa bajo) y filtros wavelet (pasa
altos) así (28):
y (29):

Figura 2.3. Descomposición de una señal Wavelet presentada por una estructura de árbol
Siendo filtros de cuadratura del reflejo complementario QMF [34]. La estimación del
detalle de la señal en el nivel j será hecho por convolución de la señal aproximada al
nivel j-1 con los coeficientes g(n). La convolución de la señal aproximada al nivel j-1
con los coeficientes h(n) da un estimado para la señal aproximada al nivel j. El análisis
de paso (etapa de descomposición) involucra filtrar la señal aproximada y retiene cada
siguiente muestra del filtro de salida (submuestreo). La síntesis de paso involucra
sobremuestrear y filtrar para obtener una señal reconstruida. En la figura 2.4 son
presentadas las etapas de reconstrucción y descomposición en un esquema de filtrado
sub-banda estableciendo un banco de filtros.

Figura 2.4. Esquema de procedimiento de filtrado sub-banda usando
bancos de filtros.

CAPITULO 3
APLICACIÓN AL ANÁLISIS DE VARIABLIDAD EN SEÑALES
CARDIOVASCULARES
En el capítulo anterior se mencionaron algunos de los distintos métodos utilizados en el
análisis automático de la señal ECG. También se concluyó que el método más usado en
la actualidad es el análisis de Wavelets por su robustez en el filtrado y la ganancia que
ofrece en sistemas computacionales.
En este capítulo presentaremos un algoritmo para realizar el análisis de la señal
electrocardiográfica de forma automática y mostraremos los diferentes intervalos que
ofrece una señal de este tipo, determinando algunas tendencias hacia posibles afecciones
cardiacas.
3.1 ALGORITMO DE FILTRADO DE LA SEÑAL
Un factor crucial en el análisis de la transformada Wavelet es la elección del nivel de
descomposición puesto que la escogencia de un nivel de descomposición bajo no
permitirá una buena segmentación de la señal y si por el contrario escogemos un nivel
muy alto se puede destruir la señal, eliminándose componentes frecuenciales relevantes
de la señal misma [42].
La dificultad existente con la línea base es que un nivel demasiado bajo para esta
provocará una sobre-aproximación de la señal por lo cual se incluirían algunas ondas
electrocardiográficas además de esta, mientras que si el nivel es demasiado elevado la
estimación de la línea base se aleja demasiado y los resultados no serán satisfactorios.
Por lo tanto se busca una buena aproximación (nivel 8) [36] para lograr su eliminación.
Por último, para remover interferencias de la red se tomará el nivel 3 de
descomposición[43].

3.2 ALGORITMO PARA DETECTAR ONDAS CARACTERÍSTICAS
Utilizaremos la base de datos MIT-BIH para tomar las señales que estudiaremos en este
trabajo puesto que esta nos brinda una gran cantidad de señales de alta calidad y tienen
un diagnóstico ya estudiado. Cada señal consta de tres archivos hea (cabecera), dat
(señal) y atr (anotaciones).
En este estudio realizaremos tres procedimientos fundamentales (Ver figura 3.1):
• Detección de QRS: se obtendrá el ciclo de marcadores cardíacos.
• Obtener inicios y finales de P y T: se obtendrán segmentos, duraciones y
amplitudes.
• Procesado final de los datos y deducciones.
3.3 DETECCION DEL COMPLEJO QRS
El complejo QRS se detecta por medio del módulo máximo de la transformada Wavelet,
este se define como cualquier punto Wf (2 j, τ0) tal que:
• | Wf (2 j, τ) | < | Wf (2
j, τ0) | con τ perteneciente a la izquierda o la derecha de
los alrededores de τ0. y
• | Wf (2 j, τ) | ≤ | Wf (2
j, τ0) | con τ perteneciente a otro punto de los alrededores
de τ0.
Así el complejo QRS produce 2 módulos máximos con signos opuestos de Wf (2 j, τ),
con un cruce por cero entre ellos como se indica en la figura 3.2.
El complejo QRS tiene su mayor energía entre los 3 Hz y los 40 Hz; observando
alrededor de 3 dB las frecuencias indican que la mayor parte de su energía se halla entre
las escalas 21 y 2
2 [44, 45]. A partir de 2
2 se nota un descenso y después de 2
5 se

incrementa la energía de artefactos debidos al movimiento y error de la línea base. Por
esto se eligen escalas de 21 a 2
4 para la Wavelet. [11].
Figura 3.1. Algoritmo para detección de variabilidad cardiovascular.

Figura 3.2. Escala 21 de la transformada Wavelet
Como ya se ha mencionado, el complejo QRS produce 2 módulos máximos con signos
opuestos de la transformada Wavelet. El cruce por cero entre los 2 máximos
corresponde a la onda R y se determina así [37]:
1. Se determinan y marcan posiciones de los módulos máximos de la escala 21 que
cruzan el umbral Th4.
2. Se determina el modulo máximo en la cercanía de nk4 en la escala 2
3 y se marca
su localización como nk3. Si existen muchos módulos máximos se selecciona el
más grande y si no existen nk3, nk
2 y nk
1 se envían a 0.
3. Se determinan en sus escalas la localización de los módulos máximos de las
escalas nk1, nk
2, nk
3 y nk
4, esto reducirá el ruido de alta frecuencia.
En ocasiones aparecen latidos ectópicos en lo cuales pueden ocurrir 2 o más módulos
máximos de los cuales 1 es útil; entonces se aplica la siguiente regla para saber cual de
estos extraer [38]:
1. Sí A1/L1 > 1.2 A2/L2, MIN2 es redundante.
2. Sí A2/L2 > 1.2 A1/L1, MIN 1 es redundante.
3. Sí MIN1 y MIN2 están en el mismo lado de los máximos, entonces el mínimo a
la distancia más grande del máximo es redundante.

Habiendo calculado el módulo máximo de la escala 21, estima el módulo máximo
negativo de la misma, así al tener los dos puntos se encuentra el cruce por cero entre
ellos, que equivale al pico de la onda R, usado para el cálculo de la frecuencia cardiaca.
En el algoritmo se debe calcular el umbral para los sucesivos complejos QRS, para esto
se utiliza el parámetro Ajm+1
, este se halla así:
Si
| Wf (2 j, njk) | ≥ 2 Ajm
Entonces:
Ajm+1
= Ajm
Por otra parte:
Ajm+1 = (7/8) Aj
m + (1/8) | Wf (2 j, njk) |
Thj = 0.3 para j= 1, 2, 3, 4.
Para calcular el QRS se toma una ventana de 120 ms, a la izquierda del pico R se usa
una ventana de 60 ms para encontrar el máximo en base del módulo máximo negativo
encontrado, aunque en algunos casos se presentan variaciones de este módulo máximo
negativo por lo cual se halla un punto j correspondiente al 25% del módulo máximo
negativo. Para hallar el final del QRS, se toma una ventana de 60 ms a la derecha del
pico R hallado anteriormente para encontrar un pico mínimo. Hallado el punto se
establece un umbral de sobrepaso para fijar el final del par módulo máximo que es el
25% del valor mínimo, en el momento que se produce el sobrepaso del umbral se
determina el final del QRS [38, 46].
DETECCION DE ONDAS P Y T
Debido a la naturaleza de las ondas P y T, y por tener su espectro de potencia entre 0.5
Hz y 10 Hz se utilizará una escala de 24 para reducir el ruido pues estas pueden ser
fácilmente afectadas por este tipo de fenómenos [47, 40], por lo cual para su obtención
se usa la escala 4 y se tomará una ventana de 200 ms a la izquierda de la onda R para
detectar la onda P y 200 ms a la derecha de la onda R para detectar la onda T [39]. En
la escala 21 en los primeros segmentos del inicio de QRS la transformada Wavelet
genera un par de módulos máximos como en el QRS pero de menor dimensión, esto

permite establecer de una manera más simple el inicio y final de las ondas P y T [39,
47].
El pico y el ancho de la onda P son encontrados de la siguiente manera [40]:
• El módulo máximo es un punto donde la | Wf (2 4, τ) | es un máximo.
• El pico de la onda P corresponde al cruce por cero entre un par de módulos
máximos de signos opuestos.
• El inicio de la onda P es ubicado por paso comenzado hacia atrás del punto del
módulo máximo de signo opuesto ubicado a la izquierda del cruce por cero,
hasta que el punto halla alcanzado | Wf (2 4, τ) | lo cual equivale al 5% del
módulo máximo.
• Para el final de la onda P se inicia un proceso similar ubicándose en el punto del
módulo máximo situado a la derecha del cruce por cero y avanzando hacia
adelante se selecciona como en el inicio de la onda P.
La onda T tiene el mismo procedimiento que la onda P. Una vez obtenida la matriz y
finales de las ondas P, QRS y T se extrae la duración de los latidos, las ondas y los
intervalos [47].
MEDIDA DE DESEMPEÑO EN LA DETECCIÓN DELCOMPLEJO QRS
Para evaluar el algoritmo de detección fueron definidas las siguientes clases de latidos
[41, 48]:
TP: (True Positive) latidos correctamente detectados equivalentes al número de
verdaderos positivos.
FP: (False positive) Picos de la señal que el detector tomó como latidos y no lo son,
equivale al número de falsos positivos.
FN: (False Negative) Latidos que no fueron detectados, equivale al número de falsos
negativos.
Con estas definiciones se calculan 2 medidas del rendimiento del detector:

• Valor Predictivo Positivo (+P): Medida mediante la cual se determinará
cuantos latidos detectados son verdaderos.
+P = TP / (TP + FP)
• Sensibilidad (S): Medida mediante la cual se determinará cuantos latidos son
detectados entre todos los latidos analizados por el detector.
S = TP / (TP + FN)
Con las anteriores ecuaciones se puede determinar el desempeño del detector pues si S
es baja significa que el detector tiende a perder latidos mientras que si P es baja el
detector toma latidos que no lo son. Por el contrario si S es alta se asume que no se
están perdiendo latidos y si P es alta se están obteniendo latidos correctos [41].
CAPITULO 4
RESULTADOS Y CONCLUSIONES
A continuación presentaremos los resultados obtenidos con la aplicación del algoritmo
para la detección del complejo QRS la onda P y T descrito en el capitulo anterior,
además se mostrara la efectividad del algoritmo en ondas anormales.
Para la implementación del algoritmo estudiado, se ha programado un software en java
cuyo manual de instrucciones de manejo se encuentra en el Apéndice A, al final de este
documento.
4.1 PROCESO DE FILTRADO

En este proceso se utilizó se utilizó la técnica de descomposición multinivel. Para la
línea base se utilizo el nivel de descomposición 8 y para el efecto de red se utilizo el
nivel 3 [42]. En este filtrado solo se usan coeficientes de aproximación no de detalle.
En La figura (4.1) se observa el efecto de filtrado en la línea base y en la figura (4.2)
se observa el filtrado de la interferencia de la red.
Figura 4.1. Efecto del filtrado de línea base con descomposición multinivel

Figura 4.2. Señal filtrada, sin línea base y sin interferencia de la red
4.2 DETECCION DE LAS ONDAS
.
Con la señal filtrada, se aplica la transformada wavelet continua (CWT), esta
permite tener la señal en diferentes escalas; en la escala j=21
[44, 45], se buscan los
pares máximos que corresponden a la onda R, en esta escala se minimiza el efecto
de ruido de alta frecuencia que puede generar falsos QRS el pico R se halla
buscando un par de módulos máximos de signos opuestos y el cruce por cero
determina la ubicación de dicha onda. En la figura (4.3) se puede observar esto.

Figura 4.3. Determinación de la onda R a partir del cruce por cero de la escala 21.
La energía de las ondas P y T permite utilizar la escala 24 [11], en esta escala se
evita la interferencia de la línea base se utilizo una ventana de 200ms a la izquierda
de cada pico R para calcular un par modulo básico de signo opuesto producido por
la onda P; Esto se puede observar en las figuras (4.4).

Figura 4.4. Determinación del inicio y el final de la onda P con la escala 24.
Para detectar la onda T se utilizó el mismo procedimiento de la onda P, con la
variante que la ventana de 200ms va a la derecha del pico R. Esto se muestra en las
figuras (4.5).

Figura 4.5. Determinación del inicio y el final de la onda T con la escala 24.
Para la evaluación del algoritmo presentado se utilizaron las señales de la base de
datos MIT-BIH de arritmias de la página web de fisionet y se compararon los
resultados obtenidos con los del enlace chart- omatic [49]. Cada señal tiene al
rededor de 650000 muestras que equivalen a 30 minutos de duración de cada señal.
4.3 MEDIDA DE DESEMPEÑO EN LA DETECCIÓN DEL COMPLEJO QRS
Con el fin de verificar la veracidad de los resultados obtenidos con nuestro software,
se tomó la señal 101 [49] que es una de las que presentan mayor cantidad de ritmo
normal y se compararon los valores de pico del complejo QRS obtenidos por
nosotros durante los primeros 3 minutos de la señal con las de esta base de datos
[49] ya que este valor es el único suministrado por esta página y lo que lo hace el
resultado más verás que podremos obtener; los resultados de la medida de
desempeño se encuentra en la tabla 4.1. También se colocará en la tabla 4.1 la
diferencia promedio de tiempo entre ambos resultados.

TP FP FN +P +S DIFERENCIA PROMEDIO (s)
206 0 13 1.0 0.94 0.00417
Tabla 4.1. Desempeño del algoritmo comparado con los de la base de datos [49].
Al revisar los resultados de la tabla 14.1 se observa que el valor predictivo positivo (+P)
es 99,9% y la sensibilidad 94% lo cual nos brinda una gran exactitud y efectividad,
otro punto a favor de nuestro algoritmo es que en promedio solo se desvía 4 milésimas
de segundo del resultado original.
4.4 ANALISIS DE LA VARIABILIDAD DE SEÑALES CARDIOVASCULARES
Para esta sección implementamos un algoritmo clasificador el cual fue entrenado con
datos verídicos tomados de la base de datos mit-bih [49], al ser entrenado con esta base
de datos solo se pueden estudiar las arritmias que son detectables con la distancia entre
picos de complejos QRS o frecuencia cardíaca, se analizaron las diferentes arritmias
tomando veinte muestras reales de la base de datos [49] y comparándolas con los
resultados de nuestro clasificador. Los resultados de este proceso son los siguientes.
4.4.1 RITMO NORMAL
Para este ritmo se utilizaron 20 muestras de la señal 101 [49].
SEGUNDOS ARRITMIA MIT-BIH ARRITMIA
ALGORTIMO
1 NORMAL NORMAL
14 NORMAL NORMAL
50 NORMAL NORMAL
114 NORMAL NORMAL
142 NORMAL NORMAL
160 NORMAL NORMAL
200 NORMAL NORMAL
207 NORMAL NORMAL

231 NORMAL NORMAL
330 NORMAL NORMAL
360 NORMAL NORMAL
375 NORMAL NORMAL
593 NORMAL BRADICARDIA
842 NORMAL BRADICARDIA
970 NORMAL NORMAL
1000 NORMAL NORMAL
1200 NORMAL NORMAL
1350 NORMAL BRADICARDIA
1370 NORMAL NORMAL
1450 NORMAL BRADICARDIA
Tabla 4.2. Estudio comparativo entre la base de datos MIT-BIH y el algoritmo realizado
para el ritmo normal.
Al observar la tabla 4.2, se nota claramente que el algoritmo implementado por nosotros
tiene una exactitud del 80%, en estos resultados y al observar las gráficas no podemos
decir que sean por no detección de pulsos, más bien se deba esta diferencia a los datos
del entrenador o al poco umbral entre un ritmo normal y una bradicardia sinusal.
4.4.2 BRADICARDIA SINUSAL
Para esta arritmia se utilizaron 20 muestras de la señal 232 [49].
SEGUNDOS ARRITMIA MIT-BIH ARRITMIA
ALGORTIMO
10.1 BRADICARDIA BRADICARDIA
24.78 BRADICARDIA BRADICARDIA
39.7 BRADICARDIA BRADICARDIA
45 BRADICARDIA BRADICARDIA
56 BRADICARDIA BRADICARDIA
68.3 BRADICARDIA BRADICARDIA

174.5 BRADICARDIA BRADICARDIA
200.6 BRADICARDIA BRADICARDIA
239.4 BRADICARDIA BRADICARDIA
312.1 BRADICARDIA BRADICARDIA
352.5 BRADICARDIA BRADICARDIA
363.4 BRADICARDIA BRADICARDIA
379.7 BRADICARDIA BRADICARDIA
394.8 BRADICARDIA BRADICARDIA
422.4 BRADICARDIA BRADICARDIA
462 BRADICARDIA BRADICARDIA
635.8 BRADICARDIA BRADICARDIA
645.5 BRADICARDIA BRADICARDIA
872.1 BRADICARDIA BRADICARDIA
885.6 BRADICARDIA BRADICARDIA
Tabla 4.3. Estudio comparativo entre la base de datos MIT-BIH y el algoritmo realizado
para la arritmia bradicardia sinusal.
Al observar la tabla 4.3 notamos que el algoritmo implementado tiene una exactitud de
un 99,9% con respecto a los datos de la base de datos MIT-BIH.
4.4.3 BIGEMINY VENTRICULAR
Para esta arritmia se utilizaron 20 muestras de la señal 106 [49].
SEGUNDOS ARRITMIA MIT-BIH ARRITMIA
ALGORTIMO
166.02 BIGEMINY BRADICARDIA
715.2 BIGEMINY BIGEMINY
749.06 BIGEMINY NORMAL
802.46 BIGEMINY BIGEMINY
824.1 BIGEMINY BIGEMINY
827.1 BIGEMINY BIGEMINY

830.3 BIGEMINY BIGEMINY
840.6 BIGEMINY BIGEMINY
848.6 BIGEMINY BIGEMINY
855.3 BIGEMINY BIGEMINY
885 BIGEMINY BIGEMINY
1063.5 BIGEMINY BIGEMINY
1072.4 BIGEMINY BIGEMINY
1142.2 BIGEMINY BIGEMINY
1149.1 BIGEMINY BIGEMINY
1165.4 BIGEMINY BIGEMINY
1259.5 BIGEMINY BIGEMINY
1441.3 BIGEMINY BIGEMINY
1511.35 BIGEMINY BIGEMINY
1518.8 BIGEMINY BIGEMINY
Tabla 4.4. Estudio comparativo entre la base de datos MIT-BIH y el algoritmo realizado
para la arritmia Bigeminy ventricular.
Al observar la tabla 4.4 se observa que el algoritmo implementado tiene una exactitud
de un 90% con respecto a los datos de la base de datos MIT-BIH. Este 10% se debe a
que algunos CVP’s tienen formas muy anormales y el programa no lo detecta como un
pulso (ver figura 4.6)

Figura 4.6. El CVP no es detectado por el programa por su gran anormalidad.
4.4.4 TRIGEMINY VENTRICULAR
Para esta arritmia se utilizaron 20 muestras de la señal 119 [49].
SEGUNDOS ARRITMIA MIT-BIH ARRITMIA
ALGORTIMO
175 TRIGEMINY TRIGEMINY
178 TRIGEMINY TRIGEMINY
181 TRIGEMINY TRIGEMINY
184 TRIGEMINY TRIGEMINY
239.6 TRIGEMINY TRIGEMINY
242.3 TRIGEMINY TRIGEMINY
245.1 TRIGEMINY TRIGEMINY
300 TRIGEMINY TRIGEMINY
302.8 TRIGEMINY TRIGEMINY
305.5 TRIGEMINY TRIGEMINY
308.2 TRIGEMINY TRIGEMINY
310.9 TRIGEMINY TRIGEMINY
326.2 TRIGEMINY TRIGEMINY
328.9 TRIGEMINY TRIGEMINY
331.6 TRIGEMINY TRIGEMINY
334.3 TRIGEMINY TRIGEMINY
336.9 TRIGEMINY TRIGEMINY
339.6 TRIGEMINY TRIGEMINY
369.9 TRIGEMINY TRIGEMINY
372.6 TRIGEMINY TRIGEMINY
Tabla 4.5. Estudio comparativo entre la base de datos MIT-BIH y el algoritmo realizado
para la arritmia Trigeminy ventricular.

La tabla 4.5 nos demuestra que el algoritmo implementado tiene una gran capacidad
para detectar la arritmia Trigeminy Ventricular, es posible que en esta señal estudiada
los CVP’s no sean muy anormales y nuestro algoritmo los detecte exitosamente, de aquí
el gran porcentaje de éxito (99,9%).
4.4.5 BLOQUEO DE SEGUNDO GRADO
Para esta arritmia se utilizaron 20 muestras de la señal 231 [49].
SEGUNDOS ARRITMIA MIT-BIH ARRITMIA
ALGORTIMO
98.8 BLOQUEO GRADO II BRADICARDIA
102.3 BLOQUEO GRADO II BRADICARDIA
107.3 BLOQUEO GRADO II BRADICARDIA
110.7 BLOQUEO GRADO II BRADICARDIA
115.6 BLOQUEO GRADO II BRADICARDIA
120.4 BLOQUEO GRADO II BRADICARDIA
125.3 BLOQUEO GRADO II BRADICARDIA
130 BLOQUEO GRADO II BRADICARDIA
134.9 BLOQUEO GRADO II BRADICARDIA
139.9 BLOQUEO GRADO II BRADICARDIA
143.2 BLOQUEO GRADO II BRADICARDIA
334.8 BLOQUEO GRADO II BRADICARDIA
338.3 BLOQUEO GRADO II BRADICARDIA
343.3 BLOQUEO GRADO II BRADICARDIA
348.3 BLOQUEO GRADO II BRADICARDIA
353.2 BLOQUEO GRADO II BRADICARDIA
358.1 BLOQUEO GRADO II BRADICARDIA
363.1 BLOQUEO GRADO II BRADICARDIA
368 BLOQUEO GRADO II BRADICARDIA
373.1 BLOQUEO GRADO II BRADICARDIA

Tabla 4.6. Estudio comparativo entre la base de datos MIT-BIH y el algoritmo realizado
para la arritmia bloqueo de segundo grado.
El bloqueo de primer grado no se estudia en este trabajo debido a que este no es
detectable con la frecuencia cardiaca, este es solo detectable con el intervalo PR. Al
estudiar la tabla 4.6 se nota que este bloqueo de grado 2 es 100% detectable como una
bradicardia, esto es así porque como se verá en la figura 4.7, este bloqueo se presenta
como una onda P sin QRS donde debería ir un pulso normal, y como el algoritmo solo
primero detecta el complejo QRS para después desplegarse y hallar las ondas P y T, no
lo toma como un pulso y este se convierte para él en una bradicardia sinusal.
Figura 4.7. En el bloqueo grado II, se presenta una onda P aislada, sin complejo QRS ni
onda T.
4.4.6 TAQUICARDIA VENTRICULAR
Para esta arritmia se utilizaron 20 muestras de las señales 203 y 205 [49].
SEGUNDOS SEÑAL ARRITMIA MIT-BIH ARRITMIA
ALGORTIMO
298.9 205 TAQUICARDIA VENTRIC TAQUICARDIA VENTRIC
299.9 205 TAQUICARDIA VENTRIC TAQUICARDIA VENTRIC

303.4 205 TAQUICARDIA VENTRIC TAQUICARDIA VENTRIC
304.7 205 TAQUICARDIA VENTRIC TAQUICARDIA VENTRIC
1460.6 205 TAQUICARDIA VENTRIC TAQUICARDIA VENTRIC
1462.1 205 TAQUICARDIA VENTRIC TAQUICARDIA VENTRIC
1463 205 TAQUICARDIA VENTRIC TAQUICARDIA VENTRIC
1472.4 205 TAQUICARDIA VENTRIC NORMAL
104.9 203 TAQUICARDIA VENTRIC BRADICARDIA
268.7 203 TAQUICARDIA VENTRIC BRADICARDIA
301.4 203 TAQUICARDIA VENTRIC TAQUICARDIA VENTRIC
303.5 203 TAQUICARDIA VENTRIC TAQUICARDIA VENTRIC
305.33 203 TAQUICARDIA VENTRIC TAQUICARDIA VENTRIC
510.6 203 TAQUICARDIA VENTRIC BRADICARDIA
1153 203 TAQUICARDIA VENTRIC TAQUICARDIA VENTRIC
1154 203 TAQUICARDIA VENTRIC TAQUICARDIA VENTRIC
1202.8 203 TAQUICARDIA VENTRIC NORMAL
1497 203 TAQUICARDIA VENTRIC BRADICARDIA
1605.5 203 TAQUICARDIA VENTRIC TAQUICARDIA VENTRIC
1606.5 203 TAQUICARDIA VENTRIC BRADICARDIA
Tabla 4.7. Estudio comparativo entre la base de datos MIT-BIH y el algoritmo realizado
para la arritmia taquicardia ventricular.
Al observar la tabla 4.7 observamos que el porcentaje de precisión de nuestro algoritmo
baja al 65% para esta arritmia. Esto se debe a que este tipo de arritmias como la
taquicardia, el flutter y la fibrilación, tienen una gran cantidad de ondas de distintas
formas, tamaños y son muy continuas, por lo que el algoritmo no logra detectarlas como
pulsos y simplemente toma estos segmentos como si no hubiera nada por lo que la nota
como normal o como bradicardia. Ver figura 4.8.

Figura 4.8 En arritmias como taquicardia ventricular, flútter ventricular y fibrilación
ventricular se pueden notar gran cantidad de pulsos de distintos tamaños y formas, lo
que los hace indetectables para nuestro algoritmo WAVELET.
4.5 CONCLUSIONES
La creación de nuestro software se realizó en la plataforma java, esto nos trajo ventajas
como lo fue crear un programa de buena calidad gráfica y muy fácil de manejar; pero lo
más importante es que no se necesita plataformas especiales como Matlab para poderlo
ejecutar en cualquier ordenador. Algo más que aventaja nuestra plataforma es que
permite realizar cálculos muy grandes y manejar gran cantidad de datos, en el caso de
nuestro algoritmo cada señal tiene aproximadamente 650.000 muestras las cuales son
muy robustas para que un programa como Matlab las pueda manejar.
La señal de los ECG fue depurada del ruido causado por la interferencia de la red y la
desviación de la línea base con la aplicación de descomposición multinivel que ofrece la
transformada Wavelet.

Se detectaron de manera satisfactoria los complejos QRS en la escala 21 y de las ondas
P y T, aunque estas últimas no fueron verificadas ya que la base de datos para arritmias
del MIT-BIH [49], no nos brinda esta opción.
Algunos complejos QRS son descartados por no cumplir el umbral establecido que tiene
como valor el 30% del punto máximo de la señal; lo que pudo causar la reducción de la
sensibilidad de 1 a 0,94.
Aunque se presentó el inconveniente arriba mencionado, se alcanzó un 94% de
sensibilidad, lo que hace al algoritmo de un buen desempeño, confiabilidad y precisión.
Las arritmias como la bradicardia sinusal, el bigeminy ventricular y el trigeminy
ventricular, fueron detectadas con éxito, presentando una precisión no menor del 90%
en cada una de ellas.
El bloqueo de segundo grado se detectó en nuestro algoritmo como una bradicardia
sinusal debido a que este se presenta en el ECG como una onda P aislada y el software
primero debe detectar la onda QRS para de allí proceder a encontrar las ondas P y T de
dicho pulso.
La taquicardia ventricular tiene una baja precisión (60%), esto debido a que las ondas de
taquicardia ventricular se presentan muy seguidas y con distintas formas y tamaños por
lo que el algoritmo no las considera como complejos QRS y por lo tanto como ondas.
La fibrilación ventricular y el flútter ventricular tienen pulsos que no se asemejan en
nada a un pulso normal, con lo que nuestro algoritmo Wavelet no lo detecta como
pulsos, estos casos el algoritmo los tomaría como bradicardia sinusal.
Para la continuidad de este estudio se recomienda para trabajos futuros:
• Trabajar con bases de datos que permitan evaluar con precisión las ondas P y T.
• Implementar un algoritmo que permita detectar arritmias como el bloqueo de
primero y segundo grado, el flutter ventricular, la fibrilación ventricular y
mejore la precisión de la taquicardia ventricular.

• Implementar una lector de ECG que pueda alimentar directamente el algoritmo
para hacer un estudio directo y en tiempo real de los distintos tipos de arritmias.
BIBLIOGRAFIA
1. Foto sacada de www.somatechnology.com.
2. Imagen tomada de www.nlm.nih.gov
3. Imagen tomada de www.iqb.es
4. Guyton A.C., HALL J.E., “Tratado de Fisiología Médica”, Student Consult (11º
ED.), Ed. Elsevier España, S.A., 2006.
5. VV.AA, “Atlas Sistema Cardiovascular”, ARS MEDICA, 2005.
6. Janssen M, Swenne C, de Bie J, Rompelman O & Van Bemmel J (1993),
“Methods in Heart Rate Variability Analysis: Which Tachogram Should We
Choose?”, Comput Methods Programs Biomed 41: 1 – 8.
7. Lindner U. K, Dubin D, “Introducción a la Electrocardiografía: Método
Autodidacta de Interpretación del ECG” (2º ED.), ed. MASSON, 2005.
8. Davis, Dale, “Interpretación del ECG : su Dominio Rápido y Exacto”, Ed.
Panamericana, 2007.
9. Huszar, Robert J. “Arritmias: Principios, Interpretación y Tratamiento” (3º ED.),
Elsevier España S.A., 2005.
10. Huikuri H. (1997), Abnormal dynamics of ventricular repolarization - a new
insight into de mechanisms of life-threatening ventricular arrhythmias. Eur
Heart J 18: 893-895.
11. Laguna P, Thakor N, Caminal P, Jane R & Yoon HR (1990) New algorithm for
QT interval analysis in 24-hour Holter ECG: Performance and applications.
Med Biol Eng Comput 28: 67-73.
12. Mulder L (1992) Measurement and analysis methods of heart rate and
respiration for use in applied environments. Biol Psychol 34: 205-236
13. Baevskij R, Kirillov O & Kletskin S (1984) Mathematical Analysis of the
Changes in Cardiac Rhythm During Stress. Nauka, Moscow.
14. Casolo G, Balli E, Taddei T, Amuhasi J & Gori C (1989) Decreased
spontaneous Herat rate variability in congestive heart failure. Am J Cardiol 64:
1162-1167.
15. Odemuyiwa O, Malik M, Farrell T, Bashir Y, Poloniecki J & Camm J (1991)
Comparison of the predictive characteristics of heart rate variability index and
left ventricular ejection fraction for all-cause mortality, arrhythmic events and
sudden death alter acute myocardial infarction. Am J Cardiol 68: 434-439.
Con formato: Inglés (Estados Unidos)

16. Jaffe R, Fung D & Behrman K (1993) Optimal frequency ranges for extracting
information on automatic activity from the heart rate spectrogram. J Auton Nerv
Syst 46: 37-46.
17. Sapoznikov D, Luria M & Gotsman M (1994) Di_erentation of periodic from
nonperiodic low-frequency heart rate fluctuations. Comput Biomed Res 27: 199-
209.
18. Korhonen I (1997) Methods for the analysis of short-term variability of heart
rate and blood pressure in frequency domain. PhD thesis, Tampere University of
Technology
19. Kamath M & Fallen E (1993) Power spectral analysis of heart rate variability: a
non-invasive signature of cardiac autonomic function. Crit Rev Biomed Eng
21(3): 245-311
20. Akselrod S, Gordon D, Madved J, Snidman N, Shannon D & Cohen R (1985)
Hemodynamic regulation: investigation by spectral analysis. Am J Physiol 249:
H867-H875.
21. Pagani M, Lombardi F, Guzzetti S, Rimoldi O, Furlan R, Pizzinelli P, Sandrone
G, Cerutti S & Malliani A (1986) Power spectral analysis of heart rate and
arterial pressure as a marker of sympathovagal interaction in man and concious
dog. Circ Res 59: 178-193.
22. Cerutti S, Bianchi A, Baselli G, Civardi S, Guzzetti S, Malliani A, Pagani A &
Pagani M (1989) Compressed spectral arrays for the analysis 24-hr heart rate
variability signal. Enhancement of parameters and data reduction. Comput
Biomed Res 22: 424-441.
23. Priestley M (1981) Spectral Analysis and Time Series. Academic Press Inc.,
London.
24. Kay S (1988) Modern Spectral Estimation. Theory & Application. Prentice Hall,
Englewood Cliffs.
25. Marple S (1987) Digital Spectral Analysis with Applications. Prentice Hall,
Englewood Cliffs.
26. Hlawatsch F & Boudreaux-Bartels G (1992) Linear and quadratic time-
frequency signal representations. IEEE Signal Process Mag 9(2): 21-67.
27. Rioul O & Vetterli M (1991) Wavelets and signal processing. IEEE Signal
Process Mag 8(4): 14-38.
28. Bianchi A, Mainardi L, Petrucci E, Signorini M, Mainardi M & Cerutti S (1993)
timevariant power spectrum analysis for the detection of transient episodes in
HRV signal. IEEE Trans Biomed Eng BME-40(2): 136-144.
29. Lee F & Nehorai A (1992) Adaptive power spectrum estimation algorithm for
heart rate variability analysis. Computers in Cardiology, 273-276.
30. Mainardi L, Bianchi A & Cerutti S (1994) On-line beat-to-beat monitoring of
spectral parameters of heart rate variability signal using a pole-tracking
algorithm. Methods Inf Med 33: 85-88.
31. Pola S, Macerata A, Emdin M & Marchesi C (1996) Estimation of the power
spectral density in nonstationary cardiovascular time series: Assessing the role
of the time-frecuency representations (TFR). IEEE Trans Biomed Eng 43(1): 46-
59.
32. Akay M, Landesberg G, Welkowitz W, Akay YM & Sapoznikov D (1993)
Carotid-cardiac interaction: Heart rate variability during the unblocking of the
carotid artery. In: Sideman S & Beyar R (eds) Interactive Phenomena in the
Cardiac System. Plenum Press, New York, p 365-372.

33. Priestley M (1996)Wavelets and time-dependent spectral analysis. J Time Series
Analysis 17(1): 85-103.
34. Daubechies I (1992) Ten Lectures on Wavelets. SIAM, Philadelphia.
35. Strang G & Nguyen T (1996) Wavelets and Filter Banks. Wellesley-Cambridge
Press, Wellesley.
36. H. Inoue A. Miyasaki, “A Reduction Method for ECG Signals Using the Dyadic
Wavelet Transform”, IEICE Trans. Fundamentals, Vol E81-A, Núm 6, pp.
1001-1006, Junio 1998.
37. K. shubna, R. Murray, and G. Faye. Wavelet transform-based QRS complex
detector. IEEE transactions on biomedical engineering, 46(7): 838-848, july
1999.
38. L. Archila, J. Ardila y A. Mendoza. Caracterización del intervalo QT en una
señal electrocardiográfica usando la transformada Wavelet. Tecnología Médica,
(42): 83-87.
39. V. Di Virgilio, C. Francalancia, S. Lino y S. Cerutti, “ECG Fiducial Points
Detection Through Wavelet Transform”, IEEE-EMBC and CMBEC, 1995.
40. K. Anant, “Detection of the Electrocardiogram P-Wave Using Wavelet
Analisis”, Department of Applied Science, University of California, Internal
Report, 1994.
41. G. M. Friesen, T.C. Jannet, M.A. Jadallah, S.L. Yates, S.R. Quint, y H. Troy
Nagle, “A Comparison of the Noise Sensitivity of Nine QRS Detection
Algorithms”, IEEE Transactions on Biomedical Engineering, Vol. 31, Núm 1,
pp. 85-98, Enero 1990.
42. MathWorks. Wavelet Toolbox: User’s Guide – Version 2. For use with
MATLAB. The MathWorks, Inc., Natick, MA, 2000.
43. D. Cuesta, D. Novak, V. Eck, J.C. Pérez, G. Andreu “Electrocardiogram
Baseline Renoval Using Wavelet Aproximations”, Biosignal 2000, pp 133 –
139, Brno (R. Checa), Junio 2000.
44. N. V. Thakor, J. G. Webster y W. J. Tompkins, “Estimation of QRS Complex
Power Spectra for Design of a QRS Filter”, IEEE Transactions on Biomedical
Engineering”. Vol 3.1, Núm 11, pp 702 – 706, Noviembre 1984.
45. D. Cuesta, G. Andreu y J. C. Pérez, “Detección del Periodo en Señales Holter
para su Aplicación a la Clasificación de Patologías Coronarias”, II Jornadas de
Procesamiento de la Señal, Gandia, Enero 1999.
46. F. Ojeda, “Extracción de Características Usando Transformada Wavelet en la
Identificación de Voces Patológicas. Trabajo de Grado, Universidad Nacional de
Colombia – Sede Manizales, Septiembre 2003.
47. F. Gritzali, G. Frangakis, G. Papaconstantinou, “Detection of the P and T Waves
in an ECG”, Computers and Biomedical Research, Núm. 22, pp 83 – 91, 1989.
48. AAMI, Association for the Advancement of Medical Instrumentation,
http://www.aami.org
49. http://www.physionet.org

APENDICE A
MANUAL DE INSTRUCCIONES PARA EL MANEJO DEL SOFTWARE
DETECTOR Y CLASIFICADOR DE ARRITMIAS
El primer paso para manejar el software es abrirlo, para abrir este software se debe
buscar la carpeta llamada ECG EJECUTABLE y darle doble click, después de esto se
abrirá el explorador de Windows conteniendo los archivos de esta carpeta la cual
contiene todo el programa. Ver Figura A.1.
Figura A.1. Explorar la carpeta “ECG ejecutable”.
Después de abrir la ventana de la figura A.1, debes ubicar el archivo y
dar doble click sobre este. Al hacer esto se abrirá la ventana de inicio del software de
estudio “Inicio Wavelets”. Ver figura A.2.

Figura A.2. Ventana de inicio del software.
La ventana “Inicio Wavelets” que se observa en la figura A.2. contiene varios
numerales los cuales piden datos que son necesarios para hacer una adecuada selección
de lo que se necesita graficar y calcular. Estos numerales se explican a continuación:
A.A.A.A. Señal de entrada: en este ítem se le debe especificar al programa la señal que se
quiere estudiar, para esto cuenta con una lista de señales tomadas de la base de
datos de arritmias de la página de physionet mit-bih [49]. Ver figura A.3.
Figura A.3. Listado de señales que se pueden utilizar en el programa.
B.B.B.B. : Estos son los botones normales que se usan en Windows para
minimizar, maximizar y cerrar la ventana y el programa en ejecución.

C.C.C.C. : En este ítem se indica al programa la
escala en segundos que se desea ver la señal fragmentada en el eje del tiempo,
este va desde 3 segundos hasta 20 segundos. Debe tenerse en cuenta que entre
más grande sea este tiempo, el programa necesitará más tiempo de respuesta.
D.D.D.D. : Si se desea que el programa grafique la señal ECG original se deberá
dar click sobre esta, así quedará marcada, en caso contrario el programa solo
graficará la señal Wavelet estudiada.
E.E.E.E. CWT Escala: En esta parte de la ventana se debe hacer click sobre la escala
Wavelet en la cual se quiere trabajar la señal, el programa graficará la escala
escogida; se cuentan para esto con la escala 1 a 4. El programa permite escoger
solo una de ellas.
F.F.F.F. Picos, Onda P, Onda T, Onda QRS: Aquí se debe hacer click sobre la onda que
se quiere señalar en la gráfica Wavelet y también para hallar los datos de tiempo
en que estas ondas se encuentran localizadas en la gráfica ECG. El programa te
mostrará la localización de los picos del complejo QRS, el inicio y fin de la onda
P, T y del complejo QRS. El programa permite seleccionar desde uno hasta
todos los ítems a la vez.
G.G.G.G. :Para finalizar después de haber elegido con éxito los ítems anteriores
se da click sobre este icono para que el programa comience y en seguida nos
muestre la ventana “ECG” donde está la gráfica de la señal. Ver figura A.4.

Figura A.4. Ventana “ECG”
En esta nueva ventana que nos abre el programa se pueden observar algunos ítems
distintos los cuales explicaremos a continuación:
1. La señal es graficada Amplitud (mV) contra tiempo (s), en la figura A.4, se
observa en el título el número de la señal escogida, en este caso la señal 101,
también se muestra la gráfica ECG original (gráfica de color verde) y la gráfica
de la transformada Wavelet escala 4 (gráfica de color azul) se encuentra
superpuesta a esta usando los mismos ejes que la anterior.
2. : Este ítem abre una ventana en la cual se visualizan las convenciones
que explican la gráfica observada en la ventana “ECG”. Ver figura A.5.
3. Estos botones se utilizan para adelantar o retroceder la
gráfica, esto ocurre según la escala de tiempo graficado que se escogió en la
ventana “Inicio Wavelets”.

Figura A.5. Convenciones de la gráfica “ECG”
4. : Este botón se usa cuando se quieren ver las tablas de datos, estas se
muestran en Excel. Se mostrarán 2 tablas distintas, la primera llamada logDatos
tiene 3 columnas las cuales muestran las coordenadas de la gráfica tanto en el eje
X (tiempo), como en el eje Y (señal, CWT) ver figura A.6. La segunda tabla
llamada logDatosPuntos contiene la posición de los puntos que se han escogido
anteriormente (Picos, Inicio-fin onda P, inicio-fin onda T, inicio-fin onda QRS),
ver figura A.7.
Figura A.6. Tabla logDatos

Figura A.7. Tabla logDatosPuntos
Estas tablas te muestran los valores de la señal completa y no solo la parte que
muestre la gráfica.
5. : Esta opción es la de clasificar arritmia, al dar click sobre este, se
abrirá una nueva ventana (ver figura A.8) en la cual se le preguntará el punto de
inicio del segmento de la gráfica que se desea estudiar en segundos, se debe
colocar este valor y dar click en el botón clasificar que se encuentra en la misma
ventana, después de esto, el programa te mostrará el resultado en la parte baja de
esta ventana (ver figura A.8).
Figura A.8. Ventana del clasificador de arritmia
6. : La opción final que presenta el
programa es la de mostrar tiempo, en esta se puede adelantar o atrasar la gráfica
con solo dar click sobre el minuto que se quiere observar.