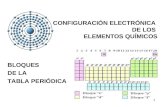
Configuración electrónica
-
Upload
nildabel-acosta -
Category
Documents
-
view
452 -
download
5
Transcript of Configuración electrónica

CONFIGURACIÓN ELECTRÓNICA
Química 11Sra. Acosta

Configuraciones electrónicasordenamiento de los electrones en un
átomo.La manera como se pueden ordenar los
electrones de los orbitales de un átomo esta definida por tres reglas o principios: el principio de Aufbau, el principio de exclusión de Pauli y la regla de Hund.

Configuraciones electrónicas• Principio de Aufbau – establece que cada electrón ocupa el orbital disponible con energía más baja.

Configuraciones electrónicasTodos los orbitales relacionados con
un nivel de energía son de igual energía.
En un átomo con múltiples electrones, los subniveles de energía dentro de un nivel principal de energía tienen energías diferentes.

Configuraciones electrónicasSegún la cantidad de energía, la
secuencia de los subniveles en un nivel principal es s, p, d, y f.
Los orbitales relacionados con subniveles de energía de un nivel principal de energía pueden superponerse a los orbitales relacionados con subniveles de energía de otro nivel principal.

Configuraciones electrónicas
Principio de exclusión de Pauli: establece que un máximo de dos electrones pueden ocupar un mismo orbital atómico, pero solamente si los electrones tienen espines opuestos.
( )

Configuraciones electrónicas• Regla de Hund – establece que los electrones cuyo giro es igual deben ocupar todos los orbitales que tienen igual energía, antes de que electrones adicionales que tengan giros opuestos puedan ocupar los mismos orbitales.




Configuraciones electrónicasElectrón de valencia – se definen como aquellos situados en los orbitales mas externos del átomo; generalmente los orbitales asociados al nivel principal de energía más alto del átomo.

Configuraciones electrónicasSímbolos electrónicos – representa el núcleo atómico y los electrones de los niveles internos, rodeados por puntos que representan los electrones de valencia del átomo.