Contenido Tematico 1.2a Teoria Atomica Cuanticaxx
-
Upload
fernando-temores-ramirez -
Category
Documents
-
view
359 -
download
0
Transcript of Contenido Tematico 1.2a Teoria Atomica Cuanticaxx

En la Universidad de Guadalajara
Por medio de la Academia de Química en la
Escuela Preparatoria 12
Se presenta:
Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos

Exposición Académica
Por:Mtro. Fernando Temores Ramírez
Guadalajara, JaliscoSeptiembre de 2007
Contenido temático 1.2:Estructura atómica de los elementos químicos
-Teoría Atómica Cuántica-
Química II
2ACADEMIA DE QUÍMICA 2
PREPARATORIA 12
Q
Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos

Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos
Representarás la configuración electrónica de los átomos, considerando la teoría atómica
cuántica.
Objetivos
Relacionaras las investigaciones de la naturaleza de la luz, la teoría quántica para la definición
del modelo atómico actual

Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos
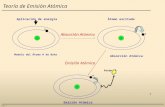
Antecedentes: la naturaleza de la luz

Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos
Luego entonces surgió la pegunta: ¿La luz son partículas u ondas?
Antecedentes: la naturaleza de la luz
Si la luz se parece a una onda en el agua, ¿que es lo que ondula? Ondula el agua.
Una botella flotando nos permite ver que cuando es alcanzada y levantada por una ola, una vez que esta pasa, la botella sigue en su sitio.
La ola no es un movimiento del agua, sino en el agua.
Cuando ocurre un sonido, ondula el aire.
Si la luz es ondas y éstas nos llegan del Sol, de la Luna, de las estrellas, y por tanto atraviesan
distancias inmensas de espacio vació. ¿que es lo que ondula?

Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos
Líneas Espectrales
A finales del siglo XIX, los físicos sabían que había electrones dentro de los átomos y que la vibración de los electrones producía luz y otras radiaciones electromagnéticas.
Pero quedaba aún un curioso misterio por resolver. Los físicos calentaban diferentes elementos hasta que estaban radiantes y entonces dirigían la luz a través de un prisma...
Se ve todo el arco iris porque el prisma separa la luz en todos sus colores.

Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos
Líneas Espectrales
Pero cuando los científicos observaron la luz que venía de un solo elemento, hidrógeno, por ejemplo, no vieron el arco iris completo. En su lugar obtuvieron líneas brillantes de ciertos colores.
Eso significaría que los átomos estaban emitiendo solamente ondas de ciertas frecuencias.
Cada tipo de átomo emite un conjunto único de colores. Las líneas de color (o Líneas Espectrales) son la "firma" de los átomos.

Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos
Modelos atómicos de Bohr y Sommerfel
Con el Modelo atómico de Rutherford no se contesta el porque los átomos absorben y emiten energía cuando son expuestos a cierta intensidad de luz o alguna otra forma de energía.
Hoy se cree que la luz se comporta como onda y partícula a la vez (dualidad). Vamos, se afirma que la luz es una forma de energía radiante o electromagnética, como las ondas de radio, los rayos infrarrojos, los rayos x, etc.
Las ondas electromagnéticas se consideran campos eléctricos y magnéticos en movimiento, que oscilan en forma de ondas en planos perpendiculares.
La luz genera haz de luz de ondas electromagnéticas que se desplaza en el espacio. Como todo movimiento electromagnético tiene longitud de onda y una frecuencia.

Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos
Postulados de Bohr
1. El átomo está constituido por un núcleo central donde se localiza la carga positiva y casi toda la masa, y el electrón, describe orbitas circulares alrededor del núcleo.
2. El electrón gira alrededor del núcleo siguiendo orbitas cuyo radio esta definido por la ecuación: r= πnh/2 mv. A mayor radio mayor energía tiene el electrón en esa orbita.
3. Cuando un electrón se mueve en una orbita de radio definido tiene una energía constante y no gana ni pierde energía, se dice que esta en un una orbita fundamental o basal. Cuando el electrón es excitado y pasa de una orbita a otra se produce una emisión o absorción de energía en forma de luz (fotón)

Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos
Modelo atómico actual
Fue desarrollado por Erwin Schrodinger, en el que se describe el comportamiento del electrón en función de sus características ondulatorias
Este modelo surgió a partir del comportamiento de la luz y de la teoría cuántica de Max Planck
Supone que el núcleo esta rodeado por una nube tenue de electrones que retiene el concepto de niveles
estacionarios de energía.
Pero a diferencia de Bohr, no le Atribuye al electrón trayectorias definidas, sino que describe su localización en términos de probabilidad.

Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos
Nubes probabilísticas de Schrodinger

Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos
Pero, como ondula la luz?
La luz ondula como una forma de energía radiante o electromagnética.
Del modelo atómico anterior surgió de los estudios del comportamiento de la luz y de la teoría cuántica.
En 1900, Max Planck, experimentó y analizó las radiaciones emitidas por sólidos sometidos a diversas temperaturas, descubrió que los átomos y las moléculas emiten energía en forma de paquetes o quantums, únicamente en números enteros múltiplos de cantidades bien definidas.
Principio de incertidumbre: Tiempo después, Heisenberg, imaginó un microscopio superpotente por medio del cual se pudiera observar la posición y velocidad de un electrón. Determinó que es imposible en un momento dado saber la posición exacta y la velocidad del electrón en un nivel energético ya que para poder hacerlo se debe de “iluminar” al electrón con luz, y al hacerlo ésta desvía o cambia la velocidad del electrón (“lo que estudias lo cambias”).

Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos
Con el modelo atómico de Schrodinger basado en su ecuación de onda se obtienen un gran numero de soluciones respecto a la posición de los electrones.
Números Cuánticos
Tales soluciones se identifican como los números cuánticos (por la teoría de Max Planck).
Los números cuánticos se identifican como:
n, l, m , s.
Cada electrón tiene un conjunto de cuatro números cuánticos, que lo especifican completamente; no hay dos electrones en el mismo átomo que tenga los mismos cuatro números cuánticos. Esa es una declaración más precisa del principio de exclusión de Pauli

Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos
n (numero cuántico principal), designa el nivel energético (orbital) en el cual se encuentra un electrón dado; este numero expresa la energía de los niveles dentro del átomo. Puede asumir
valores de 1, 2, 3 , 4, 5, 6 y 7.
l (numero cuántico secundario), determina el orbital en el que se encuentra el electrón. Sus
valores dependen del valor del numero quántico
principal n; estos van de 0 a … (n-1). Se explica mejor a continuación
Números Cuánticos

Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos
Números Cuánticos
l= 0, describe los orbitales “S” (Sharp)

Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos
Números Cuánticos
l= 1, describe tres subniveles u orbitales “p”
(principal)

Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos
Números Cuánticos
l= 2, describe cinco orbitales o subniveles
“d” (diffused)

Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos
Números Cuánticos
l= 3, describe siete subniveles u orbitales “f”
(fundamental)

Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos
Números Cuánticos
m (numero cuántico magnético), representa la orientación en el espacio del giro del electrón
alrededor del núcleo de un átomo. Sus posibles valores son - l pasando por el cero hasta +l.
Vamos, es responsable por determinar la forma de la nube de probabilidad de un electrón. He
aquí algunos ejemplos:

Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos
Números Cuánticos
s (numero cuántico spin), determina el giro del electrón sobre su propio eje, que sólo puede tener dos direcciones: uno en sentido de las agujas del reloj y el otro en sentido contrario. Puede tener valores numéricos de +1/2 y -1/2.

Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos
Según la mecánica cuántica las zonas donde es más probable encontrar los electrones son los
orbitales atómicos
Configuración electrónica
Los átomos pequeños poseen un núcleo pequeño con un numero reducido de protones y
electrones.
Cuando un átomo es más grande, la probabilidad de que los electrones se
encuentren en cierto lugar se distribuye y organiza de cierta manera. A esto se le conoce
como configuración electrónica

Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos
Reglas para la configuración electrónica
La configuración electrónica esta regida por las siguientes tres reglas:
Principio de Aufbau: los electrones en un átomo ocupan los orbitales en orden creciente de energía.
Principio de exclusión de Pauli: un orbital puede estar ocupado sólo por dos electrones con spin
antiparalelo.
Regla de Hund: cuando varios electrones ocupan orbitales con más de un subnivel
energético, los electrones ocupan orbitales diferentes y con espines paralelos.

l 3210n
1
2
3
4
5
6
7
2p6
3s2 3p6
4s2
3d10
4p6
5s2
4d10
5p6
6s2
4f14
5d10
6p6
7s2
5f14
6d10 6f14
Regla de Aufbau
Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos
1s2
2s2
7p6
Configuración electrónica extendida de Aufbau
1s2,2s2,2p6,3s2,3p6,4s2,3d10,4p6,5s2,4d10,5p6,6s2,4f14,5d10,6p6,5f14,6d10,7s27p6,6f14

Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos
1s
1s2
2s
2s2
2p
x
2py
2pz
3s
2p6“Visualización” de los orbitales
3s2 3px3p
y3p
z
3s2 3p6
4s
4s2
4s
3dxy
3dy 2
3dx2-y2
3dz2
3d10...

Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos
Principio de exclusión de Pauli
Principio de exclusión de Pauli: un orbital puede estar ocupado sólo por dos electrones con spin
antiparalelo.

Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos
Regla de Hund
Regla de Hund: cuando varios electrones ocupan orbitales con más de un subnivel
energético, los electrones ocupan orbitales diferentes y con espines paralelos (ver ejemplo
siguiente):
N7
1s 2s 2px 2py 2pz

Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos
Notación de la configuración electrónica
El Hidrogeno, cuyo numero atómico es 1, tiene un solo electrón en el orbital de mas baja energía: 1s. Entonces su configuración electrónica se
escribe así:
H 1s1
El Helio, cuyo numero atómico es 2, tiene dos electrones, y por tanto también ocupan el
orbital de mas baja energía: 1s. Entonces su configuración electrónica se escribe así:
He 1s2
El Litio tiene tres electrones. Su tercer electrón ya ocupa el siguiente nivel de energía, el orbital 2s.
Entonces su configuración electrónica se escribe así:
Li 1s22s1

l 3210n
1
2
3
4
5
6
7
2p6
3s2 3p6
4s2
3d10
4p6
5s2
4d10
5p6
6s2
4f14
5d10
6p6
7s2
5f14
6d10 6f14
Regla de Aufbau
Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos
1s2
2s2
7p6

Configuraciones electrónicas de los gases nobles
Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos
2He:1s2
10Ne:1s2,2s2,2p6
18Ar: 1s2,2s2,2p6,3s2,3p6
36Kr:1s2,2s2,2p6,3s2,3p6,4s2,3d10,4p6
54Xe:1s2,2s2,2p6,3s2,3p6,4s2,3d10,4p6,5s2,4d10,5p6
86Rn:1s2,2s2,2p6,3s2,3p6,4s2,3d10,4p6,5s2,4d10,5p6,6s2,4f14,5d10,6p6
Configuración electrónica de los gases nobles
= [2He]
= [10Ne]
= [18Ar]
= [36Kr]
= [54Xe]
= [86Rn]

Curso química II, contenido temático 1.2: Estructura atómica de los elementos químicos
Ejercicios
Escribe la configuración electrónica de los siguientes elementos:
Be4 B
5C6
F9 Ca20 Rb
37