Diagnóstico del Virus de la Fiebre Amarilla -...
Transcript of Diagnóstico del Virus de la Fiebre Amarilla -...
Características del virus de la FA
Familia: Flaviviridae Género: Flavivirus Transmisión: Por vectores selváticos como mosquitos de los géneros Haemagogus y Sabethes o por el mosquito Aedes aegypti Clínica: Va desde uma infección asintomática hasta un cuadro grave con hemorragia e icterícia que puede resultar fatal Medida de prevención mas importante: La vacunación
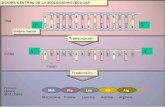
Intracelular Extracelular
PrM
E
E
• Partículas infectiva esférica (50 nm)
• Virus Envueltos: Bicapa lipídica en la que se insertan proteínas virales E (Envoltura) y M (Membrana)
• Nucleocápside: simetría no discernible
• Genoma: ARN simple cadena, polaridad positiva, infeccioso, aprox. 11 kb que codifica para tres proteínas estructurales (E, C y M) y 5 proteínas no estructurales NS1, NS2 A y B, NS3, NS4 A y B y NS5
Flaviviridae
EPIDEMIOLOGÍA MOLECULAR La secuenciación de la proteína E de la FA ha mostrado dos linajes evolutivos : Genotipo I África y América Tropical Genotipo II África Oriental y Central
Ocurre la transmisión Intercontinental adaptándose al vector local y al hospedero
Tipo de muestra y procedimientos de laboratorio Muestra idónea: Sangre total, suero o tejido fresco Diagnóstico: Métodos virológicos y moleculares : Para la detección del virus Métodos serológicos : Para la detección de anticuerpos neutralizantes
Diagnóstico de laboratorio propuesto por la OPS/OMS para confirmar la infección por FA
Consideraciones de bioseguridad El personal de laboratorio que entre en contacto con las muestras, deberá estar
vacunado contra la fiebre amarilla Realizar cualquier procedimiento de laboratorio dentro de cabinas de bioseguridad
clase II certificadas, extremando las medidas para evitar accidentes por punción
OPS/OMS 2017
http://www.paho.org/hq/index.php?option=com_topics&view=rdmore&cid=7134&Itemid=40784&lang=es
Indicaciones para el diagnóstico según el número de días desde el inicio de los síntomas
Diagnóstico molecular: Detección del ARN Viral por la Reacción en Cadena de la
Polimerasa (PCR, por sus siglas en inglés) convencional o en tiempo real
Aislamiento viral: El aislamiento viral puede realizarse por inoculación
intracerebral en ratones o en cultivo celular (células Vero o C6/36) en contención BSL 2. Sin embargo por su complejidad, es poco utilizado como metodología diagnóstica y se recomienda principalmente para estudios de investigación complementarios a la vigilancia en salud púbica http://www.paho.org/hq/index.php?option=com_topics&view=rdmore&cid=7134&Itemid=40784&lang=es
Confirmación del Diagnóstico en Fase Virémica
o virológico
Indicaciones para el diagnóstico según el número de días desde el inicio de los síntomas
Diagnóstico serológico : Detección de anticuerpos IgM mediante la técnica de ELISA
(principalmente captura de IgM, MAC-ELISA, por sus siglas en inglés) basados en procedimientos “caseros” (in-house) utilizando antígeno completo purificado o cualquier otro inmunoensayo como (inmunofluorecencia indirecta) No existen estuches comerciales validados para detección de IgM por ELISA. La confirmación de un caso de fiebre amarilla mediante ELISA IgM dependerá de la situación epidemiológica y del resultado del diagnóstico diferencial de laboratorio ya que en áreas con circulación de otros flavivirus (principalmente dengue y Zika), la probabilidad de reactividad cruzada es mayor
OPS/OMS 2017
Diagnóstico Presuntivo de una infección reciente en fase postvirémica
http://www.paho.org/hq/index.php?option=com_topics&view=rdmore&cid=7134&Itemid=40784&lang=es
o virológico
Detección de anticuerpos IgG mediante ELISA y de anticuerpos neutralizantes por la técnica de neutralización por reducción de placas (PRNT, por sus siglas en inglés) con muestras pareadas e incluyendo múltiples flavivirus de acuerdo a la situación epidemiológica de cada país
Una seroconversión (resultado negativo en la primera muestra y positivo en la segunda), un aumento de más de 4 veces de los títulos de anticuerpos en muestras pareadas, o títulos detectables de anticuerpos contra la fiebre amarilla en una muestra post-virémica (PRNT 90%) es presuntivo de infección por fiebre amarilla
OPS/OMS 2017
Otra técnica serológica para el Diagnóstico Presuntivo de una infección reciente en fase postvirémica
http://www.paho.org/hq/index.php?option=com_topics&view=rdmore&cid=7134&Itemid=40784&lang=es
Interpretación de los resultados serológicos y del diagnóstico diferencial
La reactividad cruzada de las técnicas serológicas observada principalmente en infecciones secundarias por flavivirus debe ser considerada en áreas donde existe co-circulación del virus de la fiebre amarilla con otros flavivirus y se recomienda: 1. Realizar en paralelo la detección de anticuerpos para otros flavivirus e interpretar
cuidadosamente los resultados tomando en cuenta el historial de vacunación, así como la información epidemiológica disponible
2. Incluir otros síndromes febriles y febriles-ictéricos como dengue, leptospirosis, malaria, hepatitis virales, entre otras, dependiendo del perfil epidemiológico del país o área afectada
Un caso de fiebre amarilla será confirmado mediante técnicas serológicas sólo si el diagnóstico diferencial de laboratorio, teniendo en cuenta el perfil epidemiológico del país, resulta negativo para otros flavivirus
http://www.paho.org/hq/index.php?option=com_topics&view=rdmore&cid=7134&Itemid=40784&lang=es
OMS/OPS
Positivo
Detección de anticuerpos IgM
OPS/OMS 2017
Infección reciente por otros flavivirus
Es importante incluir al menos y según la situación epidemiológica de la región o país a otros Flavivirus (Dengue, Zika, VNO, Encefalitis Japonesa y ESL). Si existen muestras disponibles considerar la realización de la PRNT en muestras pareadas en un Laboratorio de Referencia
Muestras: suero de fase aguda (colectado en los primeros 4 días de la FIS y muestras de necropsias (hígado , bazo y corazón)
LNR Arbovirus, CIDR, IPK cuenta con el diagnóstico para la confirmación de casos
Aislamiento viral Cultivos de células de Mamíferos. - Vero (Riñón de mono verde africano) Cultivos de células de Mosquitos -(Aedes albopictus) C6/36 HT
Diagnóstico Molecular por PCR PCR en tiempo Real 1. Extracción del ARN automatizado 2. PCR en Tiempo Real
Conservación de las muestras para su diagnóstico
• Colecta de las muestras en condiciones de esterilidad • Almacenamiento de las muestras de 4°C a -20°C (en dependencia de la muestra)
hasta su envío al LNR de Arbovirus del CIDR del IPK siempre en menos de 48 horas
• Mantener la cadena de frío en su trasportación • Acompañar las muestras del modelo de solicitud vigente de estudios
microbiológicos aprobado por el MINSAP, en el que el médico de asistencia completará todos los datos que en él se solicitan
• Garantizar que el modelo se almacene separado de las muestras clínicas, correctamente protegido para evitar su deterioro
• En los casos fatales colectar 1 cm3 de tejido en el momento de la necropsia y cubrir estos con solución salina en recipiente estéril. Importante que los tejidos se almacenarán en tubos individuales, no se deben mezclar aunque pertenezcan al mismo paciente. Todas las muestras de tejido se congelarán a -20°C hasta su envío al LNR de Arbovirus sino se realiza su traslado en menos de 48 horas al laboratorio
Criterios de rechazo de la muestra
Muestras derramadas Muestras en contenedores no idóneos (viales reutilizados) Muestras que vengan en viales con una numeración que no coincida con el
que aparece en la indicación clínica o sin numeración Muestra en que no se identifique en el vial/orden clínica el tipo de muestra
(suero, sangre, tejido, etc) Muestras en frascos de cristal Muestras tapadas con tapones de algodón Muestras de tejido de fallecidos o biopsias en formol Muestras de tejido todas juntas en el mismo vial Ordenes sin muestras
Nota: El envío de una muestra de fallecido debe de ser coordinado con anterioridad. Llamar al Laboratorio Nacional de Referencia de Arbovirus del CIDR del IPK para coordinar el estudio 72553554, 7 2553556.
Guzman et al., Nature Rev, 2011
Las muestras de elección para el diagnóstico de la FA son el suero , la sangre total o tejidos frescos
El Laboratorio Nacional de Referencia de Arbovirus del CIDR del IPK cuenta con el diagnóstico virológico y molecular de este virus para su detección en correspondencia con los propuesta planteada por la OMS-OPS En el caso de existir un brote el diagnóstico de laboratorio nos permitirá caracterizarlo así como certificar el cese del mismo