Diferencias Entre Celda Galvanica y Electrolitica
-
Upload
diego-ayala -
Category
Documents
-
view
961 -
download
21
description
Transcript of Diferencias Entre Celda Galvanica y Electrolitica
Celda
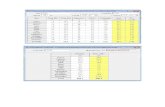
CaractersticasCelda ElectrolticaCelda Galvnica o Voltaica
EnergaHay que suministrar energa elctrica para su reaccinSu reaccin genera energa elctrica
ReaccinTiende a liberar gases, hay reaccin de xido-reduccinExiste una reaccin de xido-reduccin
FuncionamientoRequiere de energa externaRequiere de un puente salino
Tipo de reaccinQumica no EspontneaQumica Espontnea
Tipo de celdaEs electrolticaEs electroqumica
ProductoProduce una reaccin de descomposicin en base a los electrones que circulan por la solucin electroltica.Produce una reaccin y como consecuencia de esa reaccin se liberan electrones producindose una diferencia de potencial.
# de reaccionesEs una reaccin directa Existen semireacciones unidas por un puente salino
FenmenoElectrlisisCorrosin
Traslado del voltajeConduccin de electrones a travs del electrolitoMediante flujo de electrones en el puente salino
Direccin de e-Del nodo al ctodo Del nodo al ctodo
Reacciones involucradasEn el electrodo andico ocurren oxidacionesEn el electrodo catdico ocurren reduccionesEn la semicelda andica ocurren oxidacionesEn la semicelda catdica ocurren reducciones
nodo y CtodoUn electrodo funciona como nodo y el otro como ctodoUna semicelda acta como nodo, y la otra como ctodo
IonesMovimiento de iones en la solucin Movimiento de iones en la solucin
CircuitoEl circuito externo afecta a la reaccinEl circuito externo se complementa con la solucin










![Celda de flotacion de Laboratorio EDEMETid85]1.pdf · Title: Celda de flotacion de Laboratorio EDEMET Author: EDEMET Subject: Celda de flotacion Keywords: celda de flotacion; concentracion](https://static.fdocuments.co/doc/165x107/5ba4202109d3f2c0278ce248/celda-de-flotacion-de-laboratorio-id851pdf-title-celda-de-flotacion-de-laboratorio.jpg)