e Structur a Protein As
-
Upload
darinka-mendoza-espinoza -
Category
Documents
-
view
27 -
download
0
Transcript of e Structur a Protein As

ESTRUCTURA
DE PROTEÍNAS

Proteínas: • Biopolímeros
• 50% peso seco de la > de organismos.
• Versatilidad de funciones.
• Expresan la información genética.
• Secuenciación
• Const. de aa.

Clasificación:
•Enzimas

Enzimática Son las más numerosas y especializadas. Actúan como biocatalizadores de las reacciones químicas.
ENZIMA-SUSTRATO
PROTEASADE ADENOVIRUS
SITIO ACTIVO DE LA
CARBOXILASA

Clasificación:
•Enzimas
•Transporte


TransporteHemoglobina Hemocianina Citocromos Canales iónicos
CITOCROMOS

Clasificación:
•Enzimas
•Transporte
•Defensa

Defensa•Inmunoglobulinas •Trombina y fibrinógeno
ANTICUERPOS

Clasificación:
•Enzimas
•Transporte
•Defensa
•Reserva o Nutritivas

FUNCIONES DE PROTEÍNAS Y EJEMPLOS
Reserva
•Ovoalbúmina, de la clara de huevo
•Gliadina, del grano de trigo
•Lactoalbúmina, de la leche
•Transferrina
ALBÚMINA
TRANSFERRINA

Clasificación:
•Enzimas
•Transporte
•Defensa
•Reserva o Nutritivas
•Contráctiles y Mótiles
Actina


Clasificación:
•Enzimas
•Transporte
•Defensa
•Reserva o Nutritivas
•Contráctiles y Mótiles
•Estructurales

Receptor de LHEstructural
Como las glucoproteínas que forman parte de las membranas. •Las histonas que forman parte de los cromosomas •El colágeno, del tejido conjuntivo fibroso. •La elastina, del tejido conjuntivo elástico. •La queratina de la epidermis.
COLÁGENO
GLUCOPROTEÍNAS MEMBRANALES

Clasificación:
•Enzimas
•Transporte
•Defensa
•Reserva o Nutritivas
•Contráctiles y Mótiles
•Estructurales
•Reguladoras

Hormonal
•Insulina y glucagón •Hormona del crecimiento •Calcitonina •Hormonas troficas (LH, FSH, TSH)
FSH
TRANSDUCCIÓNDE SEÑALES

ANFÓTERO: presentar una base y un ácido al mismo tiempo (pH fisiológico).
ZWITTERION: Molécula con igual número de cargas positivas que nagativas.
C
CC
R
HNH3
+O
OAMINOÁCIDOS

1806 Asparagína Espárrago
1938 Treonina
Ac. Glutámico Glúten del trigo
Glicina Por su sabor dulce
20 aa Diferentes, Estándar,
Primarios o Normales


HIDROFÓBICOS

HIDROFÍLICOS

• Fosfoserína
• 4-hidroxiprolina
• -hidroxilisina
•N-metil-lisina
• Ac. carboxiglutamina Protrombina
Colágeno
Miosina
Aminoácidos modificados

ENANTIÓMEROS
C
C
R1
HNH3
+
OO
C
C
R1
H NH3
+
O O
Carbón
IMÁGENES ESPECULARES
L- aa D- aa

Aminoácido Rotación []D25 oC
Específica
L-Alanina + 1.8
L-Arginina + 12.5
L-Isoleucina + 12.4
L-Fenilalanina - 34.5
Ácido L-glutámico + 12.0
L-Histidina - 38.5
L-Lisina + 13.5
L-Serina - 7.5
L-Prolina - 86.2
L-Treonina - 28.5

Curva de Valoración de la Glicina
www.um.es/.../Quimica/Practica01/Practica01.htm
H3+N-CHR-COOH
2.34 H3+N-CHR-COOH H3
+N-CHR-COO-
H3+N-CHR-COO-
5.97
H2N-CHR-COO-
9.6
H3+N-CHR-COO- H2N-CHR-COO-

TITULACIÓN DEL
ÁCIDOGLUTÁMICO Glu
Equivalentes de NaOH
pKCOOH=2.19pKR =4.25pKNH2 =9.67

ESPECIALESÁCIDOSBASICOS
pK’s DE AMINOÁCIDOS

ENLACE PEPTÍDICO
EnlaceAMIDA
CC
O
NH
C
CC
O
NH
C
+
-

DipéptidoTripéptidoTetrapéptido… Oligopéptido
Polipéptido
Ionización de: Gpo. –N terminal Gpo. – C Terminal Gpo. R de los aa
H
H2N- C- COOH
R
H
H2N- C- COOH +
R
H H
N- C- COOH
R
H O
H2N- C- C
R Enlace peptídico
H2O
+

ESTRUCTURA DE PROTEÍNAS• La variedad de secuencias de aminoácidos
(proteínas) es infinita
• Una proteína de 100 aa puede tener 10020 secuencias diferentes.
• En promedio, una proteína de 300-400 aa tiene un peso molecular de 30-45 Kda (30,000 45,000 Da)

Estructura Tridimensional de las Proteínas
Hsp 70

TRANSCRIPCIÓN
TRADUCCIÓN
Ribosomacodón
Membrana nuclear
Nucleótidos
de RNACadena de
polipeptídos
Anticodón
Aminoácidos
1er. Nivel de organización

SÍNTESIS DE PROTEÍNAS

ESTRUCTURAS SECUNDARIAS
N-
-C
-C
-N
Secuencia de
aminoácidos
especificada por la
información
genética.
EXTREMOAMINO (N)
EXTREMOCARBOXILO (C)
Estructura Primaria



ESTRUCTURAS SECUNDARIAS
N-
-C
-C
-N
Plegamiento de la cadena polipeptídica formando arreglos.
Lámina Estructura Secundaria
Hélice
Hélice-GiroHélice
Giro-Hélice-Giro
Lámina


TERCIARIA: Forma globular Funcionalidad.
Estructura

ESTRUCTURAS SECUNDARIAS
N-
-C
-C
-N
Estructura Cuaternaria
Uniones de 2 o más subunidades,
monómeros o protómeros).

1.HOLOPROTEÍNASFormadas solamente por aminoácidos
2.HETEROPROTEÍNASo Proteínas ConjugadasFormadas por una fracción protéica y por un grupo no protéico, que se denomina "grupo prostético
CLASIFICACIÓN DE PROTEÍNAS

Proteína Gpo.Prostético / Característico
Ejemplo
Glucoproteínas Carbohidratos Globulina de la sangre
Lipoproteínas Lípidos Lipoproteína de la sangre
Fosfoproteínas Grupo fosfato Caseína de la leche
Hemoproteína Hemo Hemoglobina
Flavoproteína Núcleo de Flavina Succinato Deshidrogenasa
Metaloproteína Fe,
Zn
Ferritina
Alcohol Deshidrogenasa
Proteínas Conjugadas


Descubrimiento de las Estructuras Polipépt. Regulares
S. XX1930. Quim. Linus Pauling
1950´s Principios:
Difracción de Rayos X.De aa. y péptidos
1. La longitud y ángulos de enlace deberían desviarse lo menos posible de los hallados por DRX.

Gpo. péptido trans
Plano Amida
Enlace peptídico
2. Dos átomo no pueden hacercarse uno al otro a una distancia menor de la que les permiten sus radios de Van der Waals.

3. El gpo. Amida debe permanecer en un plano de conf. Trans, así es posible la rotación alrededor de los 2 enlaces adya-centes al C- de cada residuo de aa.

4. Es preciso algún tipo de enlace no covalente para estabilizar un plegado regular

Fig 6.3
Hélice Lámina

Fif. 6.4
Hélice 310 Hélice

Fig 6.5
Anillo Hélice (a derechas Hélice (a derechas Cinta plana Hélice (a izquierdas


Fig 6.3
Hélice

Fig 6.6

Fig 6.8
Representaciones de Ramachandran
A Ramachandran plot of Ala-Ala-Ala is nearly identical to the plot for Phe-Phe-Phe (which is unbranched at the beta carbon (the



employees.csbsju.edu/.../olunderstandconfo.html

2 Clases deProteínas:
FibrosasGlobulares:
Fibrosas: materiales estructurales de células y tejidos.
Forma filamentosa o alargada
La > su función: estructural.
El % en: PielTej. ConjuntivoFibras animales: pelo, seda
QueratinaFibroina
ColágenoElastina

A.A. -Queratina Fibroina Colágeno Elastina (lana) (Seda) (Tendón de Bovino) (Aorta Porcina)

QueratinasQueratina

Queratina
Estructura de lámina
Plumas de Aves Escamas de Reptiles

Fibroína

Colágeno
Fig.: Osteoblastos sobre un ribete de osteoide. El osteoide se observa como un material finamente fibrilar de color gris y por debajo del mismo se situa el hueso mineralizado en color negro (Microscopía electrónica x 3400).

ColágenoTropocolágeno


Elastina
Ligamentos
Vasos Sanguíneos
Edo. Relajado
Estiramiento
Monómero de elastina
Entrecruzamiento

Actina y
Miosina
Tubulina

Globulares:.
La cadena se encuentra plegada localmente formando una estructura secundaria (helice , lámina , etc.), a su vez estas regiones se pliegan unas sobre otras, para formar la estructura terciaria.


ESTRUCTURA TERCIARIA
ADENILATO CINASA
Modelo de Relleno Modelo de cintas

Modelo de RellenoModelo de cintasModelo esquelético

Miohemeritrina Prealbúmina
Piruvato quinasa, dominio 1
Hexoquinasa, dominio 2
a) Predominantemente hélice
Proteína de la cubierta del virus del mosaico de tabaco Inmunoglobulina, dominio V2
b) Predominantemente lámina c) Hélice y lámina mezcladas

Variedades de la estructura de las proteínas
La > formadas por mas de un DominioRegión compacta, plegada localmente, de la estructura 3aria.
•Conectados entre sí.
•C/u realiza una función diferente.
•Un tipo puede reconocerse en dif. proteínas

Miohemeritrina Prealbúmina
Piruvato quinasa, dominio 1
Hexoquinasa, dominio 2
a) Predominantemente hélice
Proteína de la cubierta del virus del mosaico de tabaco Inmunoglobulina, dominio V2
b) Predominantemente lámina c) Hélice y lámina mezcladas
Sandwich
Cilindro antiparalelo

ESTRUCTURA TERCIARIA

Reglas generales que rigen el plegado terciario•Prots. Glob. poseen interior y exterior definidos
Cit.c corazón de caballo


Reglas generales que rigen el plegado terciario
•Prots. Glob. poseen interior y exterior definidos.
•Las láminas gral. Enrrolladas en estruct. Cilíndrica. Con enrollamiento a izquierda. (aa L).
•Cadena polipept. Con doblamiento en esquinas de dif. Formas (usa 4 residuos)
•Prot. Glob., No todas las partes se pueden clasificar, hélice o lámina

•Expont.
•La secuencia aa
•Temperatura
•pH extremo
•Disolv. Org.
DesnaturalizaciónRenaturalización
Molécula Nativa
Molécula DesnaturalizadaTemperatura oC
Fra
cció
n d
esp
leg
ada
Ribonucleasa
¿Qué es lo que determina la estructura 2aria y 3aria?
•Favor Termodinámico


PUENTES DISULFURO

Estado desnaturalizadoEstado nativo

ESTRUCTURA CUATERNARIA
OXIHEMOGLOBINA
HEMOGLOBINA

Proteínas Oligoméricas
Proteína P.M.
No. de Residuos
No. de Cade-nas
Insulina (bovina) 5 733 51 2
Ribonucleasa (páncreas de bovino) 12640 124 1
Lisozima (clara de huevo) 13930 129 1
Mioglobina (corazón de caballo) 16890 153 1
Quimotripsina (páncreas de bovino) 22600 241 3
Hemoglobina (humano) 64500 574 4
Seroalbúmina (humano) 68500 550 1
Hexoquinasa (levadura) 96000 800 4
-Globulina (caballo) 149900 1250 4
Glutamato deshidrogenasa (hígado de buey) 1000000 8300 40


Organización Cuaternaria
Homotípica: Asociación entre cadenas polipeptídicas
idénticas o casi idénticas
Heterotípica:Interacción entre subunidades con
estructura muy distinta.
Múltiples subunidades

Simetría helicoidal
Simetría icosaédrica
Simetría C4
Simetría C2 Simetría C3
Simetría D2
Simetría cúbica
Motivo asimétrico

Actina
Virus del mosaico de tabaco.

Dimero de prealbúmina2 monoméros forman el sandwich completo

ASOCIACIONES ENTRE PROTEÍNAS
Polimerización de la fibrina Coágulo sanguíneo
Tubulina

ASOCIACIONES ENTRE PROTEÍNAS Y LÍPIDOS
Membrana biológica
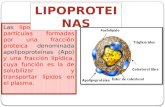
Lipoproteína del plasma sanguíneo

ASOCIACIONES ENTRE PROTEÍNAS Y ÁCIDOS NUCLEICOS
Nucleosoma
Virus HIV (SIDA)
Ribosomas

Proteoglicano de tipo muy grande
Peptidoglicano de la pared celular bacteriana



REPRESOR NATURAL
ANÁLOGO


ESTRUCTURA TERCIARIA ESTRUCTURA SECUNDARIA



REPRESENTACIONESGRÁGICAS DE LAS
PROTEÍNAS
ENTRAR EN LA SIGUIENTE PÁGINA PARA VER UNA PROTEÍNA TRIDIMENSIONAL
(Se abre en una página diferente)
http://www.mgh.harvard.edu/labmed/res/reslab/album.swf
ALBÚMINA HUMANA

PROPIEDADES DE PROTEINAS ESPECIFICIDAD
• Función determinada debido a que posee una estructura primaria y una conformación espacial propia.• Cambio en la estructura genera una pérdida de la función.• Diferentes en todos los organismos.• Cada individuo posee proteínas específicas
(rechazo de órganos transplantados). • La semejanza entre proteínas son un grado de parentesco entre individuos
(construcción de "árboles filogenéticos" )