EVOLUCIÓN DEL MODELO ATÓMICO
description
Transcript of EVOLUCIÓN DEL MODELO ATÓMICO
Diapositiva 1
EVOLUCIN DEL MODELO ATMICO
EVOLUCIN DEL MODELO ATMICO
2
La materia esta formada por partculas muy pequeas (tomos), las cuales son indivisibles y no se pueden destruir.
Los tomos de un mismo elemento son iguales entre si, tienen su propio peso y propias cualidades.TEORA ATOMICA DE DALTONLos tomos permanecen sin divisin, an cuando se combinan en las reacciones qumicas.
Los tomos al combinarse para formar compuestos guardan relaciones simples.
Los tomos de elementos diferentes se pueden combinar en proporciones distintas y formar ms de un compuesto.
* Los compuestos qumicos se forman al unirse tomos de dos o ms elementos distintos.
3
4 Explicaba el hecho de que la materia fuese elctricamente neutra, pues en los tomos de Thomson la carga positiva era neutralizada por la negativa.
Los electrones podran ser arrancados de la esfera si la energa en juego era suficientemente importante.
Era un modelo esttico.
TEORA ATOMICA DE THOMSONEste modelo postula que:
El tomo consista en una esfera uniforme de materia cargada positivamente en la que se hallaban incrustados los electrones de un modo parecido a como lo estn las semillas en una sanda.
5TEORA ATOMICA DE RUTHERFORD Los ELECTRONES se ubican en una corteza orbitando al ncleo en rbitas circulares o elpticas con un espacio vaco entre ellos.
Se trataba de un modelo dinmico.
El nmero de electrones tena que ser igual al nmero de protones: Materia es neutra.
Este modelo postula que:
La parte positiva (PROTONES) se concentra en un ncleo, el cual tambin contiene virtualmente toda la masa del tomo.
Se intua la presencia en el ncleo de unas partculas llamadas NEUTRONES, que eran partculas sin carga elctrica.
6
EXPERIMENTO DE RUTHERFORD
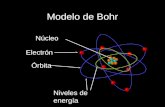
7TEORA ATOMICA DE BOHREste modelo postula que:
Los electrones giran alrededor el ncleo en rbitas circulares de radios definidos (no todas las rbitas son posibles).
Cada una de las rbitas solo puede tener un nmero determinado de electrones con una energa determinada (energa creciente de los niveles electrnicos).
Para que un electrn cambie de rbita, es necesario modificar su energa en una cantidad determinada.
8TEORA ATOMICA ACTUAL(Schrdinger, Plank, Heisemberg, Chadwichk) Un tomo est formado por el ncleo y la corteza.
En el ncleo se encuentran los protones (carga positiva y m= 1.6710-27 kg) y neutrones (sin carga y masa similar a la de los protones).
La corteza es la parte exterior del tomo.
En la corteza se encuentran los electrones (carga negativa y m= 9.1110-31 kg , unas 2.000 veces ms pequea que la de los protones). Todos los tomos son neutros :
n Electrones = n Protones
Los electrones no describen rbitas definidas alrededor del ncleo sino que los electrones se distribuyen en nubes electrnicas llamadas ORBITALES.
9TEORA ATOMICA ACTUAL(Schrdinger, Plank, Heisemberg, Chadwichk)ORBITAL: Regin del espacio, alrededor del ncleo, donde la probabilidad de encontrar un electrn , con una energa determinada es muy alta.
Los orbitales estn agrupados en NIVELES ENERGTICOS de orden creciente.
En cada orbital puede haber un mximo de 2 electrones.
Cada nivel energtico est formado a su vez por subniveles (s, p, d, f).
NIVELES Y SUBNIVELES ENERGTICOS :
SUBNIVELES : s, p, d, f
ESTRUCTURA ATMICA