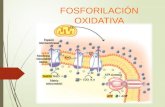
FOSFORILACION OXIDATIVA
-
Upload
miiguel-fdz-saucedaa -
Category
Documents
-
view
18 -
download
0
Transcript of FOSFORILACION OXIDATIVA

INSTITUTO TECNOLOGICO DE DIURANGO
ALUMNO: MIGUEL ANTONIO FERNANDEZ SAUCEDA DOCENTE: M.C. DULCE MARIA REYES HINOSTROZA

FOSFORILACION OXIDATIVA
La oxidación del alimento durante la respiración libera energía química
potencial que es utilizada para sintetizar ATP. El proceso implica la fosforilación
oxidativa de moléculas alimenticias como glucosa, ácidos grasos o glicerina
(las más comunes). Las moléculas son descompuestas durante
una serie de reacciones, y la energía liberada en ciertos estadios
del proceso es utilizada para producir ATP en reacciones de
fosforilacion.
CADENA DE TRANSPORTE DE ELECTRONES
La cadena de transporte eléctrico (CTE) mitocondrial, que también se
denomina sistema de transporte eléctrico, es un conjunto de transportadores
eléctricos situados en la membrana interna, en orden creciente de afinidad
electrónica, que transfiere los electrones que proceden de las coenzimas
reducidas hasta el oxigeno (existen otros sistema de transporte electrónico
dentro de las células.
Componentes del transporte eléctrico
Los componentes de la CTE de los eucariotas se encuentran en la
membrana mitocondrial interna, la mayoría de los componentes es tan
organizada en cuatro complejos, cada uno de los cuales constan de varias
proteínas y grupos prostéticos. Se describen brevemente cada complejo y las
funciones de las otras moléculas, la coenzima Q (ubiquinona, UQ y el cito
cromo c (cit c)

Inhibidores del transporte eléctrico
Han sido muy valiosos para determinar el orden correcto de los
componentes de la CTE cuando se han utilizado junto con las medidas del
potencial de reducción.
SISTEMA MITOCONDRIAL
En el proceso citoplásmico de la glucólisis se produce NADH. Estos
equivalentes reductores deben poder entrar a la mitocondria para ser utilizados
en la cadena de transporte de electrones para su oxidación aérobica. Así
mismo, los metabólicos mitocondriales como el oxaloacetato y acetil-CoA,
precursores de la biosíntesis mitocondrial de glucosa y ácidos grasos
respectivamente, deben poder abandonar la mitocondria. En la mitocondria, se
produce una enorme cantidad de energía en forma de ATP, después de la
ocurrencia de la fosforilación oxidativa, esta importante molécula energética,
debe abandonar la mitocondria para poder intervenir en múltiples reacciones
citoplásmicas.
El ATP generado en la fosforilación oxidativa a partir de ADP y Pi se
utiliza en el citoplasma; el Pi así formado, retorna al interior mitocondrial vía un
simportador Pi-H+ alimentado por el componente D pH del gradiente
electroquímico de protones. Entonces el gradiente del potencial electroquímico
generado por el bombeo redox de protones del transporte electrónico, es el
responsable de mantener los altos niveles mitocondriales de ADP y Pi, además
de proveer de la energía libre para sintetizar ATP.

La respiración
Todas las células necesitan tener energía para poder realizar todas sus
funciones y esta energía se obtiene por medio del catabolismo realizado en la
mitocondria.
En este proceso son degradadas moléculas complejas en otras más
simples, así como la glucosa que es degradada a dióxido de carbono y agua
con liberación de energía.
BALANCES ENERGETICOS
El metabolismo aeróbico es más eficiente que la glicólisis anaeróbica en lo
que se refiere a producción de ATP.
Sin embargo, como la concentración de enzimas de la glicólisis es alta, de
modo que si no están inhibidas, el ATP puede producirse más rápido que a
través de la fosforilación oxidativa.

Por otra parte, el cálculo tradicional de 36 ATP o de 38 ATP, según funcione
la lanzadera del glicerofosfato o del malato respectivamente, es obsoleto.
Mediciones recientes estiman 30 ATP por glucosa totalmente metabolizada.
La producción de ATP aeróbica es más eficiente que la producción anaeróbica.
En 1861, Louis Pasteur observó que en levadura expuesta a condiciones aeróbicas, el consumo de glucosa y la producción de etanol decae precipitadamente (Efecto Pasteur).
Glicólisis anaeróbica:
Metabolismo aeróbico de la glucosa:
Sin embargo, como la concentración de enzimas de la glicólisis es alta, de modo que si no están inhibidas, el ATP puede producirse más rápido que a través de la fosforilación oxidativa.
Por otra parte, el cálculo tradicional de 36 ATP o de 38 ATP, según funcione
la lanzadera del glicerofosfato o del malato respectivamente, es obsoleto.
Mediciones recientes estiman 30 ATP por glucosa totalmente metabolizada.
AGENTES DESACOPLANTES E INHIBIDORES
La vía del flujo de electrones a través del ensamblaje para el transporte de
los mismos, y las propiedades únicas de la PMF, han sido determinadas por
medio del uso de varios antimetabolitos importantes. Algunos de estos agentes
son inhibidores del transporte de electrones en sitios específicos en el
ensamblaje de transporte de electrones, mientras otros estimulan el transporte
al descargar el gradiente de protones. Por ejemplo, la antimicina A es un
inhibidor específico del citocromo b. En presencia de antimicina A, el citocromo
b puede ser reducido pero no oxidado. Como es de esperarse, en presencia de

la antimicina A el citocromo c permanece oxidado, así como también los
citocromos posteriores a y a3.
Inhibidores de la Fosforilación Oxidativa
Inhibidores de la cadena que bloquean la cadena respiratoria.
La rotenona, toxina de una planta, utilizada por indios amazónicos como
veneno, también ha sido usada como insecticida.
Nombre Función Sitio de Acción
Rotenona inhibidor del transporte de e– Complejo I
Amital inhibidor del transporte de e– Complejo I
Antimicina A inhibidor del transporte de e– Complejo III
Cianuro inhibidor del transporte de e– Complejo IV
Monóxido de Carbono inhibidor del transporte de e– Complejo IV
Azida inhibidor del transporte de e– Complejo IV

Actúa a inhibiendo el complejo I. Inhibe la re oxidación del NADH, no afecta
la del FADH2. Inhibe la oxidación del malato, que es dependiente del NAD+, no
así la del succinato. El succinato entra en el segundo punto de entrada a la
cadena, posterior al del NAD+.
El amital (barbitúrico) inhibe al complejo I, afecta las oxidaciones
dependientes del NAD+.
La antimicina A (Antibiótico).
Actúa a inhibiendo el complejo III. Inhibe la re oxidación del NADH y del
FADH2.
El cianuro bloquea el paso de electrones del citocromo a3 al oxígeno.
Estos inhibidores detienen el paso de electrones de modo que no hay
bombeo de protones. Sin gradiente de protones, no hay síntesis de ATP.
CONTROL DE FOSFORILACION OXIDATIVA
Permite a la célula producir solo la cantidad de ATP que se requiere de
inmediato para mantener sus actividades .el transporte electrónico y la síntesis
de ATP estrechamente acopladas. El valor del cociente P/0(el número de
moles de Pi que se consumen para que se reduzca cada átomo de oxígeno a
H2O) refleja el grado que acoplamiento que se observa entre el transporte
eléctrico y la sistesis de ATP. El cociente máximo medido para la oxidación del
NADH es 2.5 el cociente P/0 maximo para el FDH2 es 1.5 el control de la
fosforilacion oxidativa por la concentración de ATP esta ilustrada por el hecho
de que las mitocondrias solo pueden oxidar el NADH y elFADH2 cuando a hay
una concentración suficiente de ADP se convierte con el tiempo en ATP. En
este punto, disminuye mucho el consumo de oxígeno. Este aumenta
considerablemente cuando se suministra ADP. El control de la respiración
aerobia por el ADP se domina control respiratorio. La formación de ATP parece
estar fuertemente relacionada con el cociente de acción de masas del ATP

([ATP]/ [ADP][Pi]. En otras palabras, la ATP sintasa se inhibe por una
concentración elevada de su producto (ATP) y se activa cuando las
concentraciones de ADP y Pi son elevadas. Las cantidades relativas de ATP y
ADP dentro de las mitocondrias están controladas en gran medida por las
proteínas de transporte de la membrana interna: el translocalizador ADP-ATP
y el transportador de fosfato.
El translocalizador ADP –ATP es una proteína dimerica responsable del
intercambio del ATP intramitocondrial por el ADP producción en el citoplasma.
LA OXIDACION COMPLETA DE GLUCOSA
Los organismos aerobios (heterótrofos), extraen energía libre de la glucosa
que obtienen de sus alrededores al oxidarla con O2, que también obtienen de
los alrededores. Los productos finales de este metabolismo oxidativo el CO2 y
H2O se regresan a los alrededores. En este proceso los alrededores sufren de
un incremento en la entropía mientras que el organismo permanece en un
estado estacionario t no presenta un cambio en su orden interno. A pesar de
que existe un cambio en la entropía debido a la desaparición de calor, la
entropía también está relacionada con otro tipo de orden, que se ilustra a
continuación en la reacción de oxidación de la glucosa:
C6H12O6 + 6O2 ® 6 CO2 + 6 H2O

Los átomos contenidos en una molécula de glucosa más 6 moléculas de
Oxígeno, un total de 7 moléculas, están ahora, después de la oxidación de la
glucosa, repartidas en 12 moléculas (6CO2 + 6H2O).
LA OXIDACIÓN COMPLETA DE UNA ACIDO GRASO
Es un mecanismo clave para la obtención de energía metabólica (ATP) por
parte de los organismos aeróbicos. Dado que los ácidos grasos son moléculas
muy reducidas, su oxidación libera mucha energía; en los animales, incluido el
hombre, su almacenamiento en forma de triacilgliceroles es más eficiente y
cuantitativamente más importante que el almacenamiento de glúcidos en forma
de glucógeno.
La β-oxidación de los ácidos grasos lineales es el principal proceso
productor de energía, pero no el único. Algunos ácidos grasos, como los de
cadena impar o los insaturados requieren, para su oxidación, modificaciones de
la β-oxidación o rutas metabólicas distintas. Tal es el caso de la α-oxidación, la
ω-oxidación o la oxidación peroxisómica.
La oxidación de los ácidos grasos insaturados requiere algunas variantes de la
β-oxidación en la que participan algunos enzimas especiales, como la enoil-
CoA isomerasa.
α-oxidación
Artículo principal: alfa oxidación
En la α-oxidación, que es especialmente importante para el metabolismo de
ácidos grasos ramificados, se hidroxila el carbono α. Tiene lugar en el retículo
endoplasmático y en la mitocondria, donde interviene la oxidasa de función
mixta, y en el peroxisoma, donde interviene una hidroxilasa.
Otra ruta minoritaria para la oxidación de ácidos grasos es la ω-oxidación,
que tiene lugar en el retículo endoplasmático de muchos tejidos; se produce

una hidroxilación sobre el carbono metílico (–CH3) en el extremo de la molécula
opuesto al grupo carboxilo (–COOH).
ESTRÉS OXIDATIVA
Es causado por un desequilibrio entre la producción de especies reactivas
del oxígeno y la capacidad de un sistema biológico de decodificar rápidamente
los reactivos intermedios o reparar el daño resultante. Todas las formas de vida
mantienen un entorno reductor dentro de sus células. Este entorno reductor es
preservado por las enzimas que mantienen el estado reducido a través de un
constante aporte de energía metabólica. Desbalances en este estado normal
redox pueden causar efectos tóxicos a través de la producción de peróxidos y
radicales libres que dañan a todos los componentes de la célula, incluyendo las
proteínas, los lípidos y el ADN.
En el ser humano, el estrés oxidativo está involucrado en muchas
enfermedades, como la aterosclerosis, la enfermedad de Parkinson,
encefalopatía miálgica, sensibilidad química múltiple, y la enfermedad de
Alzheimer y también puede ser importante en el envejecimiento. Sin embargo,
las especies reactivas de oxígeno pueden resultar beneficiosas ya que son
utilizadas por el sistema inmunitario como un medio para atacar y matar a los
patógenos. Las especies reactivas del oxígeno son también utilizadas en la
señalización celular. Esta es denominada señalización redox.

Efectos químicos y biológicos
En términos químicos, el estrés oxidativo es un gran aumento (cada vez
menos negativo) en la reducción del potencial celular o una gran disminución
en la capacidad reductora de los pares redox celulares como el glutatión.[1] Los
efectos del estrés oxidativo dependen de la magnitud de estos cambios, si la
célula es capaz de superar las pequeñas perturbaciones y de recuperar su
estado original. Sin embargo, el estrés oxidativo severo puede causar la muerte
celular y aún una oxidación moderada puede desencadenar la apoptosis,
mientras que si es muy intensa puede provocar la necrosis.[2]
Un aspecto particularmente destructivo del estrés oxidativo es la producción
de especies de oxígeno reactivo, que incluyen los radicales libres y los
peróxidos. Algunas de las menos reactivas de estas especies (como el su
peróxido) pueden ser convertidas por una reacción redas con metales de
transición u otros compuestos de ciclo redox en quinonas, especie radical más
agresiva que puede causar extenso daño celular.[3] La mayoría de estas
especies derivadas del oxígeno se producen en un nivel bajo en condiciones
normales de metabolismo aeróbico y el daño que causan a las células es
reparado constantemente. Sin embargo, bajo los graves niveles de estrés
oxidativo que causa la necrosis, el daño produce agotamiento de ATP
impidiendo la muerte celular por apoptosis controlada, provocando que la célula
simplemente se desmorone.[
FOTOFOSRILACION
Durante la fotosíntesis la energía luminosa captura por el foto sistema de un
organismo se traduce (es decir, se convierte de una forma gen otra) en energía
de enlace fosfato del ATP. Esta conversión se denomina fotofosforilacion. De
lo expuesto anteriormente está claro que entre la síntesis de ATP en las
mitocondrias y en los cloroplastos existen muchas semejanzas. Por ejemplo,
muchas de las moléculas y términos que se han visto en la respiración aerobia
son también relevantes cuando se considera la fotosíntesis. Además, en ambos
orgánulos el transporte eléctrico se utiliza para inducir un gradiente de
protones, que luego impulsa la síntesis de ATP. Aunque entre la respiración

aerobia y la fotosíntesis hay muchas diferencias, la diferencia esencial entre los
dos procesos es la conversión de la energía luminosa en energía redox por los
cloroplastos. Otra diferencia sustancial son las características de permeabilidad
de la membrana mitocondrial interna y la membrana tilacoide. Al contrario que
la membrana interna, la membrana tilacoide es permeable al MG2+ y al CL-por
lo tanto, elMG2+y CL- se mueve a través de la membrana tilacoide al
transportarse los electrones y los protones durante la reacción luminosa. El
gradiente electroquímico a través de la membrana tilacoide que impulsa la
síntesis de ATP consta, por lo tanto, principalmente de un gradiente de
protones que puede ser de hasta 3.5 unidades de pH.
CLOROFILA Y CLOROPLASTO
La característica esencial de la fotosíntesis es la absorción de energía
luminosa mediante moléculas de pigmento especializadas. Las clorofilas son
moléculas verdes de pigmento que se asemejan al hemo. La clorofila a
desempeña un papel principal en la fotosíntesis de los eucariotas, debido a que
la absorción de energía luminosa impulsa directamente los acontecimientos
foto químicos. La clorofila b actúa como un pigmento recolector de luz
absorbiendo energía luminosa y pasándola a la clorofila a. los carotenoides son
moléculas isoprenoides de color naranja que actúan o como protectores contra
las especies de oxigeno reactivas (ROS).
La membrana externa de cada orgánulo es muy permeable, mientras que la
membrana interna posee moléculas transportadoras especializadas que
regulan el tráfico molecular.
El estroma posee varias enzimas las que catalizan las reacciones
independientes de la luz y la síntesis de almidón, DNA y ribosomas. Existen
también diferencias notables entre los orgánulos. Por ejemplo, los cloroplastos
son sustancialmente más grandes que las mitocondrias.
L os pigmentos y las proteínas responsables de las reacciones de la
fotosíntesis dependientes de la luz se encuentra dentro de la membrana

tilacoide la mayoría de etas moléculas están organizadas en las unidades de
funcionamiento de la fotosíntesis.
LUZ
El sol emite energía en forma de radiación electromagnética, que se
propaga a través del espacio en forma de ondas, parte de las cuales chocan
con tra la tierra. La luz visible, la fuente de energía que impulsa la fotosíntesis,
ocupa una pequeña parte del espectro de radiación electromagnética.
Muchas de las propiedades de la luz se explican por su comportamiento
andulario. Las ondas de energía se describen mediante los términos siguientes:
1. Longitud de onda. La longitud de onda es la distancia entre la cresta de
una onda y la cresta de la onda siguiente.
2. Amplitud. La amplitud es la altura de la onda. La intensidad de la
radiación electromagnética (p. ej., la luminosidad de la luz) es
proporcional a a2.
3. Frecuencia. La frecuencia v es el número de ondas que pasan por un
punto del espacio por segundo.
A demás de comportarse como una onda, la luz visible (y otros tipos de
radiación electromagnética) exhiben propiedades de las partículas como
la masa y la aceleración
Una vez excitado un electrón, puede volver al estado base de varias
formas:
1. Fluorescencia. En la fluorescencia el estado excitado de una
molécula desaparece al emitir un fotón. Debido a que el electrón
excitado pierde inicialmente parte de la energía relajándose a un
estado vibratorio (energético) menor, una transición consecuencia de
la emisión de un fotón tiene. Una energía menor (longitud de onda
mayor) que la del fotón que se absorbió originalmente.

2. Transferencia de energía de resonancia.
La energía de excitación se transfiere a una molécula vecina
mediante una interacción entre orbitales moleculares adyacentes.
Una molécula vecina cuyo espectro de absorción se solape con el
espectro de emisión del cromoforo diana puede absorber los fotones
liberados cuando ese cromoforo vuelve a su estado basal.
3. Oxidación – reducción. Se transfiere un electrón excitado a una
molécula cercan menor fuerza que cuando ocupa un orbital
normalmente lleno. Una molécula con un electrón excitado es un
agente reductor fuerte. Vuelve a su estado basal reduciendo a otra
molécula.
4. Descenso sin radiación. La molécula excitada vuelve a su estado
basal convirtiendo la energía de excitación en calor.
REGULACION DE LA FOTOSINTESIS
La absorción y posterior reducción del nitrato por las plantas están
reguladas por diferentes señales ambientales y metabólicas, principalmente la
luz, el nitrato y diversas formas reducidas de nitrógeno y de carbono.
El nitrato promueve la síntesis de novo de su proteína de transporte a través
del plasmalema. Dicho transporte se halla regulado negativamente por la
presencia de amonio o de otras formas reducidas de nitrógeno, como la
glutamina. Una elevada concentración interna de nitrato también ejerce un
control negativo sobre su propia absorción.
El nitrato es también la principal señal que controla la síntesis de NR y de
NiR. En efecto, la adición de nitrato a las plantas produce en las mismas un
notable incremento de las actividades NR y NiR. Ambas son dos enzimas
inducibles por nitrato, aunque en algunas especies se observan unos bajos

niveles constitutivos. Tras la adición de nitrato se produce un rápido aumento
de la cantidad de niRNA de la NR y de la NiR como resultado de la activación
de la transcripción de los respectivos genes. Además, el nitrato también ejerce
un control positivo postranscripcional incrementando la estabilidad de los
mRNA y de las proteínas enzimáticas sintetizadas de Novo.
Aunque el nitrato es el inductor primario de la expresión de la NR y la NiR, la
luz incrementa la transcripción de ambos genes y el nivel de las proteínas que
codifican. Este efecto estimulador de la luz está mediado por el fitocromo. La
luz también ejerce su efecto regulador a través de productos de la fijación
fotosintética del CO2. En efecto, la adición de distintos azúcares (glucosa,
fructosa o sacarosa) a hojas mantenidas en oscuridad ocasiona un aumento de
la síntesis de mRNA similar al producido por la luz, especialmente en el caso
de la NR. Por otra parte, el nitrógeno reducido en forma de glutamina o de
glutamato reprime la síntesis de los mRNA de la NR y la NiR. Así pues, la
inducción de la transcripción de los genes de ambas enzimas parece estar
regulada por el balance interno entre azúcares solubles y aminoácidos, lo que
constituye una prueba de que el metabolismo del nitrógeno y el del carbono
están regulados entre sí.
Regulación a través de transcripción 1º) Proteína de regulación transcripcional
TOR es un quinase de proteína, blanco del rapamycin, y considerado para
ser un integrador de la disponibilidad nutriente (los aminoácidos y energía) y
como un jugador dominante del transduction alimento-mediado de la señal. Las
proteínas del TOR se conservan altamente en eukaryotes; está generalmente
presente en una copia del gene, pero en cereviase del saccharomyces hay dos
genes, Tor1 y Tor2. En el saccharomyces cerevisiae con fuentes preferidas del
nitrógeno, tales como amonio o glutamine, TOR1 y TOR2 son activos; y
consecuentemente los genes conforme a la regulación del catabolite del
nitrógeno se reprimen. En el contrario, con fuentes no preferentes del nitrógeno
o en la presencia de las fuentes preferidas del nitrógeno más rapamycin, la
expresión de los genes represión sensible del catabólito del nitrógeno se lanza.

La blanco del camino del transducción de la señal del TOR, referente a la
represión del catabólito del nitrógeno, es el factor positivo Gln3.
Proyecte para el papel del TOR en levadura en la presencia de alimentos, el
TOR que señala camino se requiere para la expresión de los genes necesarios
para la biogénesis ribosoma y la importación nuclear de los factores de la
transcripción responsables de la expresión de los genes inducidos por la
limitación del nitrógeno es restricta. Sobre la adición de la limitación nutriente o
del rapamycin, los genes requeridos para la biogénesis ribosoma se reprimen y
los factores de la transcripción requeridos para expresar los genes stress-
induced, genes reprimidos catabólito del nitrógeno, y ciertos genes del TCA
completan un ciclo, son todos importados en el núcleo (representado por las
líneas discontinuas).

BIBLIOGRAFIA
www.bioquimicaqui11601.ucv.cl/.../traselectfofox4fid.html
es.wikipedia.org/wiki/Quimiosmosis Burnie, David. Luz. Madrid: Ediciones Altea, 1992. Libro de divulgación
con ilustraciones de gran calidad. García, J. y otros. La luz: el ayer, el hoy, el mañana. Madrid: Alianza
Editorial, 1996. Microsoft ® Encarta ® 2008. © 1993-2007 Microsoft Corporation.
Reservados todos los derechos.