Guia p. Parasitologia Medica
-
Upload
gianmarco-silva -
Category
Documents
-
view
277 -
download
1
Transcript of Guia p. Parasitologia Medica

PARASITOLOGIA MEDICA Página 1
ASOCIACIÓN
UNIVERSIDAD PRIVADA SAN JUAN BAUTISTA
FACULTAD DE CIENCIAS DE LA SALUD
ESCUELA PROFESIONAL DE MEDICINA HUMANA
GUÍA DE PRÁCTICA
PARASITOLOGÍA MÉDICA
QUINTO CICLO
SEMESTRE ACADÉMICO 2013-II

PARASITOLOGIA MEDICA Página 2
INTRODUCCIÓN
Los diferentes procedimientos y técnicas de la enseñanza universitaria pueden
aplicarse en particular a la enseñanza de la Parasitología en concordancia con los
objetivos de esta última. En una ordenación lógica de hechos, primero deben
definirse claramente los objetivos y propósitos de la Parasitología, dentro del
conjunto orgánico de las materias que conforman un plan de enseñanza pre-
profesional, profesional o técnica, y más tarde realizar la selección de los métodos y
procedimientos más adecuados para alcanzar las metas fijadas.
De acuerdo con las tendencias actuales de la enseñanza Parasicológica, cualquiera
que sea la metodología escogida, ella supone la aplicación del principio del
aprendizaje activo en cuyo desarrollo el estudiante es un actor y no un mero
espectador del proceso enseñar-aprender, donde la incorporación de nuevos
conocimientos y su edificación conceptual se realiza a través de experiencias
personales, en un esfuerzo constante por descubrir nuevas relaciones hasta
alcanzar una comprensión integrada y madura de las materias del curriculum.
Algunos elementos parasitarios del tubo digestivo (los dibujos no guardan relación
de proporción entre ellas).
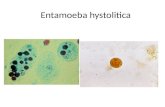
1. Trofozoito de Entamoeba histolytica
2. Quiste maduro de Entamoeba histolytica
3. Trofozoito de Entamoeba coli
4. Quiste maduro de Entamoeba coli
5. Quiste de Endolimax nana
6. Quiste de Iodamoeba bütschlii
7. Trofozoito de Giardia lamblia
8. Quiste de Chilomastix mesnili
9. Trofozoito de Chilomastix mesnili
10. Trofozoito de Trichomonas hominis
11. Trofozoito de Balantidium coli
12. Quiste de Balantidium coli

PARASITOLOGIA MEDICA Página 3
13. Trofozoito uninucleado de Dientamoeba fragilis
14. Trofozoito binucleado de Dientamoeba fragilis
15. Huevo de Taenia sp.
16. Proglótido grávido de Taenia saginata
17. Proglótido grávido de Taenia solium
18. Huevo de Diphyllobothrium pacificum
19. Proglótido grávido de Diphyllobothrium pacificum
20. Huevo de Hymenolepis diminuta
21. Huevo de Hymenolepis nana
22. Cápsula ovígera de Dipylidium caninum
23. Huevo de Fasciola hepatica
24. Huevo de Paragonimus mexicanus (=P. peruvianus)
25. Huevo de Schistosoma mansoni
26. Huevo lavado de Enterobius vermicularis
27. Huevo fértil de Ascaris lumbricoides
28. Huevo infértil de Ascaris lumbricoides
29. Huevo fértil decorticado de Ascaris lumbricoides
30. Huevo de Trichuris trichiura
31. Huevo de Ancylostoma duodenale o Necator americanus
32. Larva rabditoide de Strongyloides stercoralis
33. Huevo de Meloidogyne sp.
34. Huevo de Trichostrongylus sp.
Origen Vegetal:
35. Granos de almidón
36. Pelo vegetal
37. Pared celular vegetal
38. Gotas de grasa
39. Células vegetales en empalizada
40. Estructura vascular vegetal
41. Células vegetales
42. Grano de polen
43. Fibra de algodón

PARASITOLOGIA MEDICA Página 4
44. Hongos
45. Levaduras
Origen Mineral:
46. Fosfato amónico magnésica
47. Oxalato de calcio
48. Fosfato cálcico neutro
49. Ácido úrico
50. Cistina
51. Colesterol
52. Alucina
53. Sulfanilamida
54. Carbonato de calcio
55. Cristales de Charcot – Leyden
56. Ácidos grasos

PARASITOLOGIA MEDICA Página 5
AMEBIASIS
Definición:
Infección causada por el protozoario Entamoeba histolytica.
El parásito usualmente se localiza en la luz del intestino grueso del hombre,
pudiendo invadir la mucosa y por vía sanguínea alcanzar diversos órganos. Las
úlceras intestinales pueden ocasionar perforaciones. La infección es de distribución
cosmopolita.
El Parásito:
a. Morfología
Observe preparaciones microscópicas de heces coloreadas con hematoxilina
férrica y/o gomorritrichrome. Reconozca, con objetivo de inmersión, trofozoitos de
Entamoeba histolytica, distinguiendo la forma irregular del parásito, y la presencia
de núcleo esférico, con nucleolo central y cromatina fina en la pared interna de la
membrana nuclear (formas típicas). En algunas preparaciones pueden
observarse el ecto endoplasma, así como, pre quistes redondeados con un
núcleo.
Observe preparaciones microscópicas de heces coloreadas con lugol y con
objetivo de mayor aumento, reconozca quistes. En las prelaciones coloreadas
con hematoxilina férrica, pueden encontrar quistes con 1 a 4 núcleos y barras
cromidiales en el citoplasma.
b. Ciclo Biológico (estudie el esquema adjunto)
Relación hospedero-parásito: Observe la preparación microscópica de corte del
intestino grueso con una lesión ulcerativa. Reconozca la extensión y límites del
tejido sano y el lesionado. Ubique los trofozoitos de Entamoeba histolytica,
señalando las capas del intestino invadidas. Preste atención a los cambios de
tejido normal: necrosis, inflamación, etc. En algunas preparaciones pueden
observarse trofozoitos en el interior de los vasos sanguíneos.
La amibiasis extra intestinal más frecuente es el “absceso” (necrosis) hepático.

PARASITOLOGIA MEDICA Página 6

PARASITOLOGIA MEDICA Página 7
CICLO DE VIDA DE Entamoeba histolytica

PARASITOLOGIA MEDICA Página 8
GIARDIASIS
Definición:
Infección causada por el flagelado Giardia lamblia (=Giardia intestinalis). El trofozoito
se adhiere a la superficie de la mucosa del intestino delgado. En algunos casos se
puede producir el síndrome de mala absorción.
El Parásito:
a. Morfología
Observe trofozoitos vivos de Giardia. Preste atención al disco suctorio, y al
movimiento en vaivén. En preparaciones microscópicas coloreadas distinga los
núcleos, el funis (axostilo) y flagelos.
En preparaciones microscópicas de heces coloreadas con lugol observe los
quistes. Ponga atención a la forma, la posición de los núcleos, la presencia del
funis y flagelos.
b. Ciclo Biológico (estudie el esquema adjunto)
Relación hospedero-parásito: La acción mecánica del parásito sobre la
superficie de la mucosa intestinal, explica en parte, el síndrome de mala
absorción.

PARASITOLOGIA MEDICA Página 9
CICLO DE VIDA DE Giardia lamblia

PARASITOLOGIA MEDICA Página 10
BALANTIDIASIS
Definición:
Infección causada por un protozoo, el Balantidium coli, cuyo hábitat es el intestino
grueso.
El Parásito:
a. Morfología
Observe, a menor aumento, trofozoitos vivos y móviles, procedentes de heces de
cerdo. Reconozca la forma y tamaño, las filas ordenadas de cilios, cuya agitación
permanente permite los desplazamientos del parásito. Por transparencia puede
reconocerse la vacuola contráctil. En preparaciones microscópicas de heces de
cerdo, en fresco y coloreadas, identifique y dibuje los quistes. Preste atención a
la presencia de un solo elemento parasitario en cada quiste.
b. Ciclo Biológico (estudie el esquema adjunto)
Relación hospedero-parásito: Observe preparaciones microscópicas de intestino
grueso Balantidium coli. Preste atención a la presencia de los parásitos en las
diferentes capas del intestino. Observe la reacción inflamatoria en los bordes de
las lesiones, así como a la destrucción tisular.

PARASITOLOGIA MEDICA Página 11
CICLO DE VIDA DE Balantidium coli
OTROS PROTOZOARIOS INTESTINALES
Entamoeba sp.:
Trofozoitos: Observe preparaciones coloreadas de heces con Entamoeba coli.
Guiándose por el esquema adjunto, identifique la distribución de la cromatina nuclear
gruesa y adosada a la membrana; así como, la posición excéntrica del cariosoma.
Compare con sus observaciones de Entamoeba histolytica.

PARASITOLOGIA MEDICA Página 12
Quistes: En las mismas preparaciones anteriores y en otras de heces, teñidas con
lugol, identifique los quistes, redondeados, con 4 núcleos o más. En las
preparaciones coloreadas puede distinguir las características nucleares ya
mencionadas.
Iodamoeba bütschlii: Observe las preparaciones coloreadas de heces con
Iodamoeba bütschlii, guiándose por el esquema adjunto, identifique trofozoitos y
quistes ayudándose del esquema adjunto.
Endolimax nana: Observe preparaciones coloreadas de heces con Endolimax nana.
Identifique trofozoitos y quistes ayudándose del esquema adjunto.
Chilomastix mesnili: Observe preparaciones coloreadas de heces con Chilomastix
mesnili. Identifique quistes por la forma en “pera” de los mismos y los restos
flagelares en el citoplasma.

PARASITOLOGIA MEDICA Página 13
Cystoisospora belli (=Isospora belli)
La Isosporidiasis humana tiene como agente causal a Cystoisospora belli (=Isospora
belli), que es poco frecuente en nuestro medio.
Cystoisospora belli (=Isospora belli).
Parasita el intestino delgado del hombre. Es de ciclo de vida directo.
Ooquiste.- Se caracteriza por su forma ovoidea y la presencia de esporoblastos o de
dos esporoquistes. Su diámetro mayor oscila de 20 u por 10 u.
Cystoisospora belli (=Isospora belli): Observe preparaciones en fresco con
ooquistes, identifique los esporoquistes y los esporozoitos.

PARASITOLOGIA MEDICA Página 14
Cryptosporidium parvum
Es agente causal de la cryptosporidiasis en el hombre, siendo más afectados los
pacientes inmunoomprometidos, (SIDA).
El ooquiste es el elemento infectante, mide de 4 a 6 u de diámetro y contiene 4
esporozoitos.

PARASITOLOGIA MEDICA Página 15
Cyclospora cayetanensis
Coccidio causante de diarrea en niños y adultos. Es muy parecido a Cryptosporidium
parvum, pero de mayor tamaño.
Sarcocystis hominis
Es un parásito muy parecido a Toxoplasma sp. No se conoce con exactitud la
especie que parasita al hombre, pero es frecuente hallarlo en la musculatura del
ganado herbívoro.
Quiste.- Localizado en la musculatura en forma fusiforme o de “arrocillo”, mide de 1
a 5 cm de longitud, está rodeado de una pared gruesa, en la parte interna forma
numerosos tabiques y compartimientos, dentro de los cuales se encuentran
numerosos en forma de plátano que miden de 9 a 12 u por 2 a 4 u.
Ooquiste.- Mide 15 u en su diámetro mayor, tiene dos esporoquistes cada uno con
cuatro esporozoitos.

PARASITOLOGIA MEDICA Página 16
TRICOMONIASIS UROGENITAL
Definición:
Es una infección, esencialmente venérea causada por el protozoario flagelado
Trichomonas vaginalis, suele afectar a la mujer produciendo vulvovaginitis, y en el
hombre, en ocasiones, uretritis y prostatovesiculitis.
El Parásito: Trichomonas vaginalis
a. Morfología
Los trofozoitos: El protozoario sólo tiene estadio de trofozoito. Observe frotices
de secreción vaginal coloreados con Giemsa. Preste atención al núcleo, al
citoplasma finamente granulado, membrana ondulante, axostilo y flagelos.
Diferencie las células epiteliales vaginales de los parásitos, del polimorfo
nucleares y de las levaduras.
Observe las preparaciones microscópicas en fresco, preste atención a la forma
piriforme del parásito y al movimiento rápido, no direccional y rotatorio, cuando
se hace lento se puede observar la membrana ondulante.
b. Ciclo biológico (observe el esquema adjunto)
Relación hospedero-parásito: En el Papanicolaou (examen de células para el
diagnóstico precoz del cáncer uterino), se suele encontrar Trichomonas
vaginalis con células del tipo III, que luego de la eliminación de Trichomonas
vaginalis, dichas células pueden variar a Tipo II o Tipo IV.
Diagnóstico: Mediante la observación, en fresco de la secreción vaginal o
prostática. Se recomienda hacer concomitantemente variar a Tipo II o Tipo IV.
Epidemiología: Es una infección cosmopolita. Entre el 15 y el 30% de mujeres
en periodo de actividad sexual están parasitadas. Ocasionalmente se han
encontrado Infecciones en recién nacidas, o niñas, lo cual indica otros
mecanismos, aparte del sexual, presentes.

PARASITOLOGIA MEDICA Página 17
CICLO DE VIDA DE Trichomonas vaginalis

PARASITOLOGIA MEDICA Página 18
TRIPANOSOMIASIS AMERICANA
Definición:
Zoonosis causada por Trypanosoma cruzi y Trypanosoma rangeli.
La infección por Trypanosoma cruzi es conocida como “Enfermedad de Chagas”.
Ambas parasitosis han sido demostradas en el país y son transmitidas por especies
de triatominos.
El Parásito: Tripanosoma cruzi
a. Morfología
El Trypomastigote: Observe preparaciones de frotis de sangre con
Trypanosoma cruzi. Preste atención al tamaño (compare con el tamaño del
glóbulo rojo), la forma de “c”. Distinga el núcleo central, quinetoplasto posterior,
prominente y subterminal, membrana ondulante y flagelo.
El Amastigote: Observe preparaciones de cortes histológicos de corazón, con
objetivo de inmersión. Preste atención a la presencia de “nidos de amastigotes”
en el interior de las fibras musculares. Distinga el tamaño muy pequeño del
amastigote, la forma redondeada ú ovoide del mismo, la presencia del núcleo y
quinetoplasto y la ausencia de membrana ondulante.
El Epimastigote: Observe preparaciones de cultivos de Trypanosoma cruzi (en
fresco). Preste atención a las “rosetas” de epimastigotes, al movimiento activo
de éstos, y a la pequeña membrana ondulante y flagelo. En las preparaciones
coloreadas, observe el tamaño variable del parásito, la presencia de núcleo,
quinetoplasto, membrana ondulante y flagelo. Repare que el quinetoplasto está
situado siempre próximo al núcleo.
b. Ciclo biológico: (Vea el esquema adjunto)
Relación hospedero-parásito: Observe preparaciones de cortes histológicos
de corazón con infección con Trypanosoma cruzi. Preste atención a los cambios
degenerativos de las fibras musculares parasitadas, y en ocasiones, en las no
parasitadas, así como el infiltrado linfomonocitario cerca y a distancia de los
nidos de amastigotes.

PARASITOLOGIA MEDICA Página 19
Diagnóstico:
a. Examen de sangre: En fresco (recién nacidos con sospecha de transmisión
transplacentaria), frotis y gota gruesa (etapa aguda).
b. Hemocultivo
c. Xenodiagnóstico
d. Biopsia de ganglios y músculo
e. Pruebas inmunobiológicas
(Ver métodos de diagnóstico)
Epidemiología: (Ver mapa de distribución geográfica de la infección en el Perú)
En nuestro país, el cobayo, parece ser el más importante reservorio de la
infección por Trypanosoma cruzi.

PARASITOLOGIA MEDICA Página 20
VECTORES DE LA TRIPANOSOMIASIS AMERICANA: LOS
TRIATOMINOS
Triatominae (Hemíptera – Reduvidae)
Caracteres generales:
a. Morfología:
1. Los adultos: Observe especimenes adultos, preste atención al tamaño,
color y ornamentación del cuerpo; la cabeza prolongada hacia delante
(prognatha); ojos compuestos, ocelos, aparato bucal (picador, chupador) con
tres segmentos cortos y rectos. Antenas filiformes y cortas. Tórax con
pronoto grande y escutellum triangular, un par de hemiélitros y un par de
alas membranosas, patas con uñas. Abdomen con conexivo. Diferencie
hembras de machos por la continuidad del conexivo en el segmento caudal
(macho) o discontinuo (hembra).
2. Los huevos: Observe los huevos, que se caracterizan por ser operculados.
3. Las niñas: Observe ninfas de diferentes estadíos. Diferéncielos de los
adultos (tamaño y ausencia de alas). Distinga los siguientes hemípteros:
hematófagos, entomófagos y fitófagos (Vea esquemas).
b. Ciclo biológico:
Tienen metamorfosis gradual (observe el esquema adjunto).
Clasificación:
Observe especímenes adultos de Triatoma sp., Panstrongylus sp. y Rhodnius sp.
Preste atención en la cabeza, al nivel de la inserción de las antenas. (Estudie el
esquema adjunto).

PARASITOLOGIA MEDICA Página 21
LEISHMANIASIS
Definición:
Infección producida por especies del género Leishmania.
Se reconocen las leishmaniasis cutánea, mucocutánea y visceral. El parásito es
transmitido por mosquitos del género Lutzomyia sp. (América) y Phlebotomus sp.
(Europa, Asia y África). Las leismaniasis cutáneas se caracterizan por lesiones
ulcerativas que por extensión o por metástasis pueden ocasionar lesiones en las
mucosas oronaso-faríngeas. La leishmaniasis visceral ocasiona hepato-
esplenomegalia.
El parásito:
a. Morfología:
1. El amastigote: Observe frotases de lesiones cutáneas y mucocutáneas
coloreadas con Giemsa. Preste atención al tamaño, núcleo y
quinetoplasto.
2. El promastigote: Observe preparaciones en fresco de cultivo de
Leishmania, preste atención al movimiento del parásito, flagelos y
“roestas”. En preparaciones microscópicas coloreadas con Giemsa
observe el núcleo, la posición del quinetoplasto y flagelo. En la misma
preparación trate de ubicar formas en reproducción.
b. Ciclo biológico: (Estudie el esquema adjunto)
Relación hospedero-parásito: Observe cortes histológicos de lesiones
cutáneas, y/o mucocutáneas de leishmaniasis. Preste atención a la
destrucción de los tejidos, la proliferación, linfocitaria, y a la presencia de
amastigotes.
Diagnóstico parasicológico: Frotis y/o biopsia de las lesiones cutáneas o
mucosas (Ver métodos de diagnóstico).
Intradermoreacción de Montenegro: Útil a partir del mes de la infección, y
menos importante son las reacciones sexológicas (ver Métodos
inmunobiológicos).
Epidemiología: (Ver mapa adjunto). Las formas “uta” y “espundia” tienen
zonas de distribución predominantes.

PARASITOLOGIA MEDICA Página 22
CICLO DE VIDA DE Leshmania sp.

PARASITOLOGIA MEDICA Página 23
VECTORES DE LA LEISHMANIASIS: LAS LUTZOMYIAS Y LOS
PHLEBOTOMUS
Lutzomyia sp. (Insecta – Díptera – Nematocera – Psychodidae)
Caracteres generales:
a. Morfología:
Los adultos: En láminas con Lutzomyia sp. Observe el tamaño, color, cuerpo
piloso, cabeza pequeña con un par de ojos grandes compuestos, antenas
similares en ambos sexos, palpos pendulares, probosis gruesa. Tórax corto y
giboso, alas lanceoladas, cubiertas con pelos largos, sin venas transversas. La
extremidad posterior del macho presenta clárperes prominentes en forma de
garfios y en la hembra es roma.
(Vea mapa de distribución del vector en el Perú)

PARASITOLOGIA MEDICA Página 24
TOXOPLASMOSIS
Definición: Es una zoonosis causada por Toxoplasma gondii. Es la más difundida
de las zoonosis parasitarias. La infección en el adulto es usualmente asintomática.
La infección transparentaría es rara, pero puede producir graves alteraciones.
El parásito: Toxoplasma gondii
a. Morfología:
El trofozoito: Observe preparaciones microscópicas de frotices de exudado
peritoneal de ratón, inoculado con Toxoplasma gondii. Preste atención a las
formas intra y extracelulares del parásito. En los trofozoitos extracelulares repare
en la forma de “media luna”, presentando un extremo ensanchado, donde se
encuentra el núcleo. Las formas intracelulares se encuentran aglomeradas en el
citoplasma, en división, variando su forma a fusiforme (taquizoitos).
El quiste: Observe cortes histológicos de cerebro de ratón con quistes de
Toxoplasma gondii. Preste atención al tamaño, forma esférica, la presencia de
gran cantidad de bradizoitos, y la membrana quística.
b. Ciclo biológico:
Relación hospedero-parásito: El parásito es intracelular, la propagación (fase
aguda) se hace por invasión de células vecinas, hay destrucción de tejidos y
reacción inflamatoria periférica. Observe, en la preparación del frotis de exudado
peritoneal, la presencia de células polimorfonucleares y linfocitarias. En la fase
crónica (quistes) hay poca reacción inflamatoria por la evasión del parásito a la
respuesta inmunitaria del hospedero. En la lámina de corte histológico de cerebro,
preste atención a la falta de reacción inflamatoria periquística.
Diagnóstico:
a. Fase aguda: La demostración directa del parásito es difícil lograrse, inclusive
por la inoculación del ratón. Las muestras para examinarse lo constituyen el
L.C.R., la sangre, secreciones, macerado de ganglios, etc.
b. Las reacciones inmunológicas son más útiles en la fase crónica y en las
reactivaciones de las lesiones. (Ver métodos de diagnóstico).
c. En la transmisión transplacentaria, la detección de IgM antitoxoplasma es útil
para el diagnóstico y el seguimiento del tratamiento del niño.

PARASITOLOGIA MEDICA Página 25
Epidemiología:
En nuestro país similar a otros, se señalan tasas altas de infección humana (40-
50%), siendo más elevadas en poblados de nuestra selva y menos en los de
nuestra serranía.

PARASITOLOGIA MEDICA Página 26
CICLO DE VIDA DE Toxoplasma gondii

PARASITOLOGIA MEDICA Página 27
PALUDISMO
Definición:
Infección causada por esporozoarios del género Plasmodium (Plasmodium vivax,
Plasmodium ovale, Plasmodium malariae, Plasmodium falciparum) y que son
transmitidos por insectos anofelinos. La enfermedad se caracteriza por los accesos
palúdicos (escalofríos, fiebre y sudoración) producidos por la destrucción de los
glóbulos rojos que pueden dar lugar a la anemia. Además, Plasmodium falciparum
puede producir la obstrucción de los capilares viscerales y causar la muerte.
El parásito:
a. Morfología:
Ciclo eritrocítico: Observe frotices de sangre, coloreados con Giemsa. Distinga
los glóbulos blancos, de los rojos. El parásito se encuentra en el interior de los
glóbulos rojos. Diferéncielos de una plaqueta adherida al glóbulo. El citoplasma
del parásito se colorea de azul y su núcleo de rojo. En la misma lámina.
Compruebe, si el glóbulo rojo parasitazo es más grande que los no parasitazos
(P. vivax, P. ovale) ó es el de tamaño igual o menor (Plasmodium malariae,
Plasmodium falciparum). Precise, si el parásito tiene un solo núcleo (Trofozoito,
gametocito) o tiene más de dos núcleos (esquizonte). Identifique, si en los
glóbulos observados existe una sola especie de Plasmodium o más de una
(infección mixta). Ponga atención al pigmento malárico y a las granulaciones del
eritrocito, guiándose por el dibujo adjunto, señale el estadío y la especie de
Plasmodium que observa.
b. Ciclo biológico: (Estudie el esquema adjunto)
Relación hospedero-parásito:
a. Glóbulos rojos: Observe las alteraciones de forma y tamaño de los glóbulos
rojos parasitazos y no parasitazos.
b. Hígado y bazo: Observe en el corte histológico de hígado la presencia de
pigmento malárico en el interior de las células de Kupfner. Observe en el
corte histológico de bazo, la presencia de pigmento malárico en las células
mononucleares fagocitarias.Diagnóstico parasitológico: Usualmente se
realiza por el hallazgo del parásito en la sangre periférica frotis y gota
gruesa. (Vea métodos de diagnóstico de las hemohistoparasitosis).

PARASITOLOGIA MEDICA Página 28
La demostración de anticuerpos antiplasmodium (excluyendo la transferencia activa
y pasiva) puede ser útil para demostrar la presencia actual y/o pasada del parásito.

PARASITOLOGIA MEDICA Página 29
VECTORES DEL PALUDISMO: LOS ANOFELINOS
Anopheles sp. (Insecta – Díptera – Nematocera-Culicidae)
Caracteres generales:
a. Morfología:
1. Los adultos: Anopheles (anophelin): Examine especimenes vivos. Preste
atención a la pigmentación de las alas, y a la posición que adoptan durante
el reposo. (Vea el esquema adjunto). Observe el cuerpo esbelto. En la
cabeza note que los palpos tienen el mismo tamaño que la proboscis. En
preparaciones en lámina, distinga las características morfológicas de las
antenas en los machos (“plumoso”), y además, el último segmento de los
palpos es dilatado, en los machos.
2. Los huevos: Observe las cámaras de aire laterales.
3. Las larvas: Observe los estigmas respiratorios posteriores. Preste atención
a los pelos palmeados.
4. Las pupas: En especimenes vivos, observe la forma (coma o signo de
interrogación); y el movimiento hacia la superficie del agua.
b. Ciclo biológico: El insecto metamorfosis completa (Estudie el esquema
adjunto).

PARASITOLOGIA MEDICA Página 30
TENIASIS Y CISTICERCOSIS
Teniasis
Definición.- Es la infección del intestino delgado del hombre por los adultos de los
céstodos. Los más importantes son Taenia solium, Taenia saginata,
Diphyllobothrium pacificum, Hymenolepis nana, Hymenolepis diminuta y Dipylidium
caninum.
El parásito. Taenia solium, Taenia saginata.
a. Morfología:
Los adultos: Observe escólices de Taenia solium, Taenia saginata, montados en
láminas portaobjetos. Preste atención a la presencia de las 4 ventosas en ambas
especies, rostelo provisto de ganchos en Taenia solium y su ausencia en Taenia
saginata.
Observe proglótidos grávidos de ambas especies. Preste atención a las
ramificaciones uterinas. Cuente las ramificaciones primarias. Repare que Taenia
solium tiene como máximo 12, y Taenia saginata, más de 12.
Los huevos.- Observe preparaciones microscópicas de heces humanas con
huevos de Taenia sp. Repare en la forma redondeada, embrióforo y embrión
hexacanto. No se establece la diferencia de especie por la morfología de los
huevos.
El cisticerco.- Observe trozos de músculo de cerdo con Cisticercos cellulosae.
Preste atención al tamaño macroscópico, a su color blanquecino y a la forma
ovoidea.
Diseque los cisticercos, y observe, por transparencia la presencia de la “mancha
blanca”, correspondiente al escólex invaginado.
Observe cisticercos tratados con bilis. Preste atención al evaginamiento del
escólex. Repare en el movimiento de las ventosas, y al rostelo con ganchos.
Observe cortes histológicos de tejido muscular de cerdo con cisticercos. Preste
atención a la pared del cisticerco, y al escólex invaginado.
b. Ciclo biológico: (Estudie el esquema adjunto).
Relación hospedero-parásito: La Taenia solium, Taenia saginata se fijan por su
escólex a la mucosa y el cuerpo está en la luz del intestino. No se han
demostrado alteraciones en la mucosa.

PARASITOLOGIA MEDICA Página 31
Cisticercosis humana
Definición.- Es la infección causada por los cisticercos de Taenia solium.
Diagnóstico: La teniasis se diagnostican por el hallazgo de huevos y/o proglótidos
en las heces (Vea métodos de diagnóstico).
La cisticercosis humana se diagnostica por medio de la biopsia (cisticercosis
subcutánea), examen de fondo de ojo (cisticercosis ocular), o por reacciones
inmunológicas de sangre y líquido céfalo-raquídeo (Ver métodos de diagnóstico).
Epidemiología.- La cisticercosis es una de las zoonosis más importantes en
nuestro país. La cisticercosis humana del sistema nervioso es frecuente como causa
de morbilidad y mortalidad en los servicios de neurología.
CICLO BIOLÓGICO DE Taenia solium – Taenia saginata

PARASITOLOGIA MEDICA Página 32
Diphyllobothrium pacificum
a. Morfología:
1. Los adultos: Pueden alcanzar hasta 2 metros de longitud: Observe el escólex
acorazonado con dos botrias (dorsal y ventral). Observe proglótidos a menos
aumento. Preste atención a la presencia de las aberturas genital y uterina en
la cara ventral y anteriormente a ellas, unas rugosidades o repliegues. Preste
atención a las asas uterinas y la presencia de huevos en el interior de las
mismas. Los testículos son numerosos y se sitúan en los campos laterales del
proglótido.
2. Los huevos: Observe en preparaciones microscópicas, el grosor de la
cáscara, la presencia de un engrosamiento en el polo opuesto al opérculo.
Dibuje.
3. Las larvas: (Vea el ciclo biológico).
b. Ciclo biológico
(Vea el esquema adjunto)
Los adultos parasitan a los lobos marinos (Otaria byronia, Arctocephalus
australis, etc.) que son los hospederos definitivos naturales.
El ciclo biológico se desarrolla en el ecosistema marino e incluye a 2 hospederos
intermediarios: el primero, en un copépodo aún no conocido, en el que se
desarrolla el procercoide. En el ciclo de este parásito también intervienen los
hospederos paratémicos o de transporte. En el Perú se han encontrado varios
peces comerciales infectados con plerocercoides de Diphyllobothrium pacificum.
El hombre se infecta al ingerir peces marinos insuficientemente cocidos, bajo la
forma de “cebiche”.
Relación hospedero-parásito: El parásito generalmente no causa molestias.

PARASITOLOGIA MEDICA Página 33
Hymenolepis diminuta
a. Morfología:
1. Los adultos.- Pueden medir 1 metro de longitud. Observe el escólex
provisto de 4 ventosas. A menor aumento observe proglótido maduro posee
3 testículos reconocibles. Los proglótido grávidos están ocupados totalmente
por el útero sacciforme lleno de huevos. Preste atención a las aberturas
genitales, las que se abren a un solo lado del estróbilo.
b. Vectores:
Tribolium sp.: (Insecta-Coleoptera)
En los Tribolium sp., que se le ha proporcionado identifique los caracteres de los
coleópteros como son los 2 pares de alas, el primer par de consistencia coriácea
(élitros) que no sobrepasan la línea media del cuerpo y el segundo par membranoso
doblado debajo de los élitros, preste atención al aparato bucal de tipo masticador.
2. Los huevos: Esféricos con un embrión hexacanto. Dibuje y compare con la
morfología de los huevos de las otras tenias, principalmente Hymenolepis
nana.
b. Ciclo biológico:
(Estudie el esquema adjunto). El hospedero intermediario es un artrópodo,
comúnmente gorgojos de los cereales como Tribolium confusum; en el Perú se
han descrito otros artrópodos.
Relación hospedero-parásito: Las infecciones humanas son raras, sin embargo,
en Cajamarca se ha observado una importante prevalencia del parasitismo.

PARASITOLOGIA MEDICA Página 34
CICLO BIOLÓGICO DE Hymenolepis diminuta

PARASITOLOGIA MEDICA Página 35
Hymenolepis nana
a. Morfología:
1. Los adultos: Son pequeños, pueden medir hasta 10 cm. De longitud.
Observe el escólex provisto de 4 ventosas y un rostelo retráctil armado de
ganchos. Compruebe que los proglótidos son más pequeños que
Hymenolepis diminuta pero con morfología similar.
2. Las larvas: Observe el cisticercoide en la preparación microscópica de las
vellosidades intestinales. Dibuje.
3. Los huevos: Observe que el embrióforo que encierra al embrión hexacanto
tiene una forma de “limón” con un engrosamiento en cada polo, de donde
emergen filamentos polares que se sitúan en el espacio comprendido entre el
embrióforo y la cubierta externa. Dibuje y compare con los huevos de
Hymenolepis diminuta.
b. Ciclo biológico:
(Estudie el esquema adjunto). El hospedero definitivo, natural, es el hombre,
aunque una raza llamada Hymenolepis nana var. fraterna se desarrolla en los
ratones. Hymenolepis nana no requiere del hospedero intermediario.
Relación hospedero-parásito: La presencia del cisticercoide en las vellosidades
intestinales induce reacciones inflamatorias de la mucosa intestinal (enteritis) que
pueden ser severas. En la preparación microscópica de las vellosidades intestinales
observe los infiltrados celulares próximos al parásito.

PARASITOLOGIA MEDICA Página 36
CICLO BIOLÓGICO DE Hymenolepis nana

PARASITOLOGIA MEDICA Página 37
Dipylidium caninum
a. Morfología:
1. Los adultos: Pueden llegar a medir hasta 80 cm. de longitud. Observe el
escólex con 4 ventosas y rostelo retráctil y armado de numerosos ganchos
que tienen la forma de espinas de rosal. Preste atención a la forma de “barril”
o “pepitas de zapallo” de los proglótidos. Los proglótidos maduros tienen
doble juego de aparatos reproductores: masculino y femenino. Los proglótidos
grávidos presentan cápsulas ovígeras, dentro de las cuales se hallan los
huevos.
2. Los huevos: Compruebe que los huevos conteniendo los embriones
hexacantos se translucen dentro de las cápsulas ovígeras.
3. Las larvas: Observe y dibuje el cisticercoide de contenido en una pulga.
b. Ciclo biológico:
(Estudie el esquema adjunto). Las pulgas se infectan cuando están en el estadío
larvario. El hombre es un hospedero definitivo accidental. Los niños se infectan
por su contacto con perros o gatos infectados.
Relación hospedero-parásito.- La infección por Dipylidium caninum, generalmente
pasa desapercibida.

PARASITOLOGIA MEDICA Página 38

PARASITOLOGIA MEDICA Página 39
ASCARIASIS
Definición.- Geohelmintiasis causada por Ascaris lumbricoides. Los adultos tienen
por hábitat la luz del intestino delgado del hombre. El parasitismo está difundido en
todo el país, siendo las regiones de la Sierra y la Selva las que presentan las más
altas prevalencias.
El Parásito:
a. Morfología:
1. Los adultos: Observe la morfología externa de ejemplares masculinos y
femeninos. Preste atención al tamaño, grosor y extremidad posterior (macho:
encorvada, hembra: recta y crónica). En la extremidad anterior, haga un corte
transversal, con ayuda de una hoja de afeitar y observe los tres labios de
parásito al microscopio.
Diseque, guiándose por el dibujo adjunto, un ejemplar hembra. Haga un corte
transversal de la porción distal del útero, y obsérvelo al microscopio, entre
lámina y laminilla: preste atención a la morfología de los huevos.
Observe las preparaciones microscópicas con cortes transversales del
parásito: reconozca los elementos de la estructura interna del parásito.
Guíese por el dibujo adjunto.
2. Los huevos: Establezca las semejanzas y diferencias de los siguientes
huevos: los observados en el útero, los incubados en el medio ambiente. Los
emitidos con las heces, los fértiles, los infértiles y los decorticados. Guíese por
el dibujo adjunto.
3. Las larvas: Observe y dibuje huevos larvados. Observe y dibuje cortes
transversales y/o longitudinales de larvas en la luz bronquial de preparaciones
microscópicas de pulmones de ratones experimentalmente infectados (Ciclo
de Loos).
Relación hospedero-parásito: Los adultos tienen poca interrelación morfológica
con el hospedero, excepto si ellos migran a los conductos pancreático, biliar y/o a
otras localizaciones extraintestinales.

PARASITOLOGIA MEDICA Página 40
Las larvas pueden ocasionar cambio titulares importantes. Observe en las
preparaciones microscópicas de pulmón, además de la localización de las larvas, las
hemorragias, las zonas de condensación y las reacciones inflamatorias próximas a
las larvas, así como la presencia de eosinófilos.
CICLO DE VIDA DE Ascaris lumbricoides

PARASITOLOGIA MEDICA Página 41
OXYURUS
Definición.- Es la infección causada por Enterobius vermicularis (=Oxyuris
vermicularis). El adulto se localiza en el intestino grueso: la hembra migra colocando
sus huevos en la margen del ano.
El parásito: Enterobius vermicularis
a. Morfología:
Los adultos.- Observe ejemplares hembras. Preste atención al color blanco
nacarado y a la cola larga y terminada en punta. Observe preparaciones de
hembras en láminas portaobjeto. Preste atención a la presencia de las aletas
cefálicas. Distinga el bulbo esofágico y la presencia de huevos ocupando casi todo
el cuerpo.
Los huevos.- Observe preparaciones microscópicas conteniendo huevos de
Enterobius vermicularis. Preste atención a la forma plano convexa, y a la
presencia de la larva en su interior.
b. Ciclo biológico: (Ver esquema adjunto)
Relación hospedero-parásito: Observe preparaciones microscópicas con cortes
transversales de apéndice. Distinga el parásito, identificando los cortes transversales
del mismo a diferentes alturas del cuerpo, en algunos de ellos, se observa al útero
con huevos. En todos los cortes transversales reconozca las aletas laterales (útil en
el diagnóstico del parásito).

PARASITOLOGIA MEDICA Página 42

PARASITOLOGIA MEDICA Página 43
TRICHURIASIS
Definición.- Es una goehelmintiasis causada por Trichuris trichiura (Trichocephalus
dispar). Los adultos se insertan en la mucosa del intestino grueso del hombre.
El parásito: Trichuris trichiura (Trichocephalus dispar)
a. Morfología:
Los Adultos: Observe ejemplares adultos. Preste atención a la porción anterior
delgada, y a la posterior gruesa (forma de látigo). Distinga la parte distal
(enrollada) del macho, de la terminación recta en la hembra. Calcule el tamaño
en ambos sexos. Observe preparaciones en lámina portaobjeto de ejemplares
adultos. Distinga el esófago (esticocitos) en la porción delgada anterior. En las
hembras, repare la presencia de la vulva en la unión de las porciones gruesa y
delgada. En los machos, observe en su extremidad posterior la presencia de la
espícula con su vaina espinosa.
Los huevos: Observe preparaciones de heces, en fresco, teñidas con lugol.
Preste atención a las características morfológicas, guiándose por el esquema
adjunto.
b. Ciclo biológico: (Ver esquema adjunto)
Relación hospedero-parásito: Observe preparaciones histológicas de corte de
intestino grueso parasitazo con adultos de Trichuris trichiura. Preste atención a la
presencia de la porción delgada del parásito en la mucosa del intestino, y la porción
gruesa en la luz intestinal.
HUEVO FECUNDO

PARASITOLOGIA MEDICA Página 44
CICLO DE VIDA DE Trichuris trichiura

PARASITOLOGIA MEDICA Página 45
UNCINARIASIS
Definición.- Geohelmintiasis causada por los nematodes Ancylostoma duodenale
y/o Necator americanus, también se considera al Ancylostoma braziliensis, no
señalado para nuestro país.
Los adultos se fijan en la mucosa del intestino delgado, produciendo micro
hemorragias, que en algunos casos llevan a la anemia. Frecuente en la región de
nuestra Selva.
El parásito:
a. Morfología:
1. Los adultos: Observe en el Ancylostoma duodenale y/o Necator americanus
las cápsulas bucales. Preste atención a la presencia de dientes ventrales en
el primero y de placas cortantes en el segundo.
2. Los huevos: Observe y dibuje huevos: preste atención a que son
segmentados.
3. Las larvas: Observe larvas filariformes (forma infectante) vivas, al
microscopio. Preste atención a la movilidad y a las envolturas.
b. Ciclo biológico: Estudie el mismo en el esquema adjunto.
Relación hospedero-parásito: En la piel (puerta de entrada) se producen lesione
inflamatorias, debido al ingreso de la forma infectante y a la respuesta del hospedero
observe en los cortes histológicos de piel de ratón experimentalmente infectado,
dichas lesiones.
Las lesiones provocadas en el hospedero son consecuencia de la destrucción
mecánica y lisis tisular por la inserción del parásito adulto en las vellosidades
intestinales, así como la hemorragia consiguiente. La anemia, en casos severos de
la infección es microcítica hipocrómica por la pérdida de hierro.

PARASITOLOGIA MEDICA Página 46
STRONGYLOIDIASIS
Definición.- Infección causada por el nematodo Strongyloides stercoralis.
Esencialmente es una geohelmintiasis, pero existen casos de auto infección. El
adulto se localiza en las vellosidades del intestino delgado. Frecuente en la región
de la Selva, pero no ausente en la Costa y Sierra.
El parásito:
a. Morfología:
1. Los adultos: La hembra parásita es pequeña, filiforme, mide
aproximadamente 2 mm. de longitud y difícilmente de observarse a simple
vista.
2. Las larvas: Larva rabditoide: cavidad bucal corta comparando con el grosor
del parásito, esófago con bulbo posterior notorio (Compare con larvas de
uncinarias, vea los dibujos).
Larva filariforme: forma infectante, con esófago filariforme (Compare con
larvas de uncinarias, vea los dibujos).
b. Ciclo biológico: Estudie el esquema adjunto.
Relación hospedero-parásito: En la fase de invasión cutánea, se puede distinguir
una erupción pápulo-eritomatosa ocasionada como respuesta de sensibilización en
la zona de penetración de la larva filariforme.
Durante su migración, las larvas ocasionan lesiones infiltrativas en pulmones (ciclo
de Los).
La localización de los adultos en las vellosidades intestinales produce inflamación de
la mucosa intestinal y puede producir el síndrome de mala absorción.

PARASITOLOGIA MEDICA Página 47
CICLO DE VIDA DE Strongyloides stercoralis

PARASITOLOGIA MEDICA Página 48
FASCIOLASIS
Definición.- Zoonosis ocasionada por el trematodo Fasciola hepatica. El adulto se
localiza en las vías biliares intra y extra hepáticas.
El parásito: Fasciola hepatica
a. Morfología:
Los adultos: Observe vísceras parasitadas con adultos de Fasciola hepatica. De
las vías biliares extraiga ejemplares adultos. Preste atención a la forma, color y
tamaño. Con ayuda de lupa trate de identificar las ventosas. Coloque un ejemplar
entre dos láminas portaobjetos y mírelo a través de la luz, trate de identificar las
ramificaciones del intestino y al útero lleno de huevos. Guiándose con el
esquema adjunto, identifique los órganos de la estructura interna del parásito.
Los huevos: Con ayuda de un mondadiente, raspe la superficie de las vías
biliares y haga una preparación directa, con suero fisiológico, en una lámina
portaobjeto, y cúbrala con una laminilla. Observe el tamaño del huevo (el huevo
más grande de los helmintos estudiados), el color, la forma, la superficie externa,
la presencia de opérculo en uno de los extremos.
Los miracidios: Observe huevos con miracidio en el interior de los mismos.
Puede observar la eclosión del miracidio. Preste atención al desplazamiento
veloz, movimiento de los cilios, mancha ocular y papila apical. En las láminas
coloreadas de miracidios, corrobore las características morfológicas señaladas.
Las metacercarias: Observe preparaciones microscópicas de metacercarias.
Preste atención a la forma, y a la cubierta de la larva.
b. Ciclo biológico: (Vea el esquema adjunto)
El hospedero intermediario: Observe conchillas de Lymnaea sp.
Relación hospedera-parásito: Observe cortes histológicos de hígado parasitazo
con formas juveniles de Fasciola hepatica. Preste atención a la destrucción celular,
hemorragia e infiltración inflamatoria aguda, alrededor del parásito, con presencia de
eosinófilos.
Observe el corte histológico del hígado parasitado con ejemplares adultos, en
canales biliares de Fasciola hepatica, preste atención a las alteraciones de la

PARASITOLOGIA MEDICA Página 49
mucosa (metaplasma), a la fibrosis pericanalicular y al exudado inflamatorio.
Reconozca al parásito.
Atención a la presencia de espinas en la superficie.
Diseque los canales biliares del hígado parasitazo y preste atención a la presencia
de formaciones calcáreas.
Diagnóstico
a. Fase aguda: Pruebas inmunobiológicas, es importante la inmunoelectroforesis.
Identifique el arco II en la lámina de inmunoelectroforesis.
b. Fase crónica: Hallazgo de huevos en heces, por la técnica de la sedimentación
rápida. En ocasiones se aconseja el tubaje duodenal.
Epidemiología: El parasitismo está ampliamente distribuido en el país. Los valles
interandinos parecen presentar más alta prevalencia de infección animal y humana.
CICLO DE VIDA DE Fasciola hepatica

PARASITOLOGIA MEDICA Página 50

PARASITOLOGIA MEDICA Página 51
PARAGONIMIASIS
Definición.- Infección causada por especies del trematodo Paragonimus mexicanus.
Generalmente el adulto se localiza en los pulmones, pero puede tener otras
localizaciones como el cerebro.
El parásito: Paragonimus mexicanus
a. Morfología:
Los adultos: Observe preparaciones de adultos de Paragonimus mexicanus,
montadas en láminas portaobjetos. Preste atención a las formas ovoide o
fusiforme del cuerpo. Distinga con lupa, o a menor aumento, las ventosas oral y
ventral, las dos ramas intestinales laterales zigzagueantes, no ramificadas,
testículos y ovarios ramificados. Repare que en el lado opuesto del ovario se
encuentra el útero lleno de huevos. Intente reconocer espinas en la superficie del
cuerpo.
Los huevos: Observe huevos de Paragonimus mexicanus en preparaciones de
heces de gato. Ponga atención a la asimetría de los huevos, a su superficie
ondulada y a la presencia de opérculo.
Las metacercarias: Observe metacercarias de Paragonimus mexicanus,
montadas en láminas portaobjeto y coloreadas. Repare en la ausencia de
membrana quística, la forma alargada del cuerpo, tamaño macroscópico,
presencia de ventosas, ponga atención a la ausencia de órganos genitales y a la
presencia de las ramas intestinales.
b. Ciclo biológico: (Ver el esquema adjunto)
El primer hospedero de Paragonimus mexicanus es un caracol Aroapyrgus sp.,
cuya especie aún no ha sido determinada para el Perú.
El segundo hospedero de Paragonimus mexicanus en el país es el cangrejo de
agua dulce Hypolobocera chilensis elgenmanni (=Pseudothelphusa chilensis).
Observe ejemplares de cangrejos colectados del valle de Condabamba
(Cajamarca).
Los reservorios naturales descritos, hasta ahora, en el Perú son: la “zarigueya” o
“muca” (Didelphys spp.), gato.
Relación hospedero-parásito: Observe preparaciones microscópicas de corte de
pulmón con el parásito adulto. Preste atención a la localización del adulto en el tejido

PARASITOLOGIA MEDICA Página 52
pulmonar y su relación con las vías aéreas. Distinga la membrana quística rodeando
al adulto. Observe preparaciones microscópicas de corte de pulmón con huevos de
Paragonimus mexicanus. Preste atención a la presencia de la cáscara (membrana
ondulante), a la gran infiltración celular (granuloma) con presencia de células
linfomonocitarias, eosinófilos, etc.
Diagnóstico:
a. Búsqueda de huevos en el esputo y/o heces (Ver métodos de diagnóstico)
b. Pruebas inmunobiológicas: intradermoreacción y fijación del complemento (Ver
métodos de diagnóstico).
Epidemiología: En nuestro país, la infección humana, en las zonas endémicas
(Departamentos de Cajamarca, La Libertad, Ucayali) se debería, a la inglesa de
cangrejos insuficientemente cocidos.
PARAGONIMIASIS HUMANA EN EL PERÚ

PARASITOLOGIA MEDICA Página 53
CICLO BIOLÓGICO DE Paragonimus mexicanus

PARASITOLOGIA MEDICA Página 54
HIDATIDOSIS
Definición.- Presencia del estadío larval en las vísceras de los animales
susceptibles. El estadío adulto es la tenia del perro (Echinococcus granulosus). En
otros países se han encontrado casos humanos de hidatidosis por Echinococcus
vogeli (América), Echinococcus multilocularis (Alaska, Europa).
El parásito: Echinococcus granulosus
a. Morfología:
Los adultos: Observe al microscopio las láminas coloreadas de Echinococcus
granulosus. Fije su atención en el tamaño, en el escólex con ventosas y ganchos,
y el número de proglótidos. En el proglótido maduro trate de ubicar los testículos,
y la bolsa del cirro. En el proglótido grávido, observe los cambios producidos y el
desarrollo del útero sacular lleno de huevos.
Las larvas: (Quiste hidatídico). Observe las vísceras parasitadas. Preste atención
a los cambios morfológicos ocasionados por el crecimiento del quiste. Trate de
determinar si es un quiste único o múltiple. Usando una jeringa con su aguja,
haga la punción del quiste y extraiga el líquido. Viértalo en tubos de centrífuga
ponga atención a sus características. Deje sedimentar el líquido y observe los
ganchos, las ventosas y corpúsculos calcáreos de los mismos. Observe en la
“arenilla hidatídica” protoescolises invaginados. Abra un quiste que ha sido
evacuado y separe la cutícula. Preste atención a la facilidad de su
desprendimiento, al color blanco (clara de huevo cocido) y a la elasticidad de la
misma.
b. Ciclo biológico: (Observe el esquema adjunto)
Relación hospedero-parásito: Observe al microscopio, los cortes histológicos de
quiste hidatídico, e identifique la capa adventicia, resultante de la acción mecánica
del parásito y de la respuesta del hospedero. Preste atención a las membranas del
parásito: a) cunicular, cuya estructura es patognominica (anhista), b) germinativa,
capa nucleada sincitial que produce la capa cuticular, los protoescólices y el líquido
hidatídico.

PARASITOLOGIA MEDICA Página 55
Diagnóstico: Es infrecuente el diagnóstico directo (protoescólices y membranas en
la vómica), más frecuentemente se emplean los métodos indirectos. De ellos, el más
importante es la inmunoelectroferesis. En la lámina de inmunoelectroforesis
identifique que el Arco V. Una variación es la doble difución usando suero positivo al
Arco V como control (DD5).
Epidemiología: En el Perú, los departamentos de Junín y Puno, y áreas aledañas a
los mismos, son los que presentan los más altos índices de hidatidosis.

PARASITOLOGIA MEDICA Página 56

PARASITOLOGIA MEDICA Página 57
ACARINA I
Sarcoptes spp.
Tyrophagus sp.
Glycyphagus sp.
Dermatophagoides sp.
Sarcoptes scabiei var. hominis., otros
Son ácaros microscópicos que respiran por ósmosis. En preparaciones, observe los
estadíos evolutivos de Sarcoptes spp. Podrá diferenciar las larvas hexápodas, ninfas
octópodas y éstas de los adultos. Los machos presentan en el tercer par de patas,
una cerda larga, en la hembra, el tercer y cuarto par de patas terminan en cerdas.
Moviendo ligeramente el micrométrico del microscopio, apreciará fácilmente las
estructuras dorsales como escamas, pelos modificados y espinas (Ver esquemas).
Tyrophagus sp. y Glycyphagus sp.
Son ácaros que se encuentran contaminando los alimentos, y son productores de
dermatitis de contacto.
En preparaciones de adultos de Tyrophagus sp., en lámina, observe fácilmente, el
cuerpo ovalado, cubierto de escasos pelos largos. Dorsalmente se aprecia una línea
sutural.
En preparaciones de adultos de Glycyphagus sp, observe que el cuerpo está
cubierto de abundantes pelos largos, barbulados y tarsos de los cuatro pares de
patas delgadas y largas (Ver esquema).
Dermatophagoides sp.
Es el ácaro que se encuentra formando parte del polvo doméstico, de las
habitaciones, y es uno de los agentes etiológicos del asma bronquial, y otros tipos
de alergias. Note que su cuerpo está cubierto por una fina cutícula estriada y con
escasos pelos en su superficie (ver esquema).

PARASITOLOGIA MEDICA Página 58
Trombicula sp., Demodex folliculorum. (Acarina – Prostigmata)
Estos ácaros se caracterizan, porque tienen los estigmas respiratorios ubicados en
la porción anterior del cuerpo o base del gnatosoma.
Demodex folliculorum
En las preparaciones, observe los estadíos evolutivos de Demodex folliculorum,
podrá apreciar huevos, larvas hexápodas, ninfas octópodas y adultos, que presentan
la parte terminal del cuerpo fuertemente estriado y los 4 pares de patas sumamente
cortas, formados por 3 segmentos.
En las preparaciones de cortes histológicos de piel, observe el número variado de
especimenes que se encuentran contaminando los folículos pilosos o sebáceos.
Trombicula sp. (“I sangre”)
Sólo el estadío larval es patógeno para el hombre y algunos animales.
En las preparaciones en lámina, observe la larva haxápoda, dorsalmente lleva un
escudo pequeño del que parten un par de cerdas largas barbuladas, asimismo,
podemos apreciar el cuerpo cubierto totalmente por abundantes pelos barbulados.
Fíjese en el aparato bucal, donde se aprecian los quelíceros es iliformes.
La picadura produce prurito intenso en zonas de la piel, donde usualmente está mas
ajustada la vestimenta, también hay enrojecimiento (“chapetonada”) (Ver esquema).
TROMBÍCULA

PARASITOLOGIA MEDICA Página 59
ACARINA II
Ixodes sp., Boophilus sp. y Rhipicephalus sanguineus. Ixodidae “garrapatas
duras”.
Argas sp., Ornithodorus sp. y Otobius sp. (Mesostigmata – Argasidae
“garrapatas blandas”.
Estas garrapatas están incluidas en el suborden Metastigmata porque presentan
estigmas respiratorios localizados en la base del III y IV par de patas, protegidos por
una placa quitinosa.
Observe que los adultos de Ixodes sp., Boophilus sp. y Rhipicephalus sanguineus
“garrapatas duras” tienen el capítulo terminal, escudo dorsal que cubre totalmente el
cuerpo del macho y en las hembras sólo parcialmente, motivo por el cual alcanzan
un tamaño descomunal después de la ingesta de sangre.
Con ayuda de una lupa observe que Ixodes sp. presenta el capítulo muy visible,
carecen de ojos y festones en el borde del cuerpo, las coxas con espinas; en
Boophilus sp. preste atención a los palpos que son cortos y comprimidos, poseen
ojos; la coxa III redondeada; base del capítulo hexagonal; en Rhipicephalus
sanguineus los palpos cortos, con la base del capítulo hexagonal, presentan ojos y
festones; la coxa I es bífida.
En los adultos de Argas sp., Ornithodorus sp. y Otobius sp. “garrapatas blandas”,
observe la posición del capítulo ventral o subventral y la ausencia de escudo dorsal.
Con ayuda de una lupa observe en Argas sp. que el cuerpo es muy aplanado, con
estrías radiales o placas cuadrangulares; una línea sutural bien definida que separa
las superficies dorsal y ventral.
En Ornithodorus sp. observe que el capítulo es subterminal con el hipostoma con
dientes muy desarrollados, el cuerpo cubierto por una serie de granulaciones y el
lado dorsal de las patas son festonadas. Al hacer la observación de Otobius sp.
encontrará una gran semejanza con Ornithodorus sp por las granulaciones del
tegumento que al estadío ninfal está cubierto de espinas, ponga atención al
hipostoma poco desarrollado en el adulto.

PARASITOLOGIA MEDICA Página 60
Importancia Médica: Son vectores biológicos.
Ixodes sp.: Rickettsia rickettsii (fiebre manchada)
Coxiella burnetii (fiebre Q)
Boophilus sp.: Babesiosis sp. y Anaplasmosis sp.
Rhipicephalus sanguineus: Rickettsia conorii (fiebre bitonosa)
Borrelia recurrentis (fiebre recurrente)
Francisella tularensis (Tularemia)
Argas sp.: Virosis, heridas dolorosas.
CICLO BIOLÓGICO DE Boophilus sp.

PARASITOLOGIA MEDICA Página 61
ARÁCNIDOS
(Arácnida – Araneida)
- Latrodectus mactans.
- Loxosceles laeta.
En los especimenes adultos de Latrodectus mactans (“viuda negra”) y Loxosceles
laeta (“araña casera”) que se les presenta, observe las siguientes características:
sexo, palpos dilatados en el extremo distal (machos), palpos delgados (hembra).
Queliceros quitinosos terminados en uña. Establezca diferencias entre ambos
géneros, observando los adultos y las ootecas según las características señaladas
en el cuadro adjunto.
Latrodectus mactans Loxosceles laeta
Color del cuerpo
Negro aterciopelado, brillante, con una mancha rojiza en forma de un reloj de arena, en la parte inferior del abdomen.
Pardo, o marrón claro, siendo más oscuro el céfalo-tórax.
Nº de Ojos
Son 8, dispuestos en 2 filas, pareados, en la parte anterior del céfalo-tórax.
Son 6 pareados y dispuestos en forma triangular, en la parte anterior del céfalo-tórax.
Ooteca
Esferoidales de consistencia papiracea.
Plano convexos.
En preparaciones de estadíos ninfales de Latrodectus mactans y Loxosceles laeta,
en láminas portaobjeto, corrobore las características de los ojos de los adultos.
Ciclo biológico: Metamorfosis gradual.
Importancia Médica: Observe las lesiones producidas en animales de
experimentación, con la inoculación del veneno de Loxosceles laeta. Preste atención
a los cambios de color de la piel (“Mancha livedoide”), edema, necrosis.

PARASITOLOGIA MEDICA Página 62
- Hadruroides lunatus (Aracnida – Scorpionida)
En el alacrán adulto que se le ha proporcionado, note la división del cuerpo en
céfalo-tórax, abdomen y post-abdomen terminado en una dilatación provista de
aguijón en forma de uña que aloja las glándulas venenosas.
Observe la parte anterior del céfalo-tórax, donde se insertan un par de quilíferos
cortos y un par de pedipalpos muy desarrollados terminados en tenazas.
Dorsalmente se encuentra 2 grupos de ojos, 4 laterales y 2 centrales.
En la casa ventral del abdomen observe la presencia de un par de peines situados
lateralmente.
En preparaciones de ninfas de Hadruroides lunatus observe las mismas
características señaladas para el adulto.
Ciclo biológico: Metamorfosis gradual.
Importancia Médica: La inoculación del veneno de los alacranes es un accidente
que produce, generalmente, reacciones locales moderadas (edema, dolor, rubor,
etc., y raramente manifestaciones generales).
Latrodectus mactans
Loxosceles laeta
Hadruroides lunatus

PARASITOLOGIA MEDICA Página 63
PULGAS DE IMPORTANCIA MÉDICA
(Siphonaptera – Pulicidae)
Pulex irritans; Xenopsylla cheopis; Ctenocephalides canis; Ctenocephalides
felis y Tunga penetrans.
Características Morfológicas:
Los adultos: Observe preparaciones de adultos de Pulex irritans; Xenopsylla
cheopis; Ctenocephalides canis; Ctenocephalides felis y Tunga penetrans,
guiándose por los dibujos adjuntos, preste atención a las siguientes características.
En la cabeza, a los ojos simples, antenas cortas en el surco antenario, aparato bucal
picador chupador. En el tórax, ausencia de alas, segmentos del tórax “telescopados”,
y el tercer par de patas muy desarrollado. En el abdomen: el pigidium, los claspers
en el macho y espermateca en la hembra. Por transparencia, intente ubicar el
proventrículo. Para la diferenciación de las especies mencionadas, guíese por el
esquema adjunto.
Las larvas: Observe preparaciones con larvas de pulga. Preste atención a la forma
(vermiformes), carecen de patas, cerdas en todos los segmentos del cuerpo,
dirigidas hacia atrás siendo más abundantes en el último segmento.
Ciclo biológico: Metamorfosis completa (Vea el esquema adjunto), desarrollo
holometábolo.
Importancia Médica:
a. Dermatitis por las picaduras, produciendo reacción de la piel, la especie
importante para el hombre es Pulex irritans.
b. Hospedero intermediario de Dipylidium caninum, la infección, la adquiere la
pulga, al estadío larvario.
c. Vector biológico de Yersinia pestis, Salmonella typhimurium, Rickettsia maurer.
d. Tunga penetrans, produce la tunglasis, (“pique”) por la introducción de la hembra
en la piel.

PARASITOLOGIA MEDICA Página 64
CLAVE DE IDENTIFICACION DE PULGAS PARA LA PRÁCTICA
P U L G A S
SIN
CTENIDIO
CON
CTENIDIO
Longitud de la
cabeza inferior
al doble de la
altura. Diente I
genal mas corto
que diente II
Longitud de la
cabeza igual al
doble de la
altura. Diente I
genal casi igual
longitud diente
II
CABEZA
ANGULAR
CABEZA
REDONDEAD
A
Ctenocephalides
canis
Ctenocephalides
felis
MESOPLEUR
A DIVIDIDA
MESOPLEUR
A NO
DIVIDIDA
Tunga penetrans
Xenopsylla cheopis
Pulex irritans

PARASITOLOGIA MEDICA Página 65
CICLO DE VIDA DE Ctenophalides sp.

PARASITOLOGIA MEDICA Página 66
PEDICULOSIS
Definición: Infestación causada por piojos, las especies importantes para el hombre
son: (Anoplura – Pediculidae).
- Pediculus humanus var. vestimentis.
- Pediculus humanus var. capitis
- Pthirus pubis.
Características Morfológicas:
Los adultos: Observe adultos de Pediculus humanus y Pthirus pubis, en láminas
portaobjetos. Preste atención en Pediculus humanus, la forma del cuerpo. En la
cabeza: ojos simples, antenas cortas (5 segmentos) y aparato bucal invaginado. En
el tórax se nota la fusión de los tres segmentos. Patas con pretarso en forma de
gancho, que con un apéndice de la tibia forma una tenaza. En el abdomen los
segmentos están y se distinguen los estigmas respiratorios.
En la hembra, el último segmento es hendido o bilobulado, y en el macho, el mismo
segmento termina en forma redondeada, pudiendo observarse la espícula
sobresaliente.
Preste atención en Pthirus pubis que la cabeza pentagonal se encuentra “hundida”
en el tórax, y los otros elementos de la misma son similares a Pediculus humanus. El
tórax es ancho, corto y con segmentos fusionados. En las patas, el primer par es el
más pequeño, y el tercero el más grande. En el abdomen, los tres primeros
segmentos están fusionados y los estigmas respiratorios de estos segmentos se ven
en una sola fila, los demás segmentos presentan protuberancias cubiertas por pelos.
Dimorfismo sexual poco marcado. En las hembras suele verse huevos en el útero.
Los huevos o “liendres”: En preparaciones de huevos de Pediculus humanus en
láminas, preste atención a la manera como se adhiere al pelo. Repare en la
presencia de opérculo en el huevo.
Ciclo biológico: Metamorfosis gradual simple. (Ver esquema adjunto).

PARASITOLOGIA MEDICA Página 67
Diagnóstico: El diagnóstico de la pediculosis de la cabeza se hace por el hallazgo
de ejemplares adultos o ninfas en el cuero cabelludo, o de huevos “liendres”,
adheridos al pelo.
En la Pediculosis del cuerpo, la búsqueda de los adultos se hace en la vestimenta.
En la Pthiriasis, el diagnóstico se hace por el hallazgo de adultos y estadíos
evolutivos en el vello pubiano, y en ocasiones en otras zonas pilosas del cuerpo.
Importancia Médica:
a. Dermatitis por piojos: Las picaduras producen escozor y el rascado lesiones,
las que pueden infectarse, y si ello es masivo se puede observar la “piel de
vagabundo”.
b. Al Pediculus humanus var. vetimentis se le conoce como vector biológico de
Rickettsia prowazekii y Borrelia recurrentis.
Epidemiología: Tifus exantemático y recurrente se han señalado en nuestra zona
andina.
Pediculus humanus
ADULTO
HUEVO

PARASITOLOGIA MEDICA Página 68
EL CHINCHE DE CAMA
(Hemíptera – Cimicidae)
Cimex lectularius
Características Morfológicas: En preparaciones de adultos de Cimex lectularius,
observe el cuerpo cubierto de espinas cortas, cabeza pequeña, antenas filiformes,
ojos compuestos, piezas bucales plegados en la parte ventral de la cabeza. Aparato
bucal picador chupador. Tórax cuyo pronoto tiene expansiones anterolaterales que a
manera de aletas cubren la base de la cabeza. Carecen de alas membranosas,
presentan hemiélitros muy rudimentarios, patas terminadas en uñas. Abdomen con
segmentos anchos, los machos se diferencian de las hembras por presentar el
clasper sobresaliente, en el último segmento abdominal e incursado.
Ciclo biológico: (Ver esquema adjunto). Su metamorfosis es gradual.
Importancia Médica: Las picaduras producen dermatitis, en algunas personas.

PARASITOLOGIA MEDICA Página 69
VECTORES MECANICOS DE ENTEROPARASITOS: MOSCAS Y
CUCARACHAS
- Moscas (Díptera – Muscidae) - Cucarachas (Orthoptera-Blattidae)
Caracteres generales:
Las Moscas:
a. Morfología:
1. Los adultos: Observe los especimenes adultos de Musca domestica. Preste
atención a la cabeza, distinga los ojos compuestos útil para la diferenciación
de sexos: machos con ojos más próximos a la línea media, y en la hembra,
alejados de la misma. Antenas aristadas. En tres segmentos. Observe las
alas membranosas y balancinos. En las preparaciones microscópicas de la
mosca, preste atención al aparato bucal (rostro, haustelo, labella). Observe
las características de las antenas y la presencia de excrecencias del
exoesqueleto. Las patas con sus polvillos.
2. Los huevos: Observe microscópicamente, la forma y color de los mismos.
3. Las larvas: En la preparación microscópica de larvas, observe el espiráculo
posterior y el aparato bucal quitinisado.
4. Las pupas: Observe microscópicamente pupas de M. domestica preste
atención a su morfología y color.
b. Ciclo biológico: (Estudie el esquema adjunto).
Las cucarachas:
a. Morfología:
1. Los adultos: Observe adultos de cucarachas. Preste atención a la cabeza,
distinguiendo el aparato bucal (masticador), las antenas largas y filiformes,
los ojos compuestos. Observe el primer par de alas entrecruzadas
(Terminas), y el segundo par de alas membranosas observe la terminación
posterior del abdomen. Identifique los cercos.

PARASITOLOGIA MEDICA Página 70
2. Los ootecas: Observe microscópicamente, la morfología y el color de las
mismas.
3. Las ninfas: En las preparaciones de láminas con ninfas de cucarachas,
ubique el aparato bucal, y los arolios de las patas. Preste atención a la
abundancia de excrecencias del exoesqueleto.
b. Ciclo biológico: (Estudie el esquema adjunto).
CICLO BIOLÓGICO DE LA Musca domestica
Espiráculos posteriores

PARASITOLOGIA MEDICA Página 71
CICLO BIOLOGICO DE Periplaneta americana
MIASIS
Definición.- Infecciones causadas por larvas de moscas pertenecientes a diferentes
géneros. Las lesiones son predominantemente cutáneas, cavitarias y
excepcionalmente, en otras localizaciones (ocular, auditiva, etc.). Las especies
causantes de miasis, más importantes en el país son:
Díptera : Cochliomyia hominivorax
Dermatobia hominis
Oestrus ovis.
Caracteres generales: En especímenes adultos de Cochliomyia hominivorax
observe: los ojos compuestos, las antenas aristadas, las bandas del tórax. El color
verde metálico del abdomen. Observe las pupas y note la forma y color de las
mismas.
En preparaciones en láminas con larvas de Cochliomyia hominivorax, preste
atención a la forma vermiforme, adelgazada en su parte anterior y ensanchada,
gradualmente, hacia la parte posterior. Repare en la presencia del esqueleto céfalo-
faríngeo de la parte anterior y en la posterior, los espiráculos respiratorios.
(Importantes para el diagnóstico).

PARASITOLOGIA MEDICA Página 72
Observe larvas de Dermatobia hominis, microscópicamente, preste atención a la
forma y tamaño (Compare con las larvas de Cochliomyia hominivorax) ponga
atención a la presencia y distribución de las espinas. En algunos ejemplares, se
puede apreciar los espiráculos respiratorios posteriores.
Ciclo biológico: (Ver esquema adjunto)
Tienen metamorfosis completa, desarrollo holometábolo.
Diagnóstico: Se hace por el estudio de las larvas y en caso necesario, su evolución
hasta el estadío adulto.
Epidemiología: Las miasis son frecuentes en todo el mundo. En nuestra Selva, la
infección por la larva de Dermatobia hominis se conoce con el nombre de “clavo”.
CICLO BIOLOGICO DE Cochliomyia hominivorax

PARASITOLOGIA MEDICA Página 73
CICLO BIOLOGICO DE Dermatobia hominis
MÉTODOS DE DIAGNOSTICO DE LOS ENTEROPARÁSITOS
Los parásitos intestinales del hombre son protozoarios y/o helmintos o gusanos
intestinales.
Los helminto o gusanos pueden ser cilíndricos (Nemátodos), anillados o
segmentados (Tenia).
Para observar a los protozoarios, así como larvas y huevos de helmintos, se debe
usar el microscopio, en cambio, la mayor parte de los gusanos o helmintos adultos
son macroscópicos y su morfología puede estudiarse directamente.
Los protozoos intestinales eliminan con las heces, las formas evolutivas de
trofozoito, quiste, ooquiste y espora.
Los helmintos intestinales adultos pueden salir al exterior, espontáneamente
(proglótidos de Taenia sp., adultos de Enterobius vermicularis, Ascaris lumbricoides),
con las heces, o luego del tratamiento.

PARASITOLOGIA MEDICA Página 74
Los gusanos intestinales se eliminan con las heces, según la especie de parásito,
huevos, larvas o proglótidos.
Los métodos de diagnóstico de los enteroparásitos tienen por objeto demostrar la
presencia de los parásitos, ya sea, directamente, observando microscópicamente las
formas adultas de los gusanos o microscópicamente, los trofozoitos, quistes,
ooquistes, huevos o larvas, así como, indirectamente, por la demostración de
anticuerpos circulantes en sangre o antígenos en heces (coproantígenos).
EXAMEN DE HECES
En la mayor parte de los enteros parasitismos, las formas parasitarias que permiten
el diagnóstico se encuentran en las heces de la persona a estudiarse.
En las heces podemos encontrar formas adultas, así como formas microscópicas
(huevos, larvas, trofozoitos, quistes y ooquistes de los parásitos intestinales por ello,
es importante una buena obtención de muestra fecal.
OBTENCION DE LA MUESTRA
La muestra (4-6 gramos) debe ser obtenida lo más fresca posible, y depositada en
frasco de boca ancha con tapa, rotulada, correctamente, con el nombre de la
persona de quien se obtiene la muestra y datos de identificación, edad, sexo, fecha,
procedencia, síntomas, etc.
La muestra debe obtenerse antes de la administración de medicamentos o 2-5 días
después.
Las heces depositadas en el suelo no son las recomendadas para el diagnóstico,
debido a que pueden contaminarse con formas biológicas, larvas por ejemplo
similares a los enteroparásitos del hombre (larvas de nemátodos, huevos de ácaros,
etc.).
Si el paciente no es regular en sus deposiciones y ha evacuado en la noche, se
recomienda, guardar la muestra en la refrigeradora para que no se alteren las formas
parasitarias, cuando va a demorar en llegar al laboratorio varias horas o días se
recomienda adicionar el líquido fijador y/o conservador PAF, PVA, formalina 10%,
SAF, Acetato de sodio.

PARASITOLOGIA MEDICA Página 75
MÉTODOS DE EXAMEN
1. EXAMEN DIRECTO MACROSCOPICO
1.1 Fundamento: Las características morfológicas de los parásitos adultos, enteros
o fraccionados pueden observarse directamente, así como también se pueden
observar alteraciones en las heces eliminadas que pueden o no corresponder a
un parasitismo, pero que es importante ser registrada, como el cambio de color,
presencia de sangre, etc.
a. Se observan las características organolépticas de las heces (consistencia,
aspecto, color, etc.) que en condiciones anormales puede ser útil en el
diagnóstico de las parasitosis intestinales y otras etiologías.
b. Permite observar la presencia de elementos anormales como moco, sangre,
epitelio, etc.
c. Permite estudiar las características morfológicas de los gusanos o de sus
partes que son eliminados.
1.2 Material necesario:
Suero fisiológico (ver Anexo)
Aplicador (bajalengua)
Pinza de metal
Coladera de metal o plástico
1.3 Procedimiento:
Agregar suero fisiológico, en cantidad suficiente para homogenizar la muestra.
Tamizar o colar la muestra, en caso de presencia de formas adultas.
1.4 Lectura u Observación:
Observar las características organolépticas de las heces, útiles para la ayuda
diagnóstica consistencia, color, presencia de moco, sangre, alimento sin digerir.
Presencia de gusanos redondos o aplanados, enteros o parte de ellos.
1.5 Adicionar al informe del examen parasicológico, las características
macroscópicas de las heces que no sean normales y que sean útiles para el
diagnóstico.

PARASITOLOGIA MEDICA Página 76
2. EXAMEN DIRECTO MICROCOPICO
2.1 Fundamento:
Buscar, principalmente en muestras frescas, la presencia de formas evolutivas
móviles de parásitos: trofozoitos (Entamoeba spp., Giardia lamblia, Balantidium
coli, Trichomonas hominis, etc.), larvas de Strongyloides stercoralis, así como
los quistes, ooquistes y huevos.
2.2 Materiales necesarios:
Láminas portaobjetos
Laminillas cubreobjetos
Aplicador de vidrio o madera
Marcador de vidrio
Suero fisiológico (ver Anexo)
Solución de Lugol (ver Anexo)
Verde brillante (ver Anexo)
Rojo Neutro (ver Anexo)
2.3 Procedimiento:
Colocar, en un extremo de la lámina una gota de suero fisiológico y con ayuda
de un aplicador.
Agregar 1-2 mgm. de material fecal de la muestra, emulsionarla y cubrirla con
una laminilla cubreojo.
Colocar, en el otro extremo de la lámina portaobjeto, una gota de lugol, y
proceder a la aplicación de la muestra fecal como en el párrafo anterior.
Con el suero fisiológico, los trofozoitos y quistes de los protozoarios se observan
en forma natural, y las estructuras internas, núcleos y vacuolas en las tinciones
con lugol.
En algunos casos, se recomienda el uso de colorantes vitales, que no alteran la
actividad del trofozoito, estos son: verde brillante al 0.2% y rojo neutro 0.01%.
2.4 Lectura u observación microscópica:
Se debe observar al microscopio, a menor (10x) o mediano (40x) aumentos. No
es aconsejable usar objetivo de inmersión (100x), pues se puede ensuciar el
microscopio.

PARASITOLOGIA MEDICA Página 77
Se debe recorrer la lámina siguiendo un sentido direccional, ejemplo: derecha,
izquierda, o de arriba abajo.
2.5 Se notará el nombre de la especie del parásito, y su estadío evolutivo.
3. MÉTODOS DE CONCENTRACION
Los trofozoitos, quistes, ooquistes, larvas y huevos, pueden concentrarse por
diversos procedimientos, lo cual permite corroborar el hallazgo del método
directo y conocer la intensidad del enteroparsitismo.
Los procedimientos de concentración pueden ser por Flotación, Sedimentación,
o por combinación de ambos métodos.
La elección de cada procedimiento dependerá de las facilidades de laboratorio
adiestramiento del personal del área geográfica y especie de parásito que se
desea investigar
Métodos de Concentración por Sedimentación:
Técnica de la Sedimentación Espontánea (Técnica de concentración por
sedimentación sin centrifugación)
1. Fundamento: Se basa en la gravidez que presentan todas las formas
parasitarias para sedimentar espontáneamente, en un medio menos denso y
adecuado, con la solución fisiológica. En este método es posible la detección de
huevos de Paragonimus mexicanus y Fasciola hepatica.
2. Material necesario:
Tubos de vidrio o plástico de 16x150 ó 20x180 mm, o mejor de 50 mL de
capacidad que terminen o no en forma cónica. En caso contrario usar tubos de
13x100.
Láminas portaobjetos
Laminillas de celofán recortadas adecuadamente (2x2 í 2x6cm)
Cloruro de sodio o sal de cocina
Pipetas de vidrio o plástico
Agua destilada, hervida o de lluvia
Gasa recortada en trozos de 9x9 cm.

PARASITOLOGIA MEDICA Página 78
3. Procedimiento:
a. Tomar una porción de heces (2 a 3 grs) y homogenizarla con suero
fisiológico en un recipiente limpio, o en el mismo recipiente en que se ha
obtenido la muestra.
b. Colocar la gasa, hundiéndola en la abertura del tubo, y sujetándola con una
liga alrededor de ella.
c. Filtrar el homogenizado a través de la gasa, llenando el tubo hasta la cuarta
parte de su contenido.
d. Agregar suero fisiológico hasta 1 cm por debajo del borde del tubo.
e. Ocluir la abertura del tubo con la tapa o también con parafina platina o
celofán.
f. Agitar enérgicamente el contenido, por aproximadamente 15 segundos.
g. Dejar en reposo por 45 minutos. En caso que el sobrenadante esté muy
turbio, eliminarlo y repetir la misma operación con solución fisiológica.
h. Aspirar con la pipeta, la parte media del sedimento, y colocar unas 4 gotas
en la lámina portaobjeto. Aspirar nuevamente con la pipeta, del fondo del
sedimento y agregar 1 o 2 gotas de solución lugol.
i. Cubrir ambas preparaciones con las laminillas de celofán.
j. Observar al microscopio.
4. Lectura y observación microscópica:
Se observa primero la lámina con solución fisiológica para ver las formas
móviles (trofozoitos y larvas) y luego, la preparación con lugol, para observar
sus estructuras.
5. Resultado:
Se informará de la presencia de las formas evolutivas de los parásitos.
3.1.2 Método de Sedimentación Rápida (TSR, MSR) Lumbreras y Col. 1962
(Concentración por Sedimentación sin centrifugación)

PARASITOLOGIA MEDICA Página 79
1. Fundamento:
Se basa en la gravidez de los huevos que por su tamaño y peso, sedimentan
rápidamente, cuando se suspenden en agua. En este método también es
posible la detección de huevos de Paragonimus mexicanus y Fasciola hepatica.
2. Material necesario:
Copia o vaso de vidrio o plástico, cónico de 200 a 300 mL. Gasa
Coladera de malla metálica o plástico Pipeta pasteur
Placas Petri o lunas de reloj
Aplicador de madera (1/3 de baja lengua)
Agua corriente o filtrada
3. Procedimiento:
a. Homogenizar 4 a 6 gr de heces con unos 10 a 20 mL de agua filtrada.
b. Colocar la coladera en la abertura del vaso y a través de ella filtrar la
muestra.
c. Retirar la coladera y llenar la copia con agua filtrada hasta 1 cm del borde,
esto es 15 a 20 veces el volumen de la muestra.
d. Dejar sedimentar la muestra durante 20 a 30 minutos.
e. Decantar las 2/3 partes del contenido del vaso y agregar nuevamente agua.
f. Repetir los pasos d) y e) cada 5-10 minutos por 3 a 4 veces más, hasta que
el sobrenadante quede límpido.
g. Transferir el sedimento a una placa Petri.
h. Observar al esteroscopio o microscopio, a menor aumento.
4. Lectura u observación microscópica:
Observar al esteroscopio o al microscopio la presencia de huevos,
especialmente útil para la búsqueda de Paragonimus mexicanus, Fasciola
hepatica y nematodos como Ascaris lumbricoides huevo fecundado o no
fecundado, Trichuris trichiura, Hymenolepis sp., Diphyllobothrium pacificum, etc.
5. Resultado:
Informe de la presencia de huevos del parásito.

PARASITOLOGIA MEDICA Página 80
3.1.3 Método de Sedimentación y Flotación por Centrifugación: Técnica de
Faust
1. Fundamento:
Esta técnica concentra, por flotación, los quistes y/o huevos de parásitos
aprovechando su menor densidad frente a una solución de mayor densidad
como es el sulfato de zinc al 33%.
Previamente, se les ha concentrado por sedimentación de la muestra mediante
centrifugación.
Es útil para la búsqueda de quistes y/o huevos de parásitos, excepcionalmente
se observan larvas.
Es conveniente controlar la densidad del sulfato de zinc. Se recomienda usar
agua filtrada para el lavado previo de la muestra.
2. Material necesario:
Gradilla para tubos de ensayo
Tubos de prueba 15x150
Tubos de prueba 13x100
Solución de lugol
Láminas portaobjetos
Embudo de vidrio
Laminillas cubreobjetos
Gasa
Bajalengua de madera
Sulfato de zinc 33.3%, Densidad 1.180 (ver Anexo)
3. Procedimiento:
a. Colocar 1 a 2 gr de la muestra de heces en el tubo de prueba 13x100 y
agregar 7-8 mL de agua filtrada o destilada y hacer una buena
homogenización.
b. Colocar al tubo 13x100 el embudo de vidrio con dos capas de gasa y filtrar la
muestra homogenizada hasta alcanzar 1 cm del borde del tubo.
c. Retirar el embudo y centrifugar de 2.000 a 2.500 r.p.m. durante 2-3 min.
d. Decantar el sobrenadante, adicionar el agua al sedimento y repetir la
centrifugación 1 o 2 veces más, hasta que el sobrenadante se observe
limpio.

PARASITOLOGIA MEDICA Página 81
e. Eliminar el sobrenadante y agregar la solución del sulfato de zinc (3-4 mL)
homogenizar y completar con la misma solución hasta 1 cm del borde del
tubo.
f. Centrifugar por 1-2 minutos de 2.000 a 2.500 r.p.m.
g. Colocar el tubo en la gradilla y agregar con ayuda de un gotero, la solución
de sulfato de zinc hasta formar un menisco en la boca del tubo.
h. Colocar una laminilla cubreobjeto sobre el menisco y dejar en reposo por 30
minutos.
i. Depositar una gota de solución lugol en la lámina portaobjeto.
j. Retirar la laminilla cubreobjeto y colocarla sobre la gota de lugol, o tomar con
una asa de platino la superficie del menisco y colocar 3-4 asadas en la
lámina.
k. Observar al microscopio.
4. Lectura u observación microscópica:
Se observan principalmente quiste y huevos de parásitos.
5. Resultado:
Se expresa por el hallazgo de quistes y/o huevos o larvas de parásitos y por
cruces, la cantidad de elementos observados sólo la nominación si hay 1-2 en
toda la lámina, +=escaso de 2-5 por lámina, ++=5-11 por campo y +++mayor de
11 por campo.
3.4 Métodos de Flotación:
3.4.1 Método de Flotación con solución de azúcar (Sheather sugar)
1. Fundamento:
Se basa en la flotación de quistes, ooquistes y huevos de parásitos en una
solución de azúcar que posee mayor densidad.
Esta técnica es útil para la concentración de quistes y ooquistes de protozoos y
huevos de helmintos, se usa como método preferencial en el diagnóstico de las
coccidias: Cryptosporidium parvum, Cyclospora cayetanensis, Cystoisospora
belli (=Isospora belli), etc.

PARASITOLOGIA MEDICA Página 82
2. Materiales necesarios:
Tubos de ensayo 13x100
Láminas portaobjetos
Laminillas cubreobjetos
Aplicador
Solución saturada de azúcar (ver Anexo)
Asa de platino
Gradilla para tubos de ensayo
Suero fisiológico (ver Anexo)
Embudo de vidrio
Gasa
3. Procedimiento:
a. Homogenizar 1-2 g de material fecal en suero fisiológico.
b. Colocar el embudo de vidrio en la abertura del tubo de ensayo con una gasa
doblada, filtrar el material homogenizado.
c. Centrifugar el tubo con el material homogenizado a 1.500 r.p.m. durante 2-5
minutos.
d. Eliminar el sobrenadante y agregar la solución de azúcar hasta 1cm del
borde del tubo, agitarlo hasta disolver el sedimento, centrifugar como en el
paso c) y completar, con la solución de azúcar hasta el borde y formar un
menisco (esperar 2-5 minutos).
e. Con la ayuda del asa de platino tomar una muestra de la superficie del
menisco y colocarla en una lámina portaobjeto. Agregar lugol, en caso
necesario, cubrir con una laminilla y observar al microscopio.
f. En el caso de observar coccidias, de la superficie del preparado tomar con el
asa de platina o con una pinza curva preparar frotices para teñir con Ziehl-
Neelsen.
4. Lectura y observación microscópica:
Esta técnica es apropiada para la observación de ooquiste de Cystoisospora
belli (=Isospora belli), Cryptosporidium parvum, Cyclospora cayetanensis y
Sarcocystis hominis.

PARASITOLOGIA MEDICA Página 83
5. Resultado:
Se debe informar de la presencia de las formas evolutivas de los parásitos y su
densidad en la muestra examinada.
3.4.2 Método de Parodi Alcaraz (Concentración por Flotación, sin centrifugación)
1. Fundamento:
Se basa en la propiedad que tienen los quistes y/o huevos de flotar en la
superficie de una solución sobresaturada de azúcar, debido a su menor
densidad.
1. Material necesario:
Tubos de 13x100 ó 15x150
Láminas portaobjetos
Laminillas cubreobjetos
Solución sobresaturada de azúcar (azúcar rubia) (ver Anexo)
Formol
Baguetas o aplicador de madera (1/3 de bajalengua)
Solución de lugol.
2. Procedimiento:
a. Colocar 1 a 2 g de heces en el tubo de ensayo.
b. Agregar 3 a 5 mL de la solución sobre saturada de azúcar y con un
aplicación, hacer una buena homogenización.
c. Completar el contenido del tubo con la misma solución de azúcar hasta
formar un menisco en la abertura del tubo.
d. Dejar en reposo 30 minutos.
e. Colocar en contacto con el menisco, en la abertura del tubo una laminilla
cubreobjeto que va a permitir la adherencia, por viscosidad, de los quistes y
huevos.
f. En la lámina portaobjeto colocar una gota de la solución de lugol.
g. Retirar la laminilla, con sumo cuidado de la abertura del tubo y colocarla
sobre la lámina portaobjeto.
h. Examinar al microscopio.

PARASITOLOGIA MEDICA Página 84
3. Lectura u observación al microscopio:
Es conveniente la observación inmediata a 100x y 400x, pues los quiste y/o
huevos, suelen deformarse si la densidad de la solución es demasiado alta.
4. Resultado:
Se debe informar los estados evolutivos de los parásitos encontrados. El método
es útil para quistes y huevos de nemátodos y tenias.
MÉTODO DE BAERMANN
1. Fundamento:
Se basa en los tropismos positivos: geotropismo, terinotropismo e indrotropismo
de los trofozoilos de protozoos y larvas de helmintos, principalmente para
Balantidium coli y larvas de Strongyloides stercoralis.
2. Materiales:
Copas cónicas de 200 a 300 mL
Rejilla o coladera metálica
Pipetas Pasteur
Gasa
Láminas escabadas
Láminas portaobjetos
Suero fisiológico (ver Anexo)
3. Procedimiento:
a. Verter solución salina caliente en la copa, cantidad suficiente que apenas
toque la coladera o rejilla.
b. Colocar la coladera o rejilla metálica con la base doblada dentro de la copa
(ver figura) y gasa (2 a 3 capas).
c. Colocar 4-6 gr de la muestra de heces en fresco, sobre la gasa.
d. Dejar todo el sistema a temperatura ambiente o en estufa a 28-37ºC durante
30-50 min.
e. Sacar la rejilla o coladera y con ayuda de una pipeta Pasteur obtener 1 mL
de sedimento.

PARASITOLOGIA MEDICA Página 85
f. Colocar el sedimento en una luna de reloj o lámina escabada. Observar al
microscopio o al estereoscopio.
4. Lectura y Resultados.
Se observan los trofozoilos y las larvas en movimiento. En caso del hallazgo de
larvas de nemátodos, hacer el diagnóstico diferencial, guiándose por las figuras.
En caso de duda y contando con las condiciones apropiadas, realizar el método
de Harada-Mori.
En algunas ocasiones se pueden observar formas adultas de Enterobius
vermicularis macho.
MÉTODO CUALITATIVO: Técnica de Kato
1. Fundamento:
Este método consiste en la aclaración de las heces por el uso de la glicerina, lo
que permite preparar una capa transparente y observable de las heces.
2. Materiales necesarios:
Láminas portaobjetos
Aplicador
Papel celofán, cortado en pedazos de 4 x 3 cm y sumergirlos en la solución
glicerinada por un periodo no menor de 24 horas.
Malla metálica o nylon
Solución glicerina con verde de malaquita (ver Anexo)
3. Procedimientos:
a. Tamizar 0.5 g de la muestra de heces a través de una malla metálica o de
nylon fino.
b. El tamizado se extiende sobre la lámina portaobjeto.
c. Cubrir con la laminilla impregnada en glicerina
d. Envolver con papel filtro, toalla o periódico, la lámina, para comprimir la
muestra y secar el exceso de glicerina por 30 minutos.
e. Observar al microscopio.
4. Resultado:
Es una técnica apropiada para la observación de huevos de helmintos y algunos
protozoarios como Cystoisospora belli.

PARASITOLOGIA MEDICA Página 86
4.- MÉTODOS DE COLORACION
Método de Ziehl-Neelsen (modificado para observación de Coccidias)
1. Fundamento:
Se basa en el comportamiento ácido-resistente de la cubierta de estos
parásitos, los cuales se tiñen de rojo y destacan sobre un fondo verde y azul,
dependiendo del colorante de contraste usado.
2. Material necesario:
Láminas portaobjetos
Laminillas cubreobjetos
Soporte de varillas de vidrio para coloración de láminas portaobjeto
Estiletes o pinzas curvas
Fucsina fenicada
Azul de Metileno acuoso
Metanol
Hidróxido de sodio al 4%
Alcohol ácido
3. Procedimiento:
a. Colocar las láminas portaobjeto sobre el soporte de las varillas de vidrio.
b. Con el estilete o pinza curva hacer 1 frotis en la lámina portaobjeto y dejar
secar.
c. Fijar la lámina con alcohol metílico por 2 a 5 minutos, y dejar secar
d. Agregar hidróxido de sodio sobre el preparado por un minuto, eliminar
exceso
e. Cubrir con la fucsina fenicada (previa agitación del frasco) la lámina por 5
minutos.
f. Lavar suavemente la lámina portaobjeto con agua corriente.
g. Decolorar con alcohol-ácido cubriendo el portaobjeto por unos segundos,
hasta quitar el colorante.
h. Lavar suavemente el portaobjeto con agua y enjuagarlo a chorro de agua
i. Colocar, como colorante de contraste, verde de malaquia 1% o azul de
metileno 1-1.4% durante 5 minutos.
j. Lavar la lámina, suavemente, con agua corriente, dejar secar al aire.

PARASITOLOGIA MEDICA Página 87
k. Realizar el montaje con bálsamo de Canadá y laminilla cubreobjeto.
l. Observar al microscopio.
4. Lectura u observación microscópica:
Cubrir la lámina con una gota de aceite de inmersión y observar al microscopio
a 400x y 1000x.
5. Resultado:
Los ooquistes de Cystoisospora belli (=Isospora belli), Cryptosporidium parvum,
Cyclospora cayetanensis aparecen de un color rojo fucsia sobre un fondo
verdoso o azul; sólo en algunos casos no se colorean pero, permiten
diferenciarlos.
MÉTODOS DE RITCHE
1. Fundamento:
Concentración de quistes y huevos por sedimentación mediante la
centrifugación y con la ayuda de formol y éter para separar los elementos
parasitarios.
2. Materiales:
Gradilla de tubos de ensayo
Tubos de ensayo 15x150
Pipetas Psateur
Lámina portaobjetos
Laminillas cubreobjetos
Hisopo
Solución de formol al 10%
Solución fisiológico (ver Anexo)
Eter etílico
Lugol
Baja lengua descartable

PARASITOLOGIA MEDICA Página 88
3. Procedimiento:
Colocar en el tubo de ensayo 1 a 2 g de muestra de heces, agregar 8 mL de
solución fisiológica, homogenizar y centrifugar a 2,000 rpm por 2-3 minutos.
Descartar el sobrenadante, y repetir el paso anterior hasta que se observe el
sobrenadante limpio.
Decantar el sobrenadante, agregar al sedimento 6 mL de solución de formol al
10%, homogenizar y dejar reposar 5 minutos, luego de los cuales se agrega 3
mL de éter.
Taponar el tubo y agitar cuidadosamente para evitar la salida del material.
Retirar la tapa, centrifugar el tubo a 2-3.000 rpm por 3 minutos.
Eliminar las capas formadas de sobrenadante; si es necesario, con la ayuda de
un hisopo.
Depositar una gota de lugol en la lámina portaobjeto, y con ayuda de la Pipeta
Pasteur, tomar una porción del sedimento y mezclarlo con la gota de lugol.
Cubrir con una laminilla cubreobjeto y observar al microscopio.
4. Lectura:
Se observan quiste y/o huevos de parásitos, ocasionalmente trofozoitos y
larvas.
5. Resultado:
Se expresan los nombres de los quistes y/o huevos observados. En ocasiones
se observan y deben señalarse la presencia de cristales de Charcot-Leyden.
MÉTODO CUANTITATIVO DE KATO - KATZ
1. Fundamento:
Se basa en la técnica de Kato para cuantificar la presencia de huevos de
helmintos y se expresa número de huevos por gramo de heces (nhpgh)
2. Materiales:
El kit del Kato-Katz contiene:
Aplicadores
Papel de celofán impregnado con glicerina y verde de malaquita
Molde de plástico con perforación
Malla metálica o de nylon
Además se requiere láminas portaobjetos 2.5x7.5

PARASITOLOGIA MEDICA Página 89
3. Procedimiento:
a. Con un aplicador (bajalengua) se transfiere la muestra fecal (5-10 mg) sobre
el papel absorbente.
b. Colocar la malla o nylon sobre la muestra que está en el papel absorbente,
comprimiendo la muestra con el aplicador del kit, y llenar el molde perforado
comprimiendo.
c. Transferir el molde sobre la lámina portaobjeto y dejar la muestra del
cilindro.
d. Colocar la laminilla glicerina y con ayuda de un tapón de jebe se extiende el
material sobre toda la laminilla.
e. Dejar a temperatura ambiente por 30-45 minutos, por diafanisación se
observará los huevos sobre toda la laminilla.
4. Resultado:
El número de huevos encontrados en la lámina se multiplica por 24, el resultado
es el número de huevos por gramo de heces (nhpgh). Se recomienda contar
todos los huevos que hay en el preparado.