Leucemia Mieloide Aguda
-
Upload
oswaldo-angeles -
Category
Health & Medicine
-
view
906 -
download
1
Transcript of Leucemia Mieloide Aguda
Leucemia Mieloide Aguda.Cortes Breton Blanca Ivonne Gómez Pimentel Pedro Muratalla Bedolla EstephanyRodríguez López Edith.
Daño al DNA pérdida de la regulación
Protooncogén a oncogén
Pérdida de gen supresor
Célula precursora
hematopoyética a célula
leucémica
Factores genéticos y séricos
Proliferación clonal
desordenada
Factores genéticos
Síndromes de fragilidad cromosómica
Deterioro en la reparación DNA: anemia de Fanconi, ataxia-telangiectasia y Sindrome de Bloom
Alteraciones de la mielopoyesis: agranulocitosis genética de Kostmann y anemia de Blackfand-Diamond
Factores ambientales
Benceno
Radiaciones ionizantes
Citostáticos:
Agentes alquilantes
Inhibidores de la
topoisomerasa (tenipósido y etopósido)
Virus (retrovirus HTLV-I y HTLV-II)
¿Cómo se diagnostica la leucemia mieloide aguda?
Es común que las personas con AML sientan una pérdida de bienestar, debido a la producción insuficiente de células normales de médula ósea.
Es posible que la persona se canse con más frecuencia y que le falte el aliento durante las actividades físicas normales.
Palidez.
Signos de sangrado:
Moretones.
Hematomas sin motivo aparente o debidos a una lesión menor.
Petequias.
Sangrado prolongado por cortaduras leves.
Fiebre leve.
Encías inflamadas.
Infecciones menores frecuentes, tales como llagas perianales
Pérdida de apetito y pérdida de peso
Molestias en huesos o articulaciones
Aumento del tamaño del bazo
Aumento del tamaño del hígado.
Leucopenia.
Neutropenia.
Trombocitopenia.
• Exceso de hematomas y sangrado.
• Epistaxis frecuente o severa.
• Sangrado de las encías.
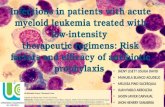
Células de médula ósea normales y células blásticas de AML
Células de médula ósea normales.
Las siluetas más oscuras son los núcleos de las células.
Algunos de los núcleos son circulares y otros tienen forma de herradura, reflejando las distintas etapas del desarrollo y los distintos tipos de células.
Células blásticas de AML.
Se “detienen” en las primeras etapas del desarrollo.
Las células de AML tienen una apariencia similar.
Requiere del analisis de sangre periferica y medula osea.
20% de blastos.
Inmunohistoquimica.
Inmunofenotipo.
Citogenética.
Biología molecular.
Tele de tórax y abdomen.
Ecocardiograma.
Imagen radiológica de cavidad oral.
Clasificación FAB
1976
Grupo cooperativo Franco-Americano-Britanico.
Aspecto morfológico.
Comportamiento cito químico de la célula blastica.
Las clasificaciones de AML de la OMS
AML con anomalías genéticas recurrentes
AML con cambios relacionados con la mielodisplasia
AML relacionada con la terapia
AML sin otra especificación
AML con una translocación entre los cromosomas 8 y 21
AML con una translocación o inversión del cromosoma 16
AML con cambios en el cromosoma 11
Leucemia promielocítica aguda (APL, M3), que suele presentar una translocación entre los cromosomas 15 y 17.
TRATAMIENTOLa finalidad del tratamiento es el control de la
enfermedad a largo plazo, el cual se divide en dos rubros:
oTratamiento de sostén o mantenimientooTratamiento especifico
Tratamiento de sostén o mantenimientoProporcionar las medidas necesarias para
mejorar las condiciones generales del paciente, este se contempla antes y durante el tratamiento especifico
Con el uso de hemoderivados:o Paquetes globulares para corregir la anemia.o Concentrados plaquetarios o aféresis de
plaquetas para control de hemorragiaso Plasma y crioprecipitados en alteraciones de la
coagulación
Fase de inducción Daunorrubicina 60 mg/m2 por
dia durante 3 dias, citarabiana 100 mg/m2 infusioncontinua por dia durante 7 dias (7+3).
De alcanzar la remision completa se administra un segundo 7 + 3 o dependiendo de tolerancia solo 5 + 2.
La presencia de neutropenia febril o prolongada son indicaciones del uso de filgrastrim
Fase de consolidaciónUna vez que alcanzaron remisión
completa. Se administra dosis alta de
citarabina 3 g/m2 cada 12 h en infusión de 3 horas los días 1, 3 y 5 por 3 a 4 ciclos, con intervalos de 28 a 35 días o a la recuperación hematológica.
AlternativoOfrecer 7 + 3 o 5 + 2 en algunos
pacientes dependiendo de la tolerancia
Fase de mantenimientoLos que tuvieron la respuesta completa
después de la consolidación o pacientes mayores con morbilidades importantes, deben recibir cuidados de soporte y tratamiento sistémico paliativo:
o 6-mercaptopurina 50 mg/m2por dia
o Metotrexate 20 mg/m2 semanal
o Ciclofosfamida 200 mg/ m2 semanal
o Vincristina 1.4 mg /m2 maximo 2 mg mensual por 2 años.
Indicaciones para trasplanteo Pacientes que no presentaron
remisión completa en el primer ciclo
o Pacientes con recaída y subsecuente segunda remisión completa
o Riesgo intermedio con mutación FLT3
o Todos aquellos que tienen riesgo desfavorable .
Cuidados de soporte
o Tratamiento de infecciones
o Transfusiones en anemia, trombocitopenia.
o Factores de crecimiento eritroide y mieloide.
o Prevención de Síndrome de lisis tumoral con hiperhidratacion y alopurinol.