Números cuánticos
-
Upload
cata-marin-cruz -
Category
Documents
-
view
8.772 -
download
2
description
Transcript of Números cuánticos

Números cuánticos
Profesora:
Karla Navarrete

NÚMERO CUÁNTICO PRINCIPAL.
• En la corteza, los electrones se sitúan siguiendo caminos determinados llamados orbitales. Cada orbital está definido por tres números cuánticos, que determinan el tamaño, la forma y la orientación del orbital.
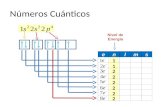
• El número cuántico principal (n), determina el tamaño del orbital. Puede tomar cualquier valor natural distinto de cero: n = 1, 2, 3, 4 ...

NÚMERO CUÁNTICO AZIMUTAL.
• El número cuántico azimutal (l), indica la forma del orbital, que puede ser circular, si vale 0, o elíptica, si tiene otro valor.
• El valor del número cuántico azimutal depende del valor del número cuántico principal. Desde 0 a una unidad menos que n. Si el número cuántico principal vale 1, n = 1, el número cuántico azimutal sólo puede valer 0, ya que sus
• posibles valores van desde 0 hasta n-1.
g4
f3
d2
p1
s0
Letras de lL

Valor de L
0,1,2,3,4 (s,p,d,f,g)N=5
0,1,2,3 (s,p,d,f)N=4
0,1,2 (s,p,d)N=3
0,1 (s,p)N=2
0 (s)N= 1
Valor de l va desdes 0 hasta n-1 (letra representa a L)
Valor de n

NÚMERO CUÁNTICO MAGNÉTICO.
• El número cuántico magnético, m, determina la orientación del orbital. Los valores que puede tomar depende del valor del número cuántico azimutal, m, variando desde - l hasta + l.
• Si el número cuántico azimutal vale 1, l = 1, el número cuántico magnético puede tomar los valores -1, 0 y 1, ya que sus posibles valores van desde -l hasta l. Hay, por lo tanto, tres orbitales p, ya que si l = 1 el orbital se llama p

Valor del número magnético
-4,-3,-2,-1,0,1,2,3,4L=4
-3,-2,-1,1,2,3L=3
-2,-1,0,1,2L=2
-1,0,1l= 1
Valor de ml
Su valor va desde –L a L
Valor de l

NÚMERO CUÁNTICO DE SPÍN.
• Este giro del electrón sobre sí mismo está indicado por el número cuántico de espín, que se indica con la letra s. Como puede tener dos sentidos de giro, el número de espín puede tener dos valores: ½ y - ½.

Orbital atómico
93s
3px, 3py, 3pz
3dyz 3dxz 3dxy 3dx2-y2 3dz2
1
3
5
0
-1,0,1
-2,-1,0,1,2
0
1
2
3
42s
2px, 2py, 2px
1
3
0
-1,0,1
0
1
2
11s1001
Número total de orbital
Designación de orbitalesNúmeros de orbitales
MLN

Configuración Electrónica

Principio de construcción
• Los electrones se ubican primero en los orbitales de más baja energía, por lo tanto los de mayor energía se ocupan sólo cuando los primeros hayan sido ocupados.

Orden de llenado de orbitales

Principio de exclusión de Pauli
• Los orbitales son ocupados por dos electrones como máximo, siempre que ocupen espines distintos.

Principio de máxima multiplicidad de Hund
• En los orbitales de la misma energía los electrones entran de a uno, ocupando cada orbital con el mismo espin y cuando alcanza el semillenado, se produce el apareamiento en los espines opuestos.

Ejercicios
• Realice la configuración electrónica para los siguientes elementos.
• Z=4 = 1s 2s• Z=10
• Z=19
• Z=26