Reaciones Quimicas Nt
-
Upload
natalia-toubes -
Category
Technology
-
view
3.869 -
download
3
Transcript of Reaciones Quimicas Nt

Prof. Natalia Toubes
CAMBIOS FÍSICOS Y
CAMBIOS QUÍMICOS.

Prof. Natalia Toubes

Prof. Natalia Toubes

Prof. Natalia Toubes

Prof. Natalia Toubes
Aquí se identifican fenómenos físicos y químicos, para un fenómeno natural y para un hecho de la vida diaria:
Durante el proceso de FOTOSÍNTESIS:
• La hoja toma dióxido de carbono (CO2) del aire,(también llega el H2O tomada del suelo por la raíz ). FÍSICO
• El AGUA se transforma en HIDRÓGENO (H2) y OXÍGENO (O2). QUÍMICO
• El OXÍGENO se desprende de la planta y vuelve a la atmósfera .FÍSICO
• El HIDRÓGENO reacciona con el DIÓXIDO DE CARBONO para formar ALMIDÓN .QUÍMICO

Prof. Natalia Toubes
INDICIOS DE QUE HA PODIDO OCURRIR UN CAMBIO QUÍMICO O REACCIÓN QUÍMICA:
• Formación de un precipitado.• Desprendimiento de gases.• Cambios de color.• Absorción o liberación de calor.• Cambios en otras propiedades como
acidez, olor, aparición de propiedades magnéticas o eléctricas.

Prof. Natalia Toubes
¿ qué sucede a nivel microscópico durante un cambio químico?

Prof. Natalia Toubes

Prof. Natalia Toubes

Prof. Natalia Toubes
¿Cómo se representa un cambio químico o reacción
química?

Prof. Natalia Toubes

Prof. Natalia Toubes

Prof. Natalia Toubes
PRINCIPIO DE CONSERVACIÓN DE LA MASA

Prof. Natalia Toubes
PRINCIPIO DE CONSERVACIÓN DELA MASA.
2 IK + Pb (NO3)2 PbI2 + 2KNO3

Prof. Natalia Toubes
PRINCIPIO DE CONSERVACIÓN DELA MASA.
• Ahora bien, el número de átomos de cada elemento en los reactivos debe ser igual al que existe en los productos
• Esto nos obliga a realizar un ajuste de la ecuación química para que el número de átomos de cada elemento en los reactivos sea igual al que existe en los productos.

Prof. Natalia Toubes
Ajuste de ecuaciones para que se cumpla la ley de conservación de la
masa.H2 + O2 H2O
Vemos que en los reactivos hay dos átomos de oxígeno mientras que en los productos sólo hay uno.
• ¿Qué tal si multiplicamos por dos la molécula de agua? H2 + O2 2 H2O
Ahora tenemos igualdad en los átomos de oxígeno, pero no en los de hidrógeno. De estos hay cuatro en los productos y sólo dos en los reactivos.
• ¿Por qué no multiplicamos por dos el hidrógeno en los reactivos?
2 H2 + O2 2 H2O

Prof. Natalia Toubes
Ajuste de ecuaciones.Formación del agua.
A los números que hemos añadido para ajustar la ecuación se les llama coeficientes estequiométricos.
2 H2 + O2 2 H2O nº de átomos en la molécula.
coeficiente estequiométrico (nº de moléculas)
“ las ecuaciones químicas son las representaciones simbólicas de las reacciones reales. En ellas, el número de átomos de cada elemento es el mismo en las sustancias iniciales y en las finales.”

Prof. Natalia Toubes
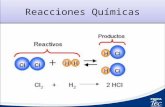
REPRESENTACIÓN GRÁFICA DE REACCIONES QUÍMICAS.
• Las reacciones químicas pueden ser representadas mediante los modelos moleculares.
Dibujando los átomos como si fueran esferas y construyendo así las
moléculas de las sustancias que intervienen en una reacción.

Prof. Natalia Toubes
REPRESENTACIÓN GRÁFICA DE la reacción química de formación
de agua.
H2 + O2 H2O
esta representación no cumple el principio de conservación de la masa.!!!

Prof. Natalia Toubes
2 H2 + O2 2 H2O
esta representación si cumple el principio de conservación de la masa.!!!

Prof. Natalia Toubes
Representación de reacciones.
Zn + HCl ZnCl2 + H2
Procedemos a ajustar:Zn +2 HCl ZnCl2 + H2

Prof. Natalia Toubes
Otro ejemplo de representación de reacciones.
CaCO3 CaO + CO2

Prof. Natalia Toubes
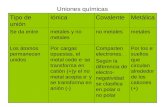
TIPOS DE REACCIONES QUÍMICAS
S ÍN TE S ISD E S C O M P O S IC IÓN
S U S TITU C IÓNIN TE RC AM B IOC O M B U S TIÓN

Prof. Natalia Toubes
REACCIONES DE SÍNTESIS
Varias Sustancias Una SustanciaHidrógeno + Azufre + Oxígeno → Ácido Sulfúrico
H2 + S + O
2→ H
2SO
4

Prof. Natalia Toubes
2Na (s) + Cl2 (g) 2 NaCl (s)
+

Prof. Natalia Toubes
REACCIONES DE DESCOMPOSICIÓN
Una Sustancia Varias Sustancias
Clorato de potasio → Cloruro de potasio + oxígeno
K ClO3 → K Cl + O
2

Prof. Natalia Toubes
Estas reacciones son opuestas a las reacciones de síntesis y por lo general Un ejemplo que se usa en los Airbags
NH4NO3(s) N2O (g) + 2H2O (l)

Prof. Natalia Toubes
REACCIONES DE SUSTITUCIÓN
AB + C AC + BCloruro de Hidrógeno + Zinc → Cloruro de Zinc + Hidrógeno
H Cl + Zn → ZnCl2 + H
2

Prof. Natalia Toubes
los átomos de un elemento sustituyen o reemplazan los átomos de otro en un
compuesto.
Mg (s) + Cu2SO4 (s) MgSO4(s) + Cu (s)
+ +

Prof. Natalia Toubes
REACCIONES DE INTERCAMBIO
AB + CD AD + BCCloruro de Sodio + Nitrato de Plata → Nitrato de Sodio + Cloruro de Plata
Na Cl + AgNO3 → NaNO
3 + AgCl

Prof. Natalia Toubes

Prof. Natalia Toubes
REACCIONES DE COMBUSTIÓN
COMBUSTIBLE + OXÍGENO → DIÓXIDO DE CARBONO + AGUA
CH4 + O
2 → CO
2 + H
2O
COMBUSTIÓN DEL GAS METANO

Prof. Natalia Toubes

Prof. Natalia Toubes
Reacción de COMBUSTIÓN.Siempre los productos son dióxido de carbono gaseoso,
vapor de agua y energía (en forma de luz, calor, etc)
EtanolCarbónButano
Propano + O2 CO2 +H2O+ EnergíaGasolinaMaderaPlásticos…………

Prof. Natalia Toubes
¿Como ajustar una reacción de combustión?
C2H6 + O2 CO2 + H2O
1º.-Ajustamos los átomos de hidrógeno. Ponemos el coeficiente estequiométrico a la molécula de agua, para ajustar estos.
C2H6 + O2 CO2 +3 H2O

Prof. Natalia Toubes
¿Como ajustar una reacción de combustión?
2º.-Ajustamos los átomos de carbono. Ponemos el coeficiente estequiométrico a la molécula de dióxido de carbono, para ajustar estos.
C2H6 + O2 2CO2 +3 H2O

Prof. Natalia Toubes
¿Como ajustar una reacción de combustión?
3º.-Ajustamos los átomos de oxigeno. Ponemos el coeficiente estequiométrico a la molécula de oxígeno, para ajustar estos.
C2H6 + 7/2 O2 2CO2 +3 H2O
• !!ojo!!.Frecuentemente aparecen coeficientes fraccionarios.

Prof. Natalia Toubes
Ajuste y representación de la reacción
C2H6 + 7/2 O2 2CO2 +3 H2O
Para poder representarla ,eliminamos el coeficiente fraccionario, multiplicando por dos la ecuación:
2 C2H6 + 7 O2 4CO2 +6H2O
+ +

Prof. Natalia Toubes
Energía de las reacciones
• Durante el curso de una reacción siempre se produce ,en mayor o menor medida ,un desprendimiento o una absorción de energía.
• Así clasificamos las reacciones en:1.-EXOTÉRMICAS: Aquellas en las que se
desprende calor.Aunque en un principio haya que suministrar una mínima cantidad de calor.
2.-ENDOTÉRMICAS: Son aquellas en las que se absorbe calor.