RELEVAMIENTO DE LA BIODIVERSIDAD COSTERA€¦ · Arroyo la Caballada Arroyo Pando Laguna José...
Transcript of RELEVAMIENTO DE LA BIODIVERSIDAD COSTERA€¦ · Arroyo la Caballada Arroyo Pando Laguna José...

1

2
RELEVAMIENTO DE LA BIODIVERSIDAD COSTERADE URUGUAY: INVERTEBRADOS BENTÓNICOS Y
PECES
RESUMEN
Dentro de la provincia biogeográfica “Atlántico Sudoccidental templada-cálida”, laecoregión “Plataforma Uruguay-Buenos Aires” fue catalogada como de alta prioridad entérminos de conservación (Sealey & Bustamante, 1999). La evaluación del estado deconocimiento de la biodiversidad costera de Uruguay, muestra vacíos de información.El objetivo de este proyecto es describir la distribución espacial en términos depresencia y ausencia, de las principales especies de la zona intermareal rocosa y delas especies estuarinas del macrobentos y peces de la costa uruguaya entre losdepartamentos de Colonia y Rocha. Para realizar los muestreos se definieron tresregiones de la costa Uruguaya: Río de la Plata, de Colonia a Montevideo, Ecotonoestuarial, de Montevideo a Punta del Este y Zona oceánica Atlántica, de Punta del Esteal Chuy. En cada región se muestrearon tres puntas rocosas y tres desembocadurasde ríos, arroyos o lagunas.
Para las puntas rocosas se encontraron un total de 67 especies y la mayorriqueza específica se encontró en la región oceánica Atlántica y la menor riqueza en laregión Río de la Plata encontrándose una correlación positiva de la riqueza con lasalinidad. En cada una de las regiones se encontraron especies exclusivas. Sediscuten las regiones encontradas luego de analizados los datos con las regionesdefinidas a priori al comienzo de este proyecto.
Para los invertebrados de los sistemas estuarinos se encontraron un total de 36especies y la mayor riqueza específica se encontró en la región del ecotono que incluyePando, Solis y Maldonado, y en la región oceánica. Ocho especies fueron exclusivasde la región Ecotono estuarial y cinco exclusivas de la región oceánica. Se compara lariqueza específica encontrada en los sistemas estuarinos con la encontrada en laspuntas rocosas.
Para los peces, se encontraron un total de 20 especies diferentes entre lascuales algunas se caracterizan por frecuentar ambientes estuarino-marinos y otras porhabitar sitios de agua dulce. La especie mas abundante fue P. platana con 367individuos. La riqueza específica mayor se encontró en la zona del Río de la Plata. Nose observó una relación clara entre la diversidad o la equitatividad y la salinidad de lossitios de estudio. El análisis factorial de correspondencias determinó dos grupos elprimero constituido por los ambientes de agua dulce y el segundo grupocorrespondientes al ecotono y costa Atlántica. Se discuten las distribuciones de tallasde las especies encontradas y el número de especies en relación a la zona demuestreo.

3
RELEVAMIENTO DE LA BIODIVERSIDAD COSTERADE URUGUAY: INVERTEBRADOS BENTÓNICOS Y
PECES
1. INTRODUCCIONLos ambientes marinos ocupan las tres cuartas partes de la superficie de la
Tierra. En la actualidad, conjuntamente con el reconocimiento del extraordinario valor
de estos ambientes, se ha comenzado a percibir su fragilidad ante la creciente presión
antrópica impuesta por el desarrollo económico. De tal forma, se ha llegado a un
consenso respecto a la imperiosa necesidad de conservar la integridad ecológica de los
sistemas marinos, de tal manera de preservar los valiosos servicios que éstos otorgan
a la humanidad, tales como recursos pesqueros, productos farmacéuticos, recreación,
turismo, etc. (Meffe & Carroll, 1997., Sealey & Bustamante, 1999).
Dentro de la provincia biogeográfica “Atlántico Sudoccidental templada-cálida”, la
ecoregión “Plataforma Uruguay-Buenos Aires” (34°- 41° S) se caracteriza por su alta
productividad, por albergar abundantes poblaciones de peces, y numerosas colonias de
mamíferos marinos y aves (Sealey & Bustamante, 1999). La polución generada por
industrias y descarga de petróleo, conjuntamente con la pesquería de peces y
moluscos, gran desarrollo urbanístico costero e intenso turismo, han determinado que
esta ecoregión haya sido catalogada dentro de América del Sur como zona de alta
prioridad en términos de conservación (Sealey & Bustamante, 1999). Sin embargo, en
el caso de Uruguay, aún no se ha implementado ningún sistema de protección de la
biodiversidad costera.
Estado del conocimiento de la biodiversidad costera de UruguayLa evaluación del estado de conocimiento de la biodiversidad costera de
Uruguay, muestra claramente la existencia de varios vacíos de información, tanto
relacionados con algunos grupos taxonómicos en particular (e.g., invertebrados de
fondos rocosos, peces y aves), como con tópicos de estudio (e.g., distribución
geográfica de biodiversidad, endemismos). La carencia de información limita

4
enormemente la capacidad de manejar y conservar la biodiversidad costera de
Uruguay.
El objetivo de este proyecto es describir la distribución espacial en términos de
presencia y ausencia, de las principales especies de la zona intermareal rocosa y de
las especies estuarinas del macrobentos y peces de la costa Uruguaya entre los
departamentos de Colonia y Rocha.
2. MATERIALES Y METODOS2.1. Sitios de estudio
En este muestreo, con fines prácticos, se definieron 3 regiones de la costa
Uruguaya: (1) Río del la Plata, de Colonia a Montevideo, (2) Ecotono estuarial, de
Montevideo a Punta del Este y (3) Zona oceánica Atlántica, de Punta del Este al Chuy.
En cada región se muestrearon 3 puntas rocosas y 3 desembocaduras de ríos, arroyos
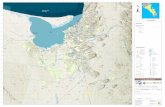
o lagunas (Tabla 1 y Fig.1).
Tabla 1. Lista de sitios de colecta de organismos bentónicos y peces en desembocaduras de arroyos ríos
o lagunas costeras y de organismos intermareales en puntas rocosas.
Río de la Plata Ecotono AtlánticoPuntas Rocosas
Colonia Atlántida Punta José Ignacio
Punta del Rosario Punta Colorada La Pedrera
Punta Espinillo Punta Ballena Santa Teresa
Desembocaduras
Arroyo la Caballada Arroyo Pando Laguna José Ignacio(*)
Río Rosario Arroyo Solís Grande Laguna Garzón
Río Santa Lucía Arroyo Maldonado Laguna de Rocha
Arroyo Valizas(*) Este sitio fue muestreado sólo para la captura de peces.

2.2. Di2.2.1. P
D
en 10 c
propues
grupos
infralito
todas la
la costa
con un
ARGENTINA
Figura 1. Mapa de la región indicando l
seño de muestreountas Rocosas
entro de cada sitio se realizaron
uadrantes (0.1m2) distribuidos en
tas por Stephenson & Stephenso
de organismos: franja supralitoral
ral (mejillones). En todas las pu
s condiciones posibles de aislam
. Una vez colocado el cuadrante
raspador y una espátula, de modo
Figura 2. Punta José Ignacio,
= puntas rocosas = sistemas estuariales
URUGUAY
5
os puntos de muestreo en la costa Uruguaya.
3 transectos en los que se tomaron muestras
las tres zonas típicas del intermareal rocoso
n (1949) en base a la distribución de ciertos
(líquenes), zona mesolitoral (balanos) y franja
ntas rocosas muestreadas se trato de cubrir
iento, exposición y complejidad de hábitats de
sobre la roca, los individuos fueron colectados
de dejar la roca vacía.
departamento de Maldonado.

6
En las figuras 2 y 3 se muestran dos de los sitios en los cuales se realizó la
colecta de material. El material extraído, fue fijado en formol al 8% y llevado al
laboratorio para su análisis. Todos los individuos fueron identificados al nivel
taxonómico mas bajo posible; en muchos casos fueron identificados a nivel de
especies. Para esto se utilizaron claves dicotómicas para poliquetos (Nonato & Amaral,
1979), moluscos (Rios, 1994) y anfípodos (Escofet, 1973). La identificación de los
crustáceos fue realizada con la colaboración de Msc. Ana Verdi. Para la clasificación
de las algas se utilizó la clave de Gabrielson et. al. (2000). Dado que esta clave fue
diseñada para el hemisferio norte, se constató que los géneros encontrados estuvieran
citados también para el hemisferio sur, en particular en nuestra costa (Coll & Oliveira,
1999).
Análisis de DatosSe realizó un análisis factorial de correspondencias (AFC), utilizando la matriz de
presencia ausencia de especies en los nueve sitios muestreados. Este método permite
la representación espacial, simultáneamente, de los sitios y las especies. Se ajustó
una regresión lineal entre la riqueza de especies y la salinidad, utilizando la salinidad
como variable independiente.
2.2.2. Sistemas Estuarinos
A continuación se presenta una breve descripción de los sitios de muestreo.
Figura 3. Punta Santa Teresa, departamento de Rocha.

7
ARROYO LA CABALLADAEste curso de agua se ubica en el departamento de Colonia, desembocando en el Río de laPlata al este de la ciudad de Colonia del Sacramento. En la desembocadura del mismo seEncuentra un extenso bañado.
Figura 4- Arroyo La Caballada (Vista aérea de la desembocadura)Fuente: DINAMA
Figura 5- Arroyo La Caballada. Vista del sitio de muestreo.

8
Figura 4- Arroyo La Caballada (Vista aérea de la desembocadura)Fuente: DINAMA
Figura 5- Arroyo La Cabalada. Vista del sitio de muestreo.
RIO ROSARIOEl Río Rosario desemboca en el departamento de Colonia, en aguas del Río de la Plata. Cercade su desembocadura recibe aguas de efluentes industriales.
Figura 6- Río Rosario (Vista aérea de la desembocadura)Fuente: DINAMA
Figura 7- Río Rosario. Vista del sitio de muestreo.

9
RIO SANTA LUCIAEste río se ubica en el límite entre los departamentos de San José y Montevideo,desembocando en el Río de la Plata. En su desembocadura predomina el ecosistema debañados.
Figura 8-Río Santa Lucía (Vista aérea de la desembocadura)Fuente: IMM
Figura 9- Río Santa Lucía. Vista del sitio de muestreo.

10
ARROYO PANDOUbicado en el departamento de Canelones, este arroyo desemboca en el Río de laPlata. Su desembocadura está dominada por sedimento arenoso, predominando enesta área el proceso de erosión debido a la presión antrópica sobre el sistema.
Figura 10- Arroyo Pando (Vista aérea de la desembocadura)Fuente: DINAMA
Figura 11- Arroyo Pando. Vista del sitio de muestreo.

11
ARROYO SOLIS GRANDEEste arroyo se encuentra en el límite entre los departamentos de Canelones yMaldonado. Su desembocadura se abre sobre el Río de la Plata, predominando enla zona los sedimentos gruesos.
Figura 12- Arroyo Solís Grande (Vista aérea de la desembocadura)Fuente: DINAMA
Figura 13- Arroyo Solís Grande. Vista del sitio de muestreo.

12
ARROYO MALDONADOUbicado en el departamento de Maldonado, este arroyo desemboca en el Océano Atlántico,próximo a la ciudad de Punta del Este
Figura 14- Arroyo Maldonado (Vista aérea de la desembocadura)Fuente: DINAMA
Figura 15- Arroyo Maldonado. Vista del sitio de muestreo.

13
LAGUNA GARZONEsta laguna se encuentra al este del departamento de Maldonado, en el límite con eldepartamento de Rocha. Cuando su barra está abierta se comunica con el Océano Atlántico.
Figura 16- Laguna Garzón (Vista aérea de la desembocadura)Fuente: DINAMA
Figura 17- Laguna Garzón. Vista del sitio de muestreo.

14
LAGUNA DE ROCHAUbicada en el departamento de Rocha, esta laguna se comunica con el Océano Atlánticocuando su barra se abre, fenómeno dependiente del balance entre el aporte fluvial y lascondiciones hidrodinámicas costeras.
Figura 18- Barra de la Laguna de Rocha (abierta). Julio 1999.Fuente: DINAMA
Figura 19- Barra de la Laguna de Rocha (cerrada).Enero 2000. Fuente: DINAMA
Figura 20- Laguna de Rocha. Vista del sitio de muestreo.

ARROYO VALIZASUbicado en el departamento de Rocha, este arroyo desemboca en el OcéanoAtlántico. En su desembocadura existe un sistema de dunas costeras. La barrapuede cerrarse dependiendo del balance entre los aportes hídricos y la dinámicacostera
15
Figura 21- Arroyo Valizas (Vista aérea de la desembocadura)Fuente: DINAMA
Figura 22- Arroyo Valizas. Vista del sitio de muestreo.

16
2.2.2.1. Invertebrados
En cada sitio se realizaron 4 transectos con tres estaciones en la zonas
supralitoral, mesolitoral e infralitoral. El menor número de muestras tomados en fondos
blandos se debe a el mayor esfuerzo requerido para tamizar las muestras y separar los
organismos del sedimento. Los organismos de la infauna se colectaron con un corer
de 16 cm de diámetro y los de la epifauna por medio de una trampa de caída de 0.5 m2
de superficie.
La trampa de caída consiste en una caja de aluminio de 70 cm de ancho, alto y
largo, sin tapa ni fondo, que cuelga de una varilla de madera de 4 m de largo sostenida
por dos personas ubicadas en sus extremos (Fig.23). Una vez definido el sitio de
muestreo, se deja caer la varilla y así la trampa, de forma que ésta se entierra algunos
centímetros en el sedimento y al mismo tiempo sobresale del agua. La porción de
agua así también como los primeros centímetros de sedimento aislados por la trampa
fueron tamizados reiteradamente usando calderines de 2 mm de malla, con el fin de
capturar organismos de la epifauna poco móviles (e.g cangrejos, camarones).
Figura 23. Trampa de caída utilizada en el presente estudio para el
muestreo de los organismos epifaunales.
El material extraído fue procesado utilizando la metodología descrita para puntas
rocosas. La identificación de los organismos fue hecha al nivel taxonómico mas bajo
posible; en muchos casos fueron identificados a nivel de especies. Para esto se
utilizaron las claves dicotómicas antes mencionadas para las puntas rocosas.

17
Análisis de DatosSe realizó un análisis factorial de correspondencias (AFC), utilizando la matriz de
presencia ausencia de especies en los nueve sitios muestreados. Se ajustó una
regresión lineal entre la riqueza de especies y la salinidad, utilizando la salinidad como
variable independiente.
2.2.2.2. Peces
Una vez definido el sitio de muestreo se procedió a realizar los arrastres de
pesca. El arte utilizado consistió en una red de arrastre de playa tipo “picaré” de 12
metros de longitud con copo de 3 metros. La distancia entre nudos fue de 1 cm, en la
parte inferior contenía una cadena con pequeñas plomadas para optimizar el contacto
con el fondo en el momento del arrastre y en la superior presentaba pequeñas bollas
para aumentar su flotabilidad. En cada sitio de muestreo se realizaron arrastres
paralelos a la línea de costa. Estos eran hechos manualmente por dos muestreadores
y comenzaban al caer la tarde y por la noche, o comenzaban en la noche y se
extendían hasta la madrugada. La duración de cada lance era de aproximadamente 10
minutos. Una vez realizado el arrastre se procedió a almacenar las muestras en bolsas
de nylon con su respectiva identificación separadas por lance.
El material extraído en los muestreos, se congeló y se llevó al laboratorio para su
análisis. Todos los individuos fueron identificados al nivel taxonómico de especie con
la excepción de 2 grupos; “lisa” y “mojarra” que se llegó solo a género. En el caso de la
lisa (Mugil sp) se citan para la región Mugil platanus y Mugil liza (Menezes, 1983)
aunque en estos momentos estas especies están en revisión pues al parecer estaría
presente solo una de ellas (González-Castro & Couseau, com. pers.). En el caso de la
mojarra la identificación de la especie se dificultó porque los caracteres encontrados se
corresponden con los de más de una especie.
Para la identificación de la familia Atherinidae se utilizaron las claves de
(Bemvenuti, 2002); para la familia Characidae (Ringuelet et al.,1967; Braga, 1994);
para Clupeidae (Cione et al.,1998; Cousseau & Perrotta, 2000); para Curimatidae
(Azpelicueta & Braga, 1991); para Engraulidae (Ringuelet et al.,1967); para Loricáridae
(López, 1992); para Mugilidae (Menezes, 1983); para Paralichthyidae (Fabre & Días de

18
Astarloa, 1996); para Pimelodidae (Ringuelet et al.,1967); para Poeciliidae (Ringuelet et
al.,1967) Prochilodontidae (Ringuelet et al.,1967); para Scienidae (Ringuelet et
al.,1967; Cousseau & Perrotta, 2000).
Análisis de DatosSe analizó la estructura de tallas de cada especie que contó con 30 individuos
como mínimo en la muestra general. Las clases de longitud se definieron de acuerdo a
las tallas mínimas y máximas de cada especie. Para todas las especies capturadas se
construyó una tabla que presenta para cada especie: su sitio de captura, su
abundancia (Nº de individuos) y los estadísticos básicos para la talla. Se calculó para
cada sitio la riqueza especifica (Nº de especies), la varianza de la abundancia de las
especies (logaritmizada en base e), el índice de diversidad de Shannon – Weiner (H;
log2) y su equitatividad (J).
Se realizó un análisis factorial de correspondencias (AFC; programa
STATISTICA 99), utilizando la matriz de presencia ausencia de especies en los diez
sitios muestreados. Este método permite la representación espacial, simultáneamente,
de los sitios y las especies (Cuadras & Fortiana, 1998). Se calculo el índice de
distancia de Ochiai a partir de la matríz de presencia – ausencia y posteriormente la
matriz de distancias fue analizada por medio del escalado multidimensional (MDS;
programa STATISTICA 99) (Cuadras & Fortiana, 1998). Este índice es una media
geométrica de las co-ocurrencias y permite minimizar los efecto negativo de las
especies poco frecuentes.
3. RESULTADOS3.1. Puntas Rocosas
Se encontró un total de 67 especies comprendidas en 8 Phyla y dos divisiones
de algas (Rodophytas y Chlorophytas). En la tabla 2 se muestra el total de los taxa
hallados. Mollusca fue el único Phylum observado en todos los ambientes rocosos
muestreados.

19
Tabla 2. Lista sistemática de Phyla y especies ocurrentes obtenidas en las puntas rocosas,durante la presente investigación. Se indica en la cuarta columna al grupo que perteneció cadaespecie en el AFC (ver Figuras 26 y 27).
SITIO Phylum Especie GrupoColonia Alga indeterminada 1 1
Mollusca Chilina fluminea 1Heleobia piscium 1Limnoperna fortunei 1
Crustácea Hyalella curbiespina 1Uniramea Baetidae indeterminado 1
Chironomidae indeterminado 3b2Coleoptera indeterminado 1
Rosario Alga indeterminada 2 1Alga indeterminada 3 1Mollusca Asolene megastoma 1
Chilina fluminea 1Heleobia australis 1Heleobia piscium 1Hidrobiidae sp. 1Limnoperna fortunei 1
Crustácea Hyalella curbiespina 1Psephenine 1
Uniramea Baetidae indeterminado 1Chironomidae indeterminado 3b2Coleoptera indeterminado 1
Pta. Espinillo Chlorophyta Enteromorpha sp 4 2Rhodophyta Ceramiacea indeterminada 2Mollusca Limnoperna fortunei 1Crustácea Cyrtograpsus angulatus 3b2
Metasesarma rubripes 2Panopeus meridionalis 3b2Pseudosphaeroma platense 2Sinelobus stanfordi 3b2
Atlántida Chlorophyta Enteromorpha sp.5 3aEnteromorpha sp.6 3b2
Rhodophyta Ceramium sp.7 3aPterocladiella capillacea 3b2
Platyhelminthes Polyclada sp. 3b2Annelida Neanthes succinea 3b2Mollusca Brachidontes darwinianus 3b2
Brachidontes rodriguezi 3b2Mytilus edulis platensis 3b2Siphonaria lessoni 3b2
Crustacea Balanus improvisus 3b2Chtamalus bisinuatus 3b2Cyrtograpsus angulatus 3b2Panopeus meridionalis 3b2Cymadusa filosa 3b2Hyale grandicordis 3b2

20
Tabla 2 (Continuación). Lista sistemática de Phyla y especies ocurrentes obtenidas en laspuntas rocosas, durante la presente investigación. Se indica en la cuarta columna al grupo queperteneció cada especie en el AFC (ver Figuras 26 y 27).
SITIO Phylum Especie GrupoAtlántida Icliidae indeterminado 3a
Tanaidacea indeterminado 3aUniramea Chironomidae indeterminado 3b2Bryozoa Membranipora sp. 3b2
Piriápolis Chlorophyta Ulva lactuca 3b2Enteromorpha sp.6 3b2
Rhodophyta Pterocladiella capillacea 3b2Cnidaria Antozoa sp.1 3b2Platyhelminthes Polyclada sp. 3b2Nemertea 3b2Annelida Neanthes succinea 3b2Mollusca Brachidontes darwinianus 3b2
Brachidontes rodriguezi 3b2Mytilus edulis platensis 3b2Siphonaria lessoni 3b2
Crustacea Balanus improvisus 3b2Chtamalus bisinuatus 3b2Cyrtograpsus angulatus 3b2Panopeus meridionalis 3b2Corophium sp. 3b2Cymadusa filosa 3b2Hyale grandicordis 3b2Idotea balthica 3b2Ligia exotica 3b2
Uniramea Chironomidae indeterminado 3b2Bryozoa Membranipora sp. 3b2
Pta. Ballena Chlorophyta Enteromorpha sp.6 3b2Ulva lactuca 3b2
Rhodophyta Polysiphonia sp.7 3b2Pterocladiella capillacea 3b2
Cnidaria Antozoa sp. 1 3b2Platyhelminthes Polyclada sp. 3b2Annelida Neanthes succinea 3b2Nemertea 3b2Mollusca Brachidontes rodriguezi 3b2
Brachidontes darwinianus 3b2Mytilus edulis platensis 3b2Perna perna 3b2Collisella subrugosa 3b2Siphonaria lessoni 3b2Bivalvia indeterminado 3b2
Crustacea Balanus improvisus 3b2Chtamalus bisinuatus 3b2Cyrtograpsus angulatus 3b2Panopeus meridionalis 3b2Decápoda indeterminado 3b2Corophium sp. 3b2

21
Tabla 2 (Continuación). Lista sistemática de Phyla y especies ocurrentes obtenidas en las puntasrocosas, durante la presente investigación. Se indica en la cuarta columna al grupo queperteneció cada especie en el AFC (ver Figuras 26 y 27).
SITIO Phylum Especie GrupoPta. Ballena Cymadusa filosa 3b2
Hyale grandicordis 3b2Idotea balthica 3b2Sinelobus stanfordi 3b2Ligia exotica 3b2
Uniramea Chironomidae ideterminado 3b2Bryozoa Membranipora sp. 3b2
José Ignacio Chlorophyta Ulva lactuca 3b2Rhodophyta Corallina officinalis 3b2
Cryptopleura sp.8 3b2Polysiphonia sp.7 3b2Pterocladiella capillacea 3b2
Cnidaria Antozoa sp. 1 3b2Platyhelminthes Polyclada sp. 3b2Annelida Chaetacanthus sp. 3b2
Neanthes succinea 3b2Syllidae indeterminado 3b2
Nemertea 3b2Mollusca Brachidontes rodriguezi 3b2
Brachidontes darwinianus 3b2Mytilus edulis platensis 3b2Perna perna 3b2Collisella subrugosa 3b2Siphonaria lessoni 3b2Bivalvia indeterminado 3b2
Crustacea Balanus improvisus 3b2Chtamalus bisinuatus 3b2Cyrtograpsus angulatus 3b2Panopeus meridionalis 3b2Decápoda indeterminado 3b2Caprella sp. 3b2Corophium sp. 3b2Cymadusa filosa 3b2Hyale grandicordis 3b2Idotea balthica 3b2Ligia exotica 3b2
Uniramea Chironomidae ideterminado 3b2Bryozoa Membranipora sp. 3b2
La Pedrera Alga indeterminada 10 3b1Chlorophyta Ulva lactuca 3b2Rhodophyta Ceramium sp.11 3b1
Corallina officinalis 3b2Cryptopleura sp.8 3b2Polysiphonia sp.7 3b2Pterocladiella capillacea 3b2Indeterminada 12 3b1Indeterminada 13 3b1

22
Tabla 2 (Continuación). Lista sistemática de Phyla y especies ocurrentes obtenidas en las puntasrocosas, durante la presente investigación. Se indica en la cuarta columna al grupo queperteneció cada especie en el AFC (ver Figuras 26 y 27).
SITIO Phylum Especie GrupoLa Pedrera Cnidaria Antozoa sp. 2 3b1
Antozoa sp. 3 3b1Nemertea 3b2Annelida Chaetacanthus sp. 3b2
Neanthes succinea 3b2Syllidae indeterminado 3b2
Mollusca Brachidontes rodriguezi 3b2Collisella subrugosa 3b2Littorina ziczac 3b1Mytilus edulis platensis 3b2Perna perna 3b2Siphonaria lessoni 3b2Bivalvia indeterminado 3b2
Crustacea Balanus improvisus 3b2Chtamalus bisinuatus 3b2Pachycheles haigae 3b1Bathyporeiapus sp. 3b1Caprella sp. 3b2Cymadusa filosa 3b2Hyale grandicordis 3b2Idotea balthica 3b2Sinelobus stanfordi 3b2
Uniramea Chironomidae ideterminado 3b2Bryozoa Membranipora sp. 3b2
Sta. Teresa Chlorophyta Enteromorpha sp. 6 3b2Ulva lactuca 3b2Codium sp. 3b1
Rhodophyta Corallina officinalis 3b2Cryptopleura sp.8 3b2Polysiphonia sp.7 3b2Pterocladiella capillacea 3b2Indeterminada 14 3b1Indeterminada 15 3b1Indeterminada 16 3b1
Cnidaria Antozoa sp. 2 3b1Antozoa sp. 3 3b1
Nemertea 3b2Annelida Chaetacanthus sp. 3b2
Neanthes succinea 3b2Syllidae indeterminado 3b2
Mollusca Brachidontes rodriguezi 3b2Collisella subrugosa 3b2Littorina ziczac 3b1Mytilus edulis platensis 3b2Perna perna 3b2Siphonaria lessoni 3b2
Crustacea Chtamalus bisinuatus 3b2

23
Tabla 2 (Continuación). Lista sistemática de Phyla y especies ocurrentes obtenidas en las puntasrocosas, durante la presente investigación. Se indica en la cuarta columna al grupo queperteneció cada especie en el AFC (ver Figuras 26 y 27).
SITIO Phylum Especie GrupoSta. Teresa Pachycheles haigae 3b1
Panopeus meridionalis 3b2Caprella sp. 3b2Corophium sp. 3b2Cymadusa filosa 3b2Hyale grandicordis 3b2Idotea balthica 3b2
Uniramea Chironomidae indeterminado 3b2Bryozoa Membranipora sp. 3b2
La mayor riqueza especifica se encontró en la región oceánica Atlántica, José
Ignacio con 31 especies, La Pedrera con 33 especies y Santa Teresa con 32 especies,
mientras que el menor número de especies fue observado en la región Río de la Plata,
Colonia con 8 especies, Rosario con 13 especies y Punta Espinillo con 8 especies
(Figura 24). La riqueza específica estuvo positivamente correlacionada con la salinidad
de cada sitio (r = 0.97, p<0.05) estableciéndose aproximadamente una relación lineal
(Figura 25). De este modo los sitios con mayor salinidad fueron los que presentaron
mayor riqueza específica.
Figura 24. Variación de la riqueza especifica en las puntas rocosas muestreadas.
0
5
10
15
20
25
30
35
Col
onia
Ros
ario
Pta
Espi
nillo
Atlá
ntid
a
Piria
polis
Pta.
Bal
lena
José
Igna
cio
La P
edre
ra
Sta.
Ter
esa
Sitio
Riq
ueza
de
espe
cies

24
Figura 25. Relación entre la riqueza de especies y la salinidad para los nueve sitios estudiados.
En la región Río de la Plata el mejillón Limnoperna fortunei fue la única especie
exclusiva y común a las tres zonas. Además los moluscos Chilina fluminea y Heleobia
piscium, el crustáceo Hyalella curbiespina y una especie de Baetidae y otra de
Coleoptera ambas indeterminadas, fueron las cinco especies exclusivas de Colonia y
Rosario. En Punta Espinillo ocurrieron cuatro especies exclusivas: los crustáceos
Metasesarma rubripes y Pseudosphaeroma platense y dos especies de algas, una
ceramiácea y otra enteromorpha ambas indeterminadas.
En Atlántida, región ecotono estuarial, ocurrieron cuatro especies exclusivas:
una especie indeterminada de anfípodo, otra especie indeterminada de tanaidáceo, y
dos especies indeterminadas de algas, una del género Enteromorpha y otra del género
Ceramium.
Finalmente, en la región atlántico oceánica, zona con mayor riqueza especifica,
ocurrieron 3 especies exclusivas: Littorina ziczac (moluscos), Pachycheles haigae y
Caprella sp. (crustáceos).
En el análisis factorial de correspondencias (AFC) los tres primeros componentes
obtenidos, basados en la matriz de presencia ausencia de las especies en los nueve
sitios muestreados, dan cuenta de más del 80% de la variación (Figura 26).
Salinidad
Riq
ueza
de
espe
cies
5
10
15
20
25
30
35
-1 3 7 11 15 19 23

25
El primer y segundo eje (Figura 26a) separaron 3 regiones: la primera compuesta por
los sitios ubicados al oeste (Colonia y Rosario), la segunda por Punta Espinillo y la
tercera compuesta por aquellos ubicados en la zona central y este del área de estudio
(Atlántida a Santa Teresa). Los sitios de la zona oeste están caracterizados por las
especies exclusivas de Colonia y Rosario (G.1 en Figura 26a). Punta Espinillo está
también caracterizado por especies exclusivas de este sitio (G.2 en Figura 26a). En los
sitios de la zona central y este dominaron las especies estuarinas y marinas
destacándose entre otras especies Mytilus platensis, Brachidontes rodriguezi
(bivalvos), Siphonaria lessoni (gasterópodo), Cymadusa filosa (anfípodo) Chtamalus
bisinuatus (cirripédio), Panopeus meridionalis (decapodo), Membranipora sp
(briozoario), Neanthes succinea (poliqueto), Pterocladiella capillacea (alga) y larvas de
quironómidos (G.3 en Figura 26a). El primer y tercer eje (Figura 26b) separaron los
grupos anteriormente nombrados y además a Atlántida del resto de los sitios ubicados
al este del área de estudio. Exclusivamente en este sitio se encontraron una especie
indeterminada de anfípodo (subórden Icliidae) y otra especie indeterminada de
tanaidáceo, al igual que dos Rodophytas indeterminadas (G.3a en Figura 26b). El eje 2
y 3 (Figura 26c) separaron Punta espinillo del resto de los sitios.
En el AFC con los sitios del grupo 3 los 3 primeros ejes explicaron un 90% de la
variación (Figura 27). El primer y segundo eje separaron 3 grupos compuestos por
Atlántida (grupo 3a), Santa Teresa y La Pedrera (grupo 3b1) y los 6 sitios restantes
(grupo 3b2). Santa Teresa y La Pedrera se diferenciaron de los otros grupos en
presentar exclusivamente a Brachidontes rodriguezi (bivalvo), Littorina ziczac
(gastropodo) y Caprella sp (anfípodo) y a dos especies de antozoarios indeterminados
(G.3b1 en Figura 27a). El eje 1 y 3 separaron los grupos antes nombrados y además a
Santa Teresa de La Pedrera: en la Pedrera se encontró una especie de Ceramiun
(Rodophyta) no encontrada en otros mientras que Santa Teresa presentó otras
especies no encontradas en la Pedrera (Figura 27b). El eje 2 y 3 separaron a grandes
rasgos los mismos sitios que los ejes anteriores (Figura 27c).

26
Figura 26. Gráficos obtenidos del Análisis Factorial de Correspondencias para los tres primeros ejes.
Símbolos: Col:Colonia; Ros:Rosario; Esp:Pta. Espinillo; Atl:Atlántida; Pir:Piriápolis; Ign:José
Ignacio;Ball:Pta. Ballena; Ped:La Pedrera; Ter: Sta. Teresa. Por referencias de las especies ver en la
tabla 2.

27
Figura 27. Gráficos obtenidos del Análisis Factorial de Correspondencias para los tres primeros ejes.
Símbolos: Col:Colonia; Ros:Rosario; Esp:Pta. Espinillo; Atl:Atlántida; Pir:Piriápolis; Ign:José
Ignacio;Ball:Pta. Ballena; Ped:La Pedrera; Ter: Sta. Teresa. Por referencias de las especies ver en la
tabla 2.

28
3.2. Sistemas Estuarinos3.2.1. Invertebrados
Se encontraron un total de 36 especies, 22 pertenecientes a tres Phyla en las
muestras de infauna y 32 pertenecientes a 5 Phyla en las de epifauna. Cabe señalar
que 18 especies aparecieron tanto en las muestras de infauna como en las de epifauna
(Tabla 3). En el caso de la infauna, los tres Phyla Annelida, Mollusca y Artropoda
estuvieron presentes en todos los sitios excepto en “La Caballada”, en donde solo se
encontró el primero. Para las muestras de epifauna, Annelida y Arthropoda ocurrieron
en todos los sitios, Mollusca se encontró en todos los sitios excepto en el arroyo
Maldonado, Chordata sólo fue encontrado en los Arroyos La Caballada, Pando y Solís
y Bryozoa solo se presentó en la Laguna de Rocha.
En general la mayor riqueza especifica se encontró en la región del ecotono
(Figura 28a), que incluye Pando, Solís y Maldonado, y en la región oceánica (Lag.
Garzón, Lag. de Rocha, Valizas), mientras que el menor número de especies fue
observado en la región Río de la Plata (Caballada, Rosario y Santa Lucía). Este patrón
se cumple también al considerar solo la infauna, o sólo la epifauna (Figuras 28b y 28c).
La riqueza específica no mostró una correlación clara con la salinidad de cada sitio
(Figura 29).
En la región Río de la Plata, Corbicula fluminea, Astyanax sp. (mojarra) y una
especie de Chinche fueron exclusivas de la región. Ninguna especie fue común a los
tres sitios ya que no se encontraron organismos en las muestras de Rosario. La
Chinche solo fue encontrada en la Caballada.
Ocho especies fueron exclusivas de la región Ecotono Estuarial: Neanthes
succinea, Tagelus plebeius, Excirolana armata, un anfípodo, un tanaidáceo y un
díptero Indeterminados, Mugil sp. y una larva de pez no identificada. A su vez Tagelus
plebeius, el tanaidáceo, el díptero y la larva de pez fueron encontrados exclusivamente
en el arroyo Solís, mientras que Neanthes succinea y el anfípodo fueron exclusivos del
Arroyo Maldonado.

29
Tabla 3. Lista sistemática de Phyla y especies ocurrentes obtenidas en los Estuarios. Se indica en la cuartacolumna al grupo que perteneció cada especie en el AFC (ver Figura 30).
SITIO Phylum Especie Inf Epi GrupoLa caballada Annelida Heteromastus similis X X G3
Nephtys fluviatilis X X G3Arthopoda Amphipoda sp. 1 X X G3
Chinche X G3Chordata Astyanax sp. X G3Mollusca Corbicula fluminea X X G1
Santa Lucía Annelida Heteromastus similis X X G3Laeonereis cuvieri X X G3Nephtys fluviatilis X X G3Polichaeta sp. 1 X G3Hyrudinea sp. 1 X X G4
Artrhopoda Balanus improvisus X X G3Camarón X G3Cyrtograpsus angulatus X X G3Dies fluminensis X X G3Pseudosphaeroma platense X X G3Tanaidacea sp. 2 X X G3
Mollusca Corbicula fluminea X X G1Erodona mactroides X X G3Heleobia spp. X X G3
Pando Annelida Heteromastus similis X X G3Laeonereis cuvieri X X G3Polychaeta sp. 1 X G3
Artrhopoda Amphipoda sp. 1 X X G3Chasmagnatus granulata X G3Cyrtograpsus angulatus X X G3Neomysis americana X X G2
Chordata Mugil sp. X G3Mollusca Erodona mactroides X X G3
Heleobia spp. X X G3Planorbis sp. 1 X G4
Solís Annelida Heteromastus similis X X G3Laeonereis cuvieri X X G3Nephtys fluviatilis X X G3
Artrhopoda Balanus improvisus X X G3Chasmagnatus granulata X G3Cyrtograpsus angulatus X X G3Embriones X G3Diptera sp. 1 X G3Excirolana armata X X G2Neomysis americana X X G2Tanaidacea sp. 1 X X G2
Chordata Mugil sp. X G3Pez sp. 2 X G3
Mollusca Erodona mactroides X X G3Heleobia spp. X X G3Tagelus plebeius X G3

30
Tabla 3 (Continuación). Lista sistemática de Phyla y especies ocurrentes obtenidas en los Estuarios. Seindica en la cuarta columna al grupo que perteneció cada especie en el AFC (ver Figura 30).
SITIO Phylum Especie Inf Epi GrupoMaldonado Annelida Heteromastus similis X X G3
Laeonereis cuvieri X X G3Neanthes succinea X G3Nephtys fluviatilis X X G3
Artrhopoda Amphipoda sp. 1 X X G3Amphipoda sp. 2 X G3Amphipoda sp. 3 X G3Balanus improvisus X X G3Chasmagnatus granulata X G3Cyrtograpsus angulatus X X G3Dies fluminensis X X G3Excirolana armata X X G2Pseudosphaeroma platense X X G3Tanaidacea sp. 2 X X G3Quironomidae sp. X X G4
Mollusca Heleobia spp. X X G3Garzón Annelida Heteromastus similis X X G3
Laeonereis cuvieri X X G3Nephtys fluviatilis X X G3Polychaeta sp. 1 X G3
Artrhopoda Amphipoda sp. 1 X X G3Amphipoda sp. 2 X G3Balanus improvisus X X G3Camarón X G3Calinectes sapidus X G4Cyrtograpsus angulatus X X G3Dies fluminensis X X G3Pseudosphaeroma platense X X G3Ostrácoda sp. X G3Tanaidacea sp. 2 X X G3
Mollusca Erodona mactroides X X G3Heleobia spp. X X G3
Rocha Annelida Heteromastus similis X X G3Laeonereis cuvieri X X G3Nephtys fluviatilis X X G3
Artrhopoda Amphipoda sp. 1 X X G3Balanus improvisus X X G3Cyrtograpsus angulatus X X G3Dies fluminensis X X G3Neomysis americana X X G2Pseudosphaeroma platense X X G3Ostrácoda sp. X G3Tanaidacea sp. 2 X X G3
Bryozoa Membranipora sp. X G3Mollusca Brachydontes spp. X X G3
Erodona mactroides X X G3Heleobia spp. X X G3

31
Tabla 3 (Continuación). Lista sistemática de Phyla y especies ocurrentes obtenidas en los Estuarios. Seindica en la cuarta columna al grupo que perteneció cada especie en el AFC (ver Figura 30).
SITIO Phylum Especie Inf Epi GrupoValizas Annelida Heteromastus similis X X G3
Laeonereis cuvieri X X G3Nephtys fluviatilis X X G3Sylidae sp. X G3Hyrudinea sp.1 X X G4
Artrhopoda Amphipoda sp. 1 X X G3Calinectes sapidus X G4Pseudosphaeroma platense X X G3Quironomidae sp. X X G4
Mollusca Brachidontes spp. X X G3Heleobia spp. X X G3Planorbis sp. X G4
Por último, se hallaron exclusivamente en la región oceánica Membranipora sp.,
Calinectes sapidus, Brachidontes spp., un poliqueto de la familia Sylidae y un ostrácodo
indeterminado. Membranipora sp. fue exclusiva de la laguna de Rocha, mientras que el
poliqueto Sylidae lo fue del Arroyo Valizas.
En el análisis factorial de correspondencias (AFC) los tres primeros
componentes obtenidos, basados en la matriz de presencia-ausencia de las especies
en los nueve sitios muestreados, dan cuenta de más del 72% de la variación en el caso
de la infauna, un 70 % en la epifauna y un 60 % si se consideran todos los datos juntos.
En los análisis para la infauna, el primer y el segundo eje permiten distinguir tres
grupos: por un lado el Arroyo Solís Grande, caracterizado por la presencia de E. armata
y el Tanaidáceo sp1, por otro el Arroyo Pando, caracterizado por la presencia de
Neomysis americana y un tercer grupo que reúne el resto de los sitios (Figura 30a).
Los ejes 1 y 3 diferencian básicamente los mismos grupos (Figura 30b), mientras que
los ejes 2 y 3 agrupan Los Arroyos Solís Grande y Pando por un lado y el resto de los
sitios por otro (Figura 30c). En los análisis de epifauna, los ejes 1 y 2 también permiten
separar tres grupos: el Arroyo Valizas, caracterizado por Planorbis sp., Hirudíneos e
Insectos, el Arroyo La Caballada, caracterizado por Corbicula fluminea y el resto de los
sitios (Figura 31a). Los ejes 1 y 3 separan también el Arroyo Valizas, pero agrupan el
Arroyo La Caballada con el Río Santa Lucía, permaneciendo agrupados el resto de los
sitios (Figura 31b). Finalmente los ejes 2 y 3 separan el Arroyo La Caballada de los
demás sitios (Figura 31c). Si se consideran todos los datos de epifauna e infauna en
un solo análisis, los ejes 1 y 2 separan tres grupos: Arroyos La Caballada y Valizas por

32
un lado, el Arroyo Solís Grande por otro y un tercer grupo que incluye el resto de los
sitios (Figura 32a). Los ejes 1 y 3 separan los Arroyos La Caballada y Valizas,
manteniendo los otros dos grupos (Figura 32a). Los ejes 2 y 3 separan el Arroyo la
Caballada de los demás sitios (Figura 32c).
Figura 28 Variación de la riqueza específica en los sistemas estuariales muestreados(a = todos los datos; b = Infauna; c = epifauna)
c
02468
10121416
Cab
alla
da
Ros
ario
S. L
ucía
Pand
o
Solís
Mal
dona
do
Roc
ha
Gar
zón
Valiz
as
Sitio
Riq
ueza
de
espe
cies
b
0
2
4
6
8
10
12
Cab
alla
da
Ros
ario
S. L
ucía
Pand
o
Solís
Mal
dona
do
Roc
ha
Gar
zón
Valiz
as
Sitio
Riq
ueza
de
espe
cies
a
02468
1012141618
Cab
alla
da
Ros
ario
S. L
ucía
Pand
o
Solís
Mal
dona
do
Roc
ha
Gar
zón
Valiz
as
Sitio
Riq
ueza
de
espe
cies

33
Figura 29. Relación entre la riqueza específica y la salinidad de los sitios estudiados(a = salinidad en los estuarios; b = salinidad de las zonas rocosas adyacentes)
0
5
10
15
20
0 5 10 15 20 25
Salinidad
Riqu
eza
espe
cífic
a
0
5
10
15
20
0 5 10 15 20
Salinidad
Riqu
eza
espe
cífic
a
a
b

34
Eje 1 (VP=0,35301; I=27,02%)
Eje
2 (V
P=0,
2982
7; I=
22,8
3%)
-1
0
1
2
-2 -1 0 1 2
ValizasPando
S. Lucía
MaldonadoRocha
Caballada
Garzón
Solí
Eje 1 (VP=0,35301; I=27,02%)
Eje
3 (V
P=0,
2754
1; I=
21,0
8%)
-1
0
1
-2 -1 0 1 2
Valizas
Maldonado
Pando Solí
Caballada
S. LucíaGarzón
Rocha
Eje 2 (VP=0,29827; I=22,83%)
Eje
3 (V
P=0,
2754
1; I=
21,0
8%)
-1
0
1
-1 0 1 2
Pando
Solí
RochaMaldonado
S. Lucía
Garzón
Valizas
Caballada
Figura 31. Gráficos obtenidos del análisis factorial de correspondencias de los datos deepifauna para los tres primeros ejes.(a = eje 1vs. eje 2; b = eje 1 vs. eje 3; c = eje 2 vs. eje 3)

35
Eje 1 (VP=0,26001; I=22,31%)
Eje
2 (V
P=0,
2166
3; I=
18,5
9%)
-2
-1
0
1
2
-2 -1 0 1 2
Eje 1 (VP=0,26001; I=22,31%)
Eje
3 (V
P=0,
2120
3; I=
18,1
9%)
-2
-1
0
1
2
-2 -1 0 1 2
Valizas
Caballada
Solí
Maldonado
S. Lucía
Garzón
Pando
Rocha
Eje 2 (VP=0,21663; I=18,59%)
Eje
3 (V
P=0,
2120
3; I=
18,1
9%)
-2
-1
0
1
2
-2 -1 0 1 2
MaldonadoValizas
Caballada
PandoSolíGarzón
S. Lucía
Rocha
Figura 32. Gráficos obtenidos del análisis factorial de correspondencias de los datos deinfauna y epifauna para los tres primeros ejes. Por referencia ver la tabla 3(a = eje 1vs. eje 2; b = eje 1 vs. eje 3; c = eje 2 vs. eje 3)

36
3.2.2. Peces
Se encontraron un total de 20 especies diferentes de peces correspondientes a
12 familias, entre las cuales algunas se caracterizan por frecuentar ambientes
estuarinos-marinos y otras por habitar sitios de agua dulce. En la tabla 4 se muestra el
total de los táxones hallados destacándose la lisa (Mugil sp.) y el lenguado
(Paralichthys orbignyanus) los cuales estuvieron representados en 7 y 6 sitios
respectivamente.
Tabla 4. Lista de las especies de peces capturadas agrupadas por familia, con sus correspondientesnombres científicos y comunes.
Familia Especie Nombre comúnAtherinidae Odontesthes bonariensis (Valenciennes, 1835) PejerreyAtherinidae Odontesthes argentinensis (Valenciennes, 1835) PejerreyCharacidae Astyanax sp. (Baird y Girard, 1854) MojarraCharacidae Oligosarcus oligolepis (Steindachner, 1867) DientudoClupeidae Platanichthys platana (Regan, 1917) MandufiaClupeidae Brevoortia aurea (Agassiz, 1829) LachaCurimatidae Cyphocharax platanus (Günther, 1880) SábalitoCurimatidae Cyphocharax voga (Hensel, 1870) SábalitoEngraulidae Lycengraulis grossidens (Agassiz, 1829) Anchoa de RíoLoricariidae Hypostomus commersoni (Valenciennes, 1840) Vieja de aguaMugilidae Mugil sp. (Linné, 1758) LisaParalichthyidae Paralichthys orbignyanus (Valenciennes, 1839) LenguadoPimelodidae Pimelodus clarias (Lacépede, 1803) Bagre manchadoPimelodidae Iheringichthys platanus (Steindachner, 1908) Bagre trompudoPimelodidae Rhamdia quelen (Quoy y Gaimard, 1824) Bagre sapoPoeciliidae Jenynsia lineata (Jenyns, 1842) Piava u OveritoProchilodontidae Prochilodus lineatus (Valenciennes, 1847) SábaloSciaenidae Micropogonias furnieri (Desmarest, 1823) Corvina blancaSciaenidae Pachyurus bonariensis (Steindachner, 1879) Corvina de RíoSciaenidae Pogonias cromis (Linné, 1766) Corvina negra
DISTRIBUCIONES DE FRECUENCIAS DE LONGITUDES
Los estadísticos básicos de cada especie extraída para la talla (número, media,
mediana, desvío estándar, mínimo y máximo) y por sitio se presentan en la tabla 5. El
intervalo de tallas capturado considerando la totalidad de las especies se encontró
entre 2,2 y 35,0 cm. La especie más abundante fue P. platana con 367 individuos y las
menos abundantes fueron B. aurea, H. commersoni, y P. lineatus con un solo individuo
cada una. La especie que presentó mayor tamaño promedio fue H. commersoni (35,0
cm) y la de menor tamaño promedio fue J. lineata (2,9 cm). La especie que presentó

37
mayor heterogeneidad de tallas fue M. furnieri (DE = 8,8 cm) y la menos heterogénea
fue Astianax sp. (DE = 1,4 cm).
Tabla 5. Estadísticos para la talla (cm) de las especies capturadas por sitio (ALC: Arroyo La Caballada;RR: Río Rosario; RSL: Río Santa Lucia; AP: Arroyo Pando; ASG: Arroyo Solís Grande; AM: ArroyoMaldonado; LJI: Laguna José Ignacio; LG: Laguna Garzón; LR: Laguna de Rocha; AV: Arroyo Valizas) ytotales (sobre fondo gris).
Especie Sitio N Media Mediana DE Mínimo MáximoAstyanax sp. ALC 28 9,4 9,5 1,5 5,9 12,6
RR 6 8,9 9,2 1,3 7,1 10,3RSL 3 10,3 10,3 0,5 9,8 10,7ASG 1 7,6 7,6Total 38 9,4 9,6 1,4 5,9 12,6
Brevoortia aurea AM 1 7,7 7,7
Cyphocharax platanus RR 5 13,8 14 1,7 11,3 15,5
Cyphocharax voga ALC 6 13,6 13,2 1,7 12,0 15,9RR 31 13,9 14,2 1,6 9,8 16,4RSL 39 14,0 14,2 1,6 11,1 16,5LG 1 11,4 11,4
Total 77 13,9 14 1,6 9,8 16,5
Hypostomus commersoni RR 1 35,0 35,0
Iheringichthys platanus ALC 43 11,7 11,4 2,6 7,4 17,0RR 32 8,7 8,6 1,7 6,7 13,5
Total 75 10,4 9,8 2,7 6,7 17,0
Jenynsia lineata RR 1 3,5 3,5LG 1 2,3 2,3
Total 2 2,9 2,9 2,3 3,5
Lycengraulis grossidens RR 24 11,3 10,5 2,5 9,2 20,0AV 1 11,0 11,0
Total 25 11,3 10,5 2,5 9,2 20,0
Micropogonias furnieri AP 8 7,8 7,7 2,0 5,1 11,6ASG 6 8,6 8,8 1,0 6,9 9,7AV 2 33,6 33,6 32,4 34,7
Total 16 11,3 8,4 8,8 5,1 34,7
Mugil sp. AP 20 2,8 2,8 0,1 2,5 3,0ASG 5 17,2 9,6 10,9 8,9 30,5AM 3 9,7 3,0 2,9 23,3LJI 28 3,8 3,0 1,5 2,7 7,5LG 2 10,3 10,3 9,4 11,2LR 4 3,6 2,9 2,7 5,8AV 3 17,4 16,8 13,1 22,3
Total 65 5,6 3,0 6,0 2,5 30,5

38
Tabla 5. Continuación.Odontesthes argentinensis ASG 1 7,6 7,6
AM 6 11,1 12,1 3,8 3,8 14,2LG 18 3,4 3,5 0,9 2,2 5,1LR 2 12,8 12,8 12,5 13,0AV 1 25,2 25,2
Total 28 6,6 3,9 5,5 2,2 25,2
Odontesthes bonariensis RR 2 15,0 15,0 14,2 15,8
Oligosarcus oligolepis ALC 3 14,3 14,4 13,5 15,0RSL 1 17,4 17,4LG 65 13,5 13,2 1,7 11,4 20,3
Total 69 13,6 13,3 1,7 11,4 20,3
Pachyurus bonariensis ALC 1 12,3 12,3RR 1 9,1 9,1
Total 2 10,7 10,7 9,1 12,3
Pogonias cromis AM 2 19,0 19,0 16,5 21,5
Pimelodus clarias ALC 16 12,0 11,4 3,5 7,3 19,4RR 15 11,7 10,4 3,4 7,8 18,0
Total 31 11,8 10,7 3,4 7,3 19,4
Prochilodus lineatus RR 1 34,3 34,3
Paralichthys orbignyanus AP 2 7,6 7,6 7,4 7,8ASG 18 9,1 9,3 1,4 7,0 11,7AM 5 6,7 6,5 0,8 5,7 7,8LG 17 12,2 13,0 3,3 7,0 17,1LR 10 9,0 9,3 1,5 5,9 11,1AV 8 9,7 9,4 2,0 7,7 14,0
Total 60 9,8 9,4 2,7 5,7 17,1
Platanichthys platana LG 366 4,3 2,8 2,6 2,2 9,1AV 1 9,7 9,7
Total 367 4,3 2,8 2,6 2,2 9,7
Rhamdia quelen LG 2 32,0 32,0 29,4 34,5
Las distribuciones de frecuencias de longitudes para las especies que
presentaron un número mayor a 30 individuos se presentan a continuación.

39
Astyanax sp. (Fig. 33) Presentó una distribución de tallas entre 6 y 13 cm, por lo
que se agrupó en clases de talla de un centímetro. El promedio fue de 9,4 cm y esta
distribución fue unimodal con una moda en los 10 cm.
Figura 33. Distribución de tallas para la Mojarra (Astyanax sp.).
Iheringichthys platanus (Fig. 34) Presentó una distribución de tallas entre 7 y 17
cm, agrupado en clases de talla de un centímetro. El promedio fue de 10,4 cm y la
distribución resultante fue en apariencia bimodal con una moda situada en 9 cm y la
otra en 14 cm.
Figura 34. Distribución de tallas para el Bagre trompudo (Iheringichthys platanus).
0
5
10
15
4 5 6 7 8 9 10 11 12 13 14 15
Talla (cm)
Nº
de In
divi
duos
0
5
10
15
20
5 6 7 8 9 10 11 12 13 14 15 16 17 18 19
Talla (c m )
Nº
Ind
ivid
uo
s

40
Cyphocharax voga (Fig. 35) Presentó una distribución de tallas entre 10 y 17 cm,
agrupados en clases de talla de un centímetro. El promedio fue de 13,9 cm y la
distribución fue unimodal con una moda en 15 cm.
Figura 35. Distribución de tallas para el Sábalito (Cyphocharax voga).
Mugil sp (Fig 36.) Presentó una distribución de tallas muy dispersa (situada entre
3 y 31 cm) con una concentración de individuos en las tallas chicas y una moda situada
en 3 cm.
Figura 36. Distribución de tallas para la Lisa (Mugil sp.).
0
5
10
15
20
25
8 9 10 11 12 13 14 15 16 17 18 19
Talla (cm)
Nº
de In
divi
duos
0
10
20
30
40
50
1 3 5 7 9 11 13 15 17 19 21 23 25 27 29 31 33
Talla (cm)
Nº
de In
divi
duos

41
Platanichthys platana (Fig. 37) Presentó una distribución de tallas (con clases de
tallas de 0,1 cm como referencia) con dos modas bien marcadas, con una moda
situada en las longitudes menores (2,7 cm) y otra en las mayores (8,7 cm), siendo el
primer grupo (el de tallas chicas) el que presentó mayor número de individuos.
Figura 37. Distribución de tallas para la Mandufia (Platanichthys platana).
Oligosarcus oligolepis (Fig. 38) Presentó una distribución de tallas bastante
homogénea (con clases de tallas agrupadas al centímetro) y unimodal con la moda
situada en 13 cm, presentando un mínimo de 11 cm y un máximo de 20 cm.
Figura 38. Distribución de tallas para la Dientudo (Oligosarcus oligolepis).
0
30
60
90
120
1,5 2,1 2,7 3,3 3,9 4,5 5,1 5,7 6,3 6,9 7,5 8,1 8,7 9,3 10,1
T a llas (cm)
Nº d
e In
divi
du
os
0
5
10
15
20
25
30
5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25
Tallas (cm)
Nº d
e In
divi
duos

42
Pimelodus clarias (Fig. 39) Con su clase de talla agrupada al centímetro,
presentó una distribución de frecuencias con una moda bien marcada ocupando rango
de tallas pequeños (10 cm) y un grupo de pocos ejemplares ocupando un rango de
tallas entre 16 y 19 cm.
Figura 39. Distribución de tallas para el Bagre manchado (Pimelodus clarias).
Paralichthys orbignyanus (Fig. 40) Esta especie presentó una distribución de
frecuencias unimodal con clases de longitudes agrupada al centímetro. La moda se
situó a los 8 centímetros y la talla máxima encontrada fue de 17 cm.
Figura 40. Distribución de tallas para el Lenguado (Paralichthys orbignyanus).
Paralichthys orbignyanus
0
5
10
15
5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25Tallas (cm)
Nº d
e In
divi
duos
0
2
4
6
8
10
5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25
Tallas (cm)
Nº
de In
divi
duos

43
DISTRIBUCIÓN ESPACIAL DE LAS ESPECIES
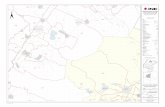
En la figura 41 se representa la ocurrencia de especies en porcentaje por zonas
con proximidad geográfica. Las mismas fueron de Oeste a Este: zona 1(Arroyo La
Caballada y Río Rosario); zona 2 (Río Santa Lucia); zona 3 (Arroyos Pando y Solís
Grande); zona 4 (Arroyo Maldonado); zona 5 (Lagunas José Ignacio y Garzón) y zona 6
(Laguna de Rocha y Arroyo Valizas).
Para la primer zona (Arroyo La Caballada y Rio Rosario) se observa una riqueza
específica mayor que en cualquiera de las zonas restantes (12 especies). Se observa
también un predominio de I. platanus con un 36% de la abundancia total, seguido por
C. voga con un 18% y Astyanax sp. con un 16%. Para la segunda zona (Río Santa
Lucía) se capturaron solo 3 especies y C. voga predominó con un 91% de la
abundancia total. En estas dos primeras zonas se observa un descenso en la
abundancia porcentual de Astyanax sp. y un aumento de C. voga en el sentido Oeste –
Este. Las mismas están habitadas por especies predominantemente dulceacuícolas.
Para la tercer zona (Arroyos Pando y Solís Grande) se capturaron 5 especies
predominando Mugil sp. con un 40%, seguida por P. orbignyanus con un 33% y M.
furnieri con un 23%. En las tres zonas analizadas anteriormente podemos observar la
continuación en el descenso de la abundancia porcentual de Astyanax sp. y la
aparición de especies que toleran salinidades mayores (Mugil sp., M. furnieri, P.
orbignyanus, y O. argentiniensis). En la zona número cuatro (Arroyo Maldonado)
fueron capturadas 5 especies siendo predominante O. argentiniensis con un 35% de la
abundancia total, seguido por P. orbignyanus con un 29% y Mugil sp. con un 18%. En
la quinta zona (Lagunas Garzón y José Ignacio) fueron capturadas 8 especies
predominando P. platana con 74% seguida por O. oligolepis con un 13% y Mugil sp.
con un 6%. En la sexta zona (Laguna de Rocha – Arroyo Valizas) fueron capturadas 6
especies siendo la predominante P. orbignyanus con un 57% seguido por Mugil sp con
un 22% y O. argentiniensis con un 9%. En las últimas cuatro zonas analizadas (Arroyo
Pando a Arroyo Valizas) se observa la co-ocurrencia de 3 especies (típicamente
eurihalinas) con porcentajes elevados, siendo estas: P. orbignyanus, Mugil sp y O.
argentiniensis.

44

45
Figura 41. Mapa de la región indicando la composición porcentual específica de la fauna ictícola colectada (referencia ver Tabla 8).


47
De la observación de la tabla 6 podemos ver que los sitios con agua dulce a
salobre (0 a 5 ups) presentaron la mayor riqueza especifica y heterogeneidad en las
abundancias de sus especies. No se observa una relación clara entre la diversidad (H)
o la equitatividad (J) y la salinidad de los sitios de estudio.
Tabla 6. Se indica para cada sitio la riqueza especifica, el logaritmo en base e de la varianza en la
abundancia de las especies (Log Var-Abu), el índice de Shannon – Weiner (H); y su equitatividad (J).
Sitio Riqueza Log Var-Abu H J Salinidad (ups)Arroyo La Caballada 6 5,61 1,94 0,75 0,0
Río Rosario 11 5,05 2,60 0,75 0,0Río Santa Lucia 3 6,13 0,52 0,33 0,2Arroyo Pando 3 2,48 1,25 0,79
Arroyo Solís Grande 5 3,89 1,66 0,71 6,6Arroyo Maldonado 5 1,46 2,10 0,90 15,7
Laguna José Ignacio 1 25,4Laguna Garzón 8 9,67 1,14 0,38 5,0
Laguna de Rocha 3 0,85 1,37 0,87 13,0Arroyo Valizas 6 2,01 2,08 0,80 0,1
ANÁLISIS MULTIVARIADOS
El Análisis Factorial de Correspondencias (AFC) determinó dos grupos en la
representación bidimensional del primer y segundo factor, y en la del primer y tercer
factor (Fig. 42 y 43). El primer grupo esta constituido por tres ambientes de agua dulce
que desembocan en la costa Oeste del Río de la Plata (Arroyo La Caballada, Río
Rosario y Río Santa Lucia). En el segundo grupo se encuentran todos los ambientes
correspondientes al Ecotono y la zona Atlántica previamente definida (Arroyo Pando a
Arroyo Valizas). La representación del segundo y tercer factor separa al Arroyo
Maldonado del resto de los sitios, pero sólo expresa un 34% de la varianza del sistema
y por ello no fue analizado con más detalle (Fig. 44). Los sitios que más influyen en el
resultado de la ordenación sobre el primer factor, son: el Arroyo Maldonado en sentido
positivo y el Río Rosario y el Arroyo La Caballada en sentido negativo (Tabla 7).

48
Figura 42. Gráfico de los dos primeros factores del AFC (% de varianza explicada: 52,94), se superponenlos resultados para sitios y especies.
Figura 43. Gráfico de los factores 1 y 3 del AFC (% de varianza explicada: 51,84), se superponen losresultados para sitios y especies.
Factor 1; Eigenvalue: 0,79294 (35,33% de Var.)
Fact
or 2
; Eig
enva
lue:
0,3
9516
(17,
61%
de
Var.)
asp
ba
cp
cv
hc
ipjl
lg
mfmspoa
ob
oo
pb
pc
pcm
pl
po
pp
rq
ALC
AM
APASGAV
LG
LJILR
RR
RSL
-2,5
-2,0
-1,5
-1,0
-0,5
0,0
0,5
1,0
1,5
-2,0 -1,5 -1,0 -0,5 0,0 0,5 1,0 1,5 2,0
Factor 1; Eigenvalue: 0,79294 (35,33% de Var.)
Fact
or 3
; Eig
enva
lue:
0,3
7055
(16,
51%
de
Var.)
asp
ba
cp
cv
hc
ipjl
lg mf
mspoa
ob
oo
pb
pc
pcm
pl
popp
rqALC
AM
AP
ASG
AV
LG
LJILR
RR
RSL
-2,5
-2,0
-1,5
-1,0
-0,5
0,0
0,5
1,0
1,5
-2,0 -1,5 -1,0 -0,5 0,0 0,5 1,0 1,5 2,0

49
Figura 44. Gráfico de los factores 2 y 3 del AFC (% de varianza explicada: 34,12), se superponen losresultados para sitios y especies.
Tabla 7. Se presentan las contribuciones de cada sitio a los tres primeros factores del AFC.Sitio Código de Sitio Factor 1 Factor 2 Factor 3
Arroyo La Caballada ALC -1,079 0,2703 -0,585Arroyo Maldonado AM 1,1502 -1,237 -1,106Arroyo Pando AP 0,9656 0,2275 0,6668Arroyo Solis Grande ASG 0,6107 0,2375 0,2642Arroyo Valizas AV 0,6771 0,1943 0,7007Laguna Garzón LG 0,181 0,6799 -0,178Laguna José Ignacio LJI 0,9965 0,0724 0,3102Laguna de Rocha LR 0,9499 0,0253 0,1465Río Rosario RR -1,114 -0,647 0,479Río Santa Lucia RSL -0,775 1,0166 -1,027
Factor 2; Eigenvalue: 0,39516 (17,61% de Var.)
Fact
or 3
; Eig
enva
lue:
0,3
7055
(16,
51%
de
Var.)
asp
ba
cp
cv
hc
ipjl
lg mf
mspoa
ob
oo
pb
pc
pcm
pl
popp
rqALC
AM
AP
ASG
AV
LG
LJILR
RR
RSL
-2,5
-2,0
-1,5
-1,0
-0,5
0,0
0,5
1,0
1,5
-2,5 -2,0 -1,5 -1,0 -0,5 0,0 0,5 1,0 1,5

50
En el caso de las especies las que más influyen sobre el resultado de la
ordenación sobre el primer factor son B. aurea y P. cromis en el sentido positivo y C.
platanus, H. commersoni, I. platanus, O. bonariensis y P. lineatus en el sentido negativo
(Tabla 8).
El análisis no presento dentro de los grupos de sitios una correspondencia con
su ubicación espacial de Oeste a Este. Para el primer grupo el sitio más legando es el
Río Rosario y el segundo grupo presenta al Arroyo Maldonado como el más distante y
a la Laguna Garzón como la más próxima al primer grupo (Fig. 42 yTabla 7).
Tabla 8. Se presentan las contribuciones de cada especie a los tres primeros factores del AFC.Especie Código de especie Factor 1 Factor 2 Factor 3
Astyanax sp. asp -0,662 0,3491 -0,357Brevoortia aurea ba 1,2916 -1,967 -1,816Cyphocharax platanus cp -1,251 -1,028 0,7869Cyphocharax voga cv -0,783 0,5251 -0,538Hypostomus commersoni hc -1,251 -1,028 0,7869Iheringichthys platanus ip -1,232 -0,299 -0,087Jenynsia lineata jl -0,524 0,0266 0,2472Lycengraulis grossidens lg -0,245 -0,36 0,969Micropogonias furnieri mf 0,8436 0,3496 0,8935Mugil sp. msp 0,8874 0,0455 0,1888Odontesthes argentinensis oa 0,8016 -0,032 -0,057Odontesthes bonariensis ob -1,251 -1,028 0,7869Oligosarcus oligolepis oo -0,626 1,043 -0,98Pachyurus bonariensis pb -1,232 -0,299 -0,087Pogonias cromis pc 1,2916 -1,967 -1,816Pimelodus clarias pcm -1,232 -0,299 -0,087Prochilodus lineatus pl -1,251 -1,028 0,7869Paralichthys orbignyanus po 0,8487 0,0339 0,1353Platanichthys platana pp 0,4818 0,6954 0,4292Rhamdia quelen rq 0,2033 1,0817 -0,293
El MDS construido en base a la matriz de distancias con el índice de Ochiai. El
mismo presenta en el gráfico de la primera y segunda dimensión una ordenación
similar al AFC conformada por los mismos dos grupos (Fig. 45). Sin embargo, a
diferencia del AFC el MDS separa a la Laguna José Ignacio del interior del segundo
grupo, solo presento una especie (Mugil sp.), y tiene como agrupamiento principal a los
Arroyos Pando, Solís Grande, Maldonado y Laguna de Rocha.
Las especies que más contribuyeron en sentido positivo a la dimensión 1 fueron
Mugil sp., M. furnieri, P. orbignyanus y O. argentinensis, y las que más contribuyeron
en sentido negativo fueron P. bonariensis, P. clarias, C. platanus y P. lineatus (Fig. 46).

51
Figura 45. Gráfico de las dimensiones 1 y 2 del MDS (distancia de Ochiai) para los sitios.
Figura 46. Gráfico de las dimensiones 1 y 2 del MDS (distancia de Ochiai) para las especies.
Dimensión 1
Dim
ensi
ón 2
ALC
AM
AP
ASG
AV LG
LJI
LR
RR
RSL
-0,8
-0,6
-0,4
-0,2
0,0
0,2
0,4
0,6
-1,0 -0,6 -0,2 0,2 0,6 1,0 1,4 1,8Stress= 0,0693
Dimensión 1
Dim
ensi
ón 2
asp
ba
cp
cv
hc
ip jl
lg mf
mspoa
ob
oo
pb
pc
pcm
plpo
pp
rq
-1,6
-1,0
-0,4
0,2
0,8
1,4
-1,2 -0,8 -0,4 0,0 0,4 0,8 1,2 1,6
Stress= 0,1692

52
4. DISCUSIÓN4.1. Puntas Rocosas
La mayor riqueza específica a lo largo de toda la costa uruguaya fue observada
en los sistemas rocosos, en particular en la región oceánica atlántica. En tal sentido, el
sistema intermareal rocoso ofrece una gran variedad de hábitats físicos como refugios
y cuevas para organismos móviles, superficies rugosas y lisas así como las piletas de
marea (Raffaelli & Hawkins, 1996). También son observados hábitats biológicos como
el caso de cubiertas algales y bancos de mejillones. Las algas, de acuerdo a
observaciones in situ, albergaron un importante número de especies de poliquetos,
crustáceos y moluscos. Además los ejemplares adultos de mejillones presentaron
organismos epibiontes como el cirripedio Balanus improvisus y Membranipora sp.,
hecho también señalado por Penchaszadeh (1973) y Riestra (1999).
Maytia & Scarabino (1979) estudiaron los cambios de las comunidades del litoral
rocoso del Uruguay. Estos autores señalan que el Río de la Plata actúa como barrera
ecológica, restringiendo la distribución latitudinal de algunas especies a esta zona. De
acuerdo a Maytia & Scarabino (1979) y Scarabino et al. (1975) existen especies de
origen frío-templado y cálido-templado en la costa uruguaya. Entre los primeros, para
el sector oceánico, se encuentran los moluscos Siphonaria lessoni, Brachidontes
rodriguezi, y Mytilus edulis platensis. Por otro lado las especies de origen cálido-
templado incluyen los moluscos Littorina zic zac y Collisella (Acmaea) subrugosa, los
cirripedios Chtamalus bisinuatus y Balanus improvisus y los mejillones Perna perna,
Brachidontes darwinianus y Mytella charruana, estos dos últimos citados para el sector
estuarino. Ambos grupos de especies fueron encontrados en este trabajo en la región
oceánica. El molusco Mytella charruana no fue observado. Scarabino & Verde (1995)
mencionan el desplazamiento de esta especie autóctona, simultáneamente con el
asentamiento de la especie invasora Limnoperna fortunei, sí encontrada en la región
Río de la Plata en la presente investigación.
Las regiones definidas a priori al comienzo de este proyecto, Río de la Plata,
ecotono y Atlántica, no coincidieron con las encontradas luego de analizados los datos.
Estos resultados muestran que las especies que ocurrieron en el departamento de
Colonia no lo hicieron en Montevideo ni en los otros sitios. De este modo quedaron

53
definidas tres zonas constituidas por Colonia, Montevideo y los sitios ubicados al este
(desde Atlántida hasta Santa Teresa). Al igual que Maytia & Scarabino (1979), se
encontraron 3 regiones principales, pero las mismas no coinciden debido a que nuestro
muestreo incluyó sitios ubicados en la costa oeste del Uruguay, no considerados por
los autores nombrados. En tal sentido, Maytia & Scarabino (1979) definieron una
región fluvio-marino correspondiente al departamento de Montevideo, un área de
ecotono entre Atlántida y José Ignacio y una región oceánica correspondiente al
departamento de Rocha principalmente. En nuestro segundo AFC el grupo 3 fue
analizado separadamente y dividió en 3 subgrupos, que representaron en términos
generales las tres regiones de Maytia & Scarabino (1979). El primer y segundo
subgrupo representado por Atlántida (G.3a) y los sitios entre Piriápolis y José Ignacio
(G.3b2) corresponden con el área de ecotono de Maytia & Scarabino (1979). Por otro
lado Santa Teresa y La Pedrera (G.3b1) coincidieron con el sector oceánico definido
por estos autores.
Las discrepancias entre los resultados del presente trabajo y los presentados por
Maytia & Scarabino (1979) respecto a las diferentes ecoregiones pueden ser atribuidas
a diferencias en la metodología empleada en cada caso (i.e. diferentes sitios de
muestreo). También es necesario considerar el hecho de que las tres regiones
propuestas por Maytia & Scarabino (1979) pueden no reflejen los patrones reales de
composición especifica a lo largo de la línea de costa, dado que fueron establecidas a
priori de realizados los muestreos.
4.2. Sistemas Estuarinos4.2.1. Invertebrados
En comparación con las puntas rocosas, la riqueza específica siempre fue
menor. Esto puede deberse a dos razones principales. La primera está relacionada
con el tipo de sustrato: los fondos blandos presentan, escasa diversidad de caracteres
topográficos, siendo la única diferencia apreciable el tamaño de grano y composición
del sedimento. Los fondos duros, por otro lado pueden presentar importantes
caracteres topográficos y por lo tanto, una mayor diversidad de hábitats (Nybakken,
1997), por lo cual albergan una mayor diversidad biológica. En segundo lugar el estrés
osmótico producido por la baja salinidad tiende a limitar el número de especies

54
presentes.
El hecho de que casi todas las desembocaduras estudiadas constituyan zonas
estuarinas explica por que el número de especies no varió considerablemente y
también explica que en su mayoría las mismas co-ocurrieron en varios sitios. Es
probable que las especies encontradas en uno o dos sitios en este estudio pudiesen
ser encontradas en los otros sitios si se realizan muestreos posteriores. Por ejemplo el
poliqueto Neanthes succinea encontrado aquí solamente en el arroyo Maldonado, ha
sido colectado en bajas densidades en la Lag. de Rocha (L.G. datos no publicados).
Los resultados del análisis multivariado no permitieron diferenciar grupos tan
claros como en el caso de los fondos rocosos o de las comunidades de peces. Fue
posible distinguir un gradiente con el arroyo La Caballada en el extremo oeste, y el
arroyo Valizas en extremo el este. La mayoría de los sitios conformaron un grupo
central. Así, no fue posible agrupar los sitios en función de las zonas definidas
previamente, ya que solo los extremos se separaron claramente.
4.2.2. Peces
Durante el presente estudio se capturaron especies de peces fundamentalmente
dulceacuícolas y de origen marino-costero. Entre las dulceacuícolas se destacaron las
familias Characidae, Clupeidae y Pimelodidae; que son características de la región
ictiofaunística Brasilica y Parano – Platense (Eigenmann, 1907 y 1909; Riguelet, 1975;
Nion, 1997).
Las especies marino-costeras encontradas se corresponderían con las especies
de la región costera de la plataforma interior del frente oceánico del Río de la Plata,
incluyendo a las familias Sciaenidae, Mugilidae y Paralichthyidae. Las familias
encontradas son típicas de la región costera que habitan en el agua de mezcla del Río,
predominantemente saladas (Angelescu & Prenski, 1987; Nión, 1997; Cousseau &
Perrotta, 2000).
Dada la poca profundidad a la que se hicieron los arrastres (Z = 1,5 m) y el
tamaño de malla utilizado para la captura (apertura de malla = 1 cm), no sorprende que

55
las tallas correspondan a individuos presumiblemente juveniles en función de sus tallas
máximas citadas (Sverlij et a., 1998; Cousseau & Perrotta, 2000). Tal es el caso de
Mugil sp. (talla máxima citada = 50 cm), M. furnieri (talla máxima citada = 63 cm), P.
cromis (talla máxima citada 120 = cm), B. aurea (talla máxima citada = 41 cm) y P.
orbignyanus (talla máxima citada = 82 cm). En el caso de otras especies, las tallas se
corresponderían con individuos adultos C. boga (talla máxima 20 = cm), L. grossidens
(talla máxima citada = 25 cm), O. oligolepis (talla máxima citada = 30 cm) y R. quelen
(talla máxima citada = 55 cm). Es de destacar que en las especies dulceacuícolas se
encontraron más individuos de tallas que corresponderían a adultos que en las
especies marino-costeras. Esto sugiere que estos sitios podrían ser áreas de cría para
las especies marinas, mientras que las dulceacuícolas podrían cumplir todo su ciclo de
vida en estos ambientes (Wootton, 1990).
En las especies que se pudo analizar la estructura de tallas, predominaron las
distribuciones unimodales, esto podría estar indicando que estos individuos podrían
pertenecer a una misma cohorte. A su vez la mayoría de estas especies presentaron
una baja heterogeneidad de tallas reforzando con esto la hipótesis previamente
mencionada (DE entre 1,4 y 6,0). Un caso de particular interés fue el de P. platana
donde la distribución de tallas se encuentra dividida en dos grupos. El primero de ellos
muy homogéneo, ocupando longitudes menores y el segundo grupo (homogéneo
también) muy apartado hacia las longitudes mayores. El primer grupo fue capturado en
su totalidad en horas del día en un único lance y sobre una zona específica. El
segundo grupo fue capturado en los siguientes lances, en horas crepusculares y
nocturnas y en diferentes zonas. Esta observación podría deberse a una segregación
de los individuos pequeños (en cohortes) probablemente relacionada con su
comportamiento.
Del análisis de la distribución de especies por zona, la riqueza específica de
cada sitio y su diversidad debemos resaltar que aquellos ambientes ubicados más al
Oeste en el área de estudio y aquellos que presentaron agua dulce se correspondieron
con el mayor número de especies. Este fenómeno se deba probablemente a que los
sitios con agua dulce brindan condiciones ambientales más estables que permiten el
desarrollo de una comunidad de peces más rica en especies. Sin embargo, aquellos
sitios con una dinámica de constante mezcla de aguas dulces y saladas solo podrían

56
mantener en forma permanente a aquellas especies adaptadas para soportar dichos
cambios (Tait, 1987).
Los análisis multivariados AFC y MDS muestran dos grupos: uno conformado
por los sitios ubicados al Oeste de Montevideo y el otro por los restantes sitios. La
zonación obtenida a través del estudio de la comunidad de peces mediante estos
análisis, podría estar indicando características ambientales marcadamente diferentes
entre los sitios al Oeste y al Este de Montevideo.
Este trabajo contó con muestreos puntuales, realizados durante los meses de
agosto, setiembre y octubre. Debido a esto no nos es posible afirmar que la zonación
observada sea permanente durante el resto del año. Además muchos de estos sitios
cuentan con una dinámica compleja de apertura y cierre de barras arenosas,
disminuyendo sus posibilidades de intercambio faunístico y generando condiciones
ambientales particulares. En este sentido también se debe señalar que el régimen de
descarga de agua dulce en los sitios estudiados podría estar afectando dicho
intercambio.
Futuros estudios deberían considerar el uso de otras artes de pesca que
permitan explorar el efecto del arte y obtener intervalos de tallas mas amplios.
También se debería considerar el realizar un monitoreo con frecuencia estacional que
permita corroborar si la zonación observada se mantiene durante todo el año.

57
5. BIBLIOGRAFIA
Azpelicueta, M.M. & Braga, L. (1991). Los curimatidos en Argentina. CONICET –
Museo de la Plata. 40(1): 1-47.
Bemvenuti, M.A. (2002). Diferenciação morfológica das espécies de peixes-rei,
Odontesthes Evermann & Kendall do Brasil: morfometria multivariada. Revista Brasilera
de Zoología. 19(1): 251-287.
Braga, L. (1994). Los Characidae de Argentina de las subfamilias Cynopotaminae y
Acestrorhynchinae. CONICET – Museo de la Plata. 40(6): 1-45.
Cione, A.L., Azpelicueta, M.M. & Casciotta, J.R. (1998). Revision of the clupeid genera
Ramnogaster, Platanichthys, and Austroclupea (Teleostei: Clupeiformes). Journal of
Ichthyology and Explorer Freshwaters. 8(4): 335-348.
Coll, J. & Oliveira, E.C. (1999). The Benthic Marine Algae of Uruguay. Botanica Marina.
42:129-135.
Cousseau, M.B. & Perrotta, R.G. (2000). Peces marinos de Argentina: Biología,
Distribución y Pesca. INIDEP -- Mar del Plata. 167 pp.
Cuadras, C.M. & Fortiana, J. (1998). Anàlisi de dades multivariants. Universitat de
Barcelona, España. 109 pp.
Escofet, A. (1973). Los géneros de anfípodos más comunes en el área de Mar del
Plata. Clave para su reconocimiento. Contribución del Instituto de Biología Marina.
239: 30pp.
Fabre, N.N. & Díaz de Astarloa, J.M. (1996). Pleuronectiformes de importancia
comercial del Atlántico Sudoccidental, entre los 34º30' y 55º S. Distribución y
consideraciones sobre su pesca. Revista Investigación y Desarrollo Pesquero. 10: 45-
55.

58
Gabrielson, P.W., Widdowson, T.B., Lindstrom, S.C., Hawkes, M.W. & Scagel, R.F.
(2000). Keys to the benthic marine algae and seagrasses of British Columbia,
Southeast Alaska, Washington and Oregon. Phycological Contribution Nº 5, Dept. of
Botany, University of British Columbia, Vancouver British Columbia, Canada.
López, H.L. (1992). Peces loriáridos de la cuenca del plata, Argentina. Parte II. El
género Hypostomus Lacépède, 1803 (Pisces, Siluriformes). Publicaciones de la
Comisión Administradora del Río Uruguay. Serie Técnica-Científica. 1: 63-79.
Maytía, S. & Scarabino, V. (1979). Las comunidades del litoral rocoso del Uruguay:
zonación, distribución local y consideraciones biogeográficas. Memorias del Seminario
sobre Ecología Bentónica y Sedimentación de la Plataforma Continental del Atlántico
Sur. UNESCO, París. 149-160.
Meffe, G.K. & Carroll, C.R. (1997). Principles of Conservation Biology, Second Edition.
Sinauer Associates, INC, Sunderland. 729 pp.
Menezes, N.A. (1983). Guia prático para conhecimento e identificação das tainhas e
paratis (Pisces, Mugilidae) do litoral Brasileiro. Revista Brasilaira de Zoología. 2(1): 1-
12.
Mianzan, H., Lasta, C., Acha, E., Gerrero, R., Macchi, G. & Bremec, C. (2001). The Río
de la Plata estuary, Argentina-Uruguay. Ecological Studies, Coastal Marine Ecosystem
of Latin America, Seeliger, U. & Kjerrfve, B. (Eds). 144:185-204.
Nonato, E.F. & Amaral, A.C.Z. (1979). Anelídeos Poliquetas. Chaves para Famílias e
Gêneros. Instituto Oceanográfico, Universidad de Sao Paulo Brasil. 78 pp.
Nybbaken, J.W. (1997). Marine biology: an ecological approach, 4th edt. BenjaminCummings, New York, USA. 481 pp.

59
Penchaszadeh, P.E. (1973). Ecología de la comunidad del mejillín (Brachidontes
rodriguezi) en el mediolitoral rocoso de Mar del Plata (Argentina): el proceso de
recolonización. Physis. 32(84): 51-64.
Raffaelli, D. & Hawkins, S. (1996). Intertidal Ecology, Second edition. Kluwer Academic
Publishers 356, Nertherlands.
Riestra, G. (1999). La comunidad Macrobentónica asociada al mejillón Mytilus edulis
platensis en costas del departamento de Maldonado: variación espacio-temporal e
incidencia del impacto pesquero. Tesis de maestría en Biología, Opción Zoología
PEDECIBA. 67 pp.
Ringuelet, R.A., Aramburu, R.H. & Alonso de Aramburu, A. (1967). Los peces
Argentinos de agua dulce. La Plata. 602 pp.
Rios, E.C. (1994). Seashells of Brazil. 2ª ed. Rio Grande: FURG. 492 pp.
Scarabino, F. & Verde, M. (1995). Limnoperna fortunei en la costa uruguaya del Río de
la Plata . Comunicaciones de la Sociedad. Malacológica Uruguaya. 7(66-67): 374-375.
Sealey, K.S. & Bustamante, G. (1999). Setting geographic priorities for marine
conservation in Latin America and the Caribbean. The Nature Conservancy, Arlington,
Virginia. 125 pp.
Stephenson, T.A. & Stephenson, A. (1949). The universal features of zonation between
tidemarks on rocky coast. Journal of Ecology. 38:289-305.
Sverlij, S.B., Delfino, R.L., López, H.L. & Espinach, A. (1998). Peces del Río Uruguay.
Publicación de la Comisión Administradora del Río Uruguay. 89 pp.
Tait, R.V. (1987). Elementos de ecología marina. Segunda Edición . Editorial Acribia
SA. España. 446 pp.
Wootton, R.J. (1990). Ecology of teleosts fishes. Chapman & Hall, London.