Sustancias puras y mezclas
-
Upload
maria-jose-campello -
Category
Education
-
view
1.014 -
download
7
description
Transcript of Sustancias puras y mezclas

IES Concepción Arenal3º ESO
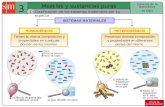
Sistemas materiais
Mesturas e sustancias puras

IES Concepción Arenal3º ESO
HOMOXÉNEOS HETEROXÉNEOS
Os seus compoñentes atópanse distribuídos de forma uniforme
Presentan unha soa fase
Teñen as mesmas propiedades en todos os seus puntos
Poden ser :
•Sustancias puras
•Mesturas homoxéneas
Presentan distinta composición e propiedades en diferentes partes do mesmo.
Presentan varias fases
Os compoñentes se distinguen a simple vista ou
con microscopio
SISTEMAS MATERIAIS

IES Concepción Arenal3º ESO
SUSTANCIAS SIMPLES
Carbono, ouro, nitróxeno, calcio, xofre, etc.Están formadas por un só elemento.Non poden descompoñerse
COMPOSTOS
Están formadas por varios elementos unidos entre sí en proporcións fixas.
Poden descompoñerse en sustancias simples por métodos químicos
SISTEMAS HOMOXÉNEOS
Sustancias puras
• Presentan un aspecto homoxéneo.
• Teñen composición fixa e invariable
• As súas propiedades físicas e químicas son sempre as mesmas.
Algunhas non poden descompoñerse e outras sí
Diamante ( C )
NaCl: Cloruro de sodio
Ouro

IES Concepción Arenal3º ESO
Mesturas homoxéneas
Os seus compoñentes atópanse distribuídos de xeito uniforme.
Presentan unha soa fase
Teñen as mesmas propiedades en todos os seus puntos.
Non se poden diferenciar os seus compoñentes a simple vista, nin cun microscopio.
Os seus compoñentes poden separarse por métodos físicos: destilación, cromatografía, etc
Exemplo: a auga salgada, o aire, a auga de mar, o aceiro, bronce.
SISTEMAS HOMOXÉNEOS

IES Concepción Arenal3º ESO
Mesturas heteroxéneas.
Os compoñentes se atopan en fases diferentes
Pódense apreciar distintas propiedades en puntos diferentes
Exemplo:
Auga e aceite
Auga con cubitos de xeo
Os seus compoñentes se distinguen a simple vista.
Emulsións, suspensións e
coloidesEx: clara de ovo, maionesa, leite, xelatina, flan,
espumas, aerosol, xeles, néboa,etc.
Parece que son homoxéneas pero non é así

IES Concepción Arenal3º ESO
¿Crees que algún sistema material heteroxéneo pode ter unha soa sustancia? Pon un exemplo
¿Cal das seguintes sustancias son sustancias puras ou mesturas:
Auga destilada Ouro
Auga potable Deterxente en po
Refresco de cola

IES Concepción Arenal3º ESO
Clasifica as sustancias seguintes en sistemas homoxéneos ou heteroxéneos:granito, polvo de talco, azúcar, vidro, área de praia, a páxina do caderno que tes diante?
Homoxéneos
Polvo de talco
Azúcar
Vidro
Heteroxéneos
Páxina do caderno
Area de praia
Granito

IES Concepción Arenal3º ESO
¿Cómo distinguir unha sustancia pura dunha mestura homoxénea?
Ambalas dúas presentan as mesmas propiedades en todos os puntos. (Non poderemos distinguilas a simple vista)
Para distinguilas nos fixaremos en que as sustancias puras teñen propiedades características fixas que podemos atopar en táboas e as mesturas non.
Unha sustancia pura en estado líquido ten unha temperatura de ebulición fixa. Unha disolución ten unha temperatura de ebulición variable que depende da composición.

IES Concepción Arenal3º ESO
Propiedades físicas
Estado de agregación Líquido
Apariencia Incoloro
Densidad 789 kg/m3; 0,789 g/cm3
Masa molar 46,07 g/mol
Punto de fusión 158.9 K (-114.3 °C)
Punto de ebullición 351.6 K (78.4 °C)
Temperatura crítica 514 K ( °C)
Viscosidad 1.074 mPa·s a 20 °C.
Propiedades químicas
Acidez (pKa) 15,9
Solubilidad en agua Miscible
Etanol

IES Concepción Arenal3º ESO
¿CÓMO DISTINGUIR ENTRE UNHA SUSTANCIA PURA E UNHA DISOLUCIÓN?
A temperatura de ebulición é unha propiedade característica das sustancias puras.
A temperatura se mantén constante durante o proceso de ebulición
A temperatura aumenta gradualmente durante a ebulición
SUSTANCIA PURA
MESTURA HOMOXÉNEA

IES Concepción Arenal3º ESO
Sustancia simple

IES Concepción Arenal3º ESO
Sustancias puras
Sustancia pura simple
Non pode descompoñerse en outras mediante procedementos físico-químicos normais.
Ouro
Hidróxeno
Nitróxeno
Composto
Está formada por dous ou máis elementos
Pode descompoñerse en sustancias simples por métodos químicos
Auga
Amoníaco
Cloruro de sodio
Glucosa

IES Concepción Arenal3º ESO
Sustancias simplesa) Átomos b) Moléculas
Mestura de composto e dúas sustancias simplesComposto
A materia a nivel molecular
Sustancia simple
Formada por partículas iguais.
Formado por una sola clase de átomos (os átomos son todos iguais) que poden estar unidos formando moléculas ou non
Compostos
Formados por partículas iguais
As partículas (moléculas) dos compostos están formadas por átomos diferentes, unidos entre sí en proporcións fixas.

IES Concepción Arenal3º ESO
Indica cal representa a unha sustancia simple, un composto, unha mestura de sustancias simples
Os debuxos representan a escala atómica tres clases diferentes de materia. Describe cada un segundo sean unha mestura, un elemento ou un composto.
A materia a nivel molecular

IES Concepción Arenal3º ESO
Sustancias simples, compostos, mesturas
Identifica cal dos dibuxos representa a un composto, a unha sustancia simple e a unha mestura
I
J
K

IES Concepción Arenal3º ESO
Sistemas materiais
Sistemas homoxéneos Sistemas heteroxéneos
Sustancias purasMesturas homoxéneas
(Disolucións)Exemplo: auga mineral,
vinagre, aleación
Mesturas heteroxéneas(Suspensións, emulsións
e coloides)Ex: clara de ovo,
maionesa, xelatina, flan, espumas, aerosol, geles,
néboa,etc.Sustancias simples
(formadas por un so elemento)
H2, Fe, O3
Compostos(están formados por
varios elementos)H2O, NaCl, NH3

IES Concepción Arenal3º ESO
TÉCNICA CONSISTE EN: SE FUNDAMENTA EN:
FILTRACIÓN
Utilizar unha barreira (filtro) que permite o paso
dos compoñentes de tamaño menor.
A diferencia de tamaño das partículas dun e doutro
compoñente. Exemplo: Auga e area
DECANTACIÓN
Deixar fluir un dos componeñentes, mentras
que os outros permanecen inmóviles
nun recipiente.
A diferencia de densidade dos diferentes compoñentes que,
ademáis, deben de ser inmiscibles. Exemplo: Auga e
aceite.
SEPARACIÓN MAGNÉTICA
Atraer cun imán as partículas dun
compoñente que ten propiedades magnéticas
(ferromagnético)
As diferencias nas propiedades magnéticas dos diferentes
compoñentes. Exemplo: Ferro e xofre.
SEPARAR OS COMPOÑENTES DUNHA MESTURA HETEROXÉNEA

IES Concepción Arenal3º ESO
DECANTACIÓN
A gravidade separa os compoñentes dunha mestura con
distinta densidade.
Tras a sedimentación se decanta un dos
compoñentes.
Permite separar os compoñentes dunha
mestura heteroxénea dun sólidoe un líquido.
As partículas de menor tamaño que os poros do filtro quedarán retidas nel
TAMIZADO
Separación dos sólidos de distinto tamaño de grao
cun tamiz ou criba que deixe pasar sómentes aos de
menor tamaño
SEPARAR OS COMPOÑENTES DUNHA MESTURA HETEROXÉNEA
Embudo de decantación
FILTRACIÓN

IES Concepción Arenal3º ESO
FiltraciónSEPARAR OS COMPOÑENTES DUNHA MESTURA HETEROXÉNEA

IES Concepción Arenal3º ESO
Decantación
embudo de decantación
aceite
agua
tubo estrecho de goteo
SEPARAR OS COMPOÑENTES DUNHA MESTURA HETEROXÉNEA

IES Concepción Arenal3º ESO
Separación magnética
SEPARAR OS COMPOÑENTES DUNHA MESTURA HETEROXÉNEA

IES Concepción Arenal3º ESO
CRISTALIZACIÓN
Sirve para separar sólidos disoltos nun líquido.
Ao evaporarse o líquido, o sólido cristaliza..
DESTILACIÓN
Utilízase para separar os diferentes compoñentes dunha disolución e se basea nas diferentes temperaturas de ebulición de cada compoñente.
Cristales de sulfato de cobre obtidos mediante cristalización
Equipo de destilación
SEPARAR OS COMPOÑENTES DUNHA MESTURA HOMOXÉNEA

IES Concepción Arenal3º ESO
Se fundamenta nos diferentes puntos de ebulición das sustancias que están mesturadas.
Ao quentar, ferve primeiro a sustancia de menor punto de ebulición.
O vapor pasa ao refrixerante, onde
condensa.
O termómetro permite coñecer a qué compoñente
pertence o vapor, xa que a Teb é
característica de cada sustancia.
SEPARAR OS COMPOÑENTES DUNHA MESTURA HOMOXÉNEA
DESTILACIÓN

IES Concepción Arenal3º ESO
Se fundamenta na diferente velocidade de difusión dos compoñentes dunha mestura a través dun soporte determinado. Utilízase para averiguar o número de compoñentes dunha mestura complexa.
Ponse unha gota da mestura sobre unha tira de papel secante (ou un xiz) e con a posición marcada cun lápiz.
Introdúcese a tira nun recipiente que contén unha mestura de
disolventes. A marca debe quedar por riba do nivel do líquido.
Os disolventes ascenden por capilaridade e arrastran aos compoñentes da mestura que
presentan diferentes velocidades de difusión, lográndose a separación dos mesmos.
SEPARAR OS COMPOÑENTES DUNHA MESTURA HOMOXÉNEA
CROMATOGRAFÍA

IES Concepción Arenal3º ESO
DESCOMPOSICIÓN POR ELECTRÓLISIS
Una composto se descompon en sustancias simples pola acción dunha corrente eléctrica continua.
SEPARAR OS COMPOÑENTES DUN COMPOSTO
Ao facer pasar a corrente eléctrica a través da auga se obtén hidróxeno e osíxeno

IES Concepción Arenal3º ESO
Electrólise da agua: Descomposición da auga en hidróxeno y osíxeno
Os gases obtidos poden recollerse nun tubo invertido
cheo de auga

¿QUÉ FIXEMOS NO LABORATORIO?Mestura heteroxénea
Separación magnética
Limaduras de ferroSustancia pura simple Mestura heteroxénea
Disolver en auga
Filtrar
Area (retida no filtro)Mestura heteroxénea Disolución azul
Destilación
AugaDisolución azul (máis concentrada)
Cristalización
Sólido azul (Sulfato de cobre)Sustancia pura simple
Electrolise
Hidróxeno e OsíxenoSustancia pura composto

¿Cómo podemos calcular a composición da mestura que usamos no laboratorio?
100·m
marea%
mesturadatotal
area
100·m
mferro%
mesturadatotal
ferro
100·m
mcobredesulfato%
mesturadatotal
cobredesulfato

¿Cómo podemos separar auga salgada e aceite?
Decantación
Aceite Auga salgada
Destilación
AugaSustancia pura (composto)
Auga salgada (máis concentrada)
Cristalización
Sal (Cloruro de sodio)Sustancia pura
(composto)