T E S I S - IBt UNAM · 2020. 2. 13. · fisicoquímicas del agua marina son la salinidad, la...
Transcript of T E S I S - IBt UNAM · 2020. 2. 13. · fisicoquímicas del agua marina son la salinidad, la...
-
UNIVERSIDAD POLITÉCNICA DEL ESTADO DE
MORELOS
INGENIERÍA EN BIOTECNOLOGÍA
Establecimiento de las condiciones de
crecimiento que permitan estudiar la
cascada de esporulación de
Oceanobacillus iheyensis
T E S I S QUE PARA OBTENER EL TÍTULO DE:
INGENIERO EN BIOTECNOLOGÍA
P R E S E N T A
MIROSLAVA ESCAMILLA ROMERO
TUTORES:
DIRECTORA: DRA. ROSA MARÍA GUTIÉRREZ RÍOS
TUTOR INTERNO: DR. JESÚS HERNÁNDEZ ROMANO
TERCER SÍNODO: M.B. MARÍA LUISA TABCHE BARRERA
JIUTEPEC, MORELOS DICIEMBRE, 2019
-
I
Tabla de contenido
Agradecimientos. ....................................................................................................................... I
Glosario y abreviaturas ............................................................................................................ II
1. Introducción ........................................................................................................................... 1
2. Antecedentes ......................................................................................................................... 2
2.1 Características geofisicoquímicas y división de los océanos por profundidad ......................... 2
2.2. Estudios de los ecosistemas y comunidades microbianas de los océanos. ............................. 6
2.3 Estudio de microorganismos en la era genómica y metagenómica. ........................................ 7
2.3.1 Comunidades microbianas ¿Cómo estudiar su estructura y composición? ........................................... 7
2.3.2 Secuenciación de genomas ..................................................................................................................... 8
2.3.2.1 Secuenciación Sanger ...................................................................................................................... 9
2.3.3 Las tecnologías de la nueva generación (NGS)...................................................................................... 10
2.3.3.1 Pirosecuenciación .......................................................................................................................... 10
2.3.3.2 Illumina .......................................................................................................................................... 11
2.3.3.3 SOLiD.............................................................................................................................................. 12
2.3.3.4 Ion Torrent ..................................................................................................................................... 14
2.3.3.5 Helicos BioSciences ........................................................................................................................ 15
2.3.3.5 SMRT (Single Molecule Real Time) ................................................................................................ 16
2.4 Caracterización de especies bacterianas por medio del gen 16S ........................................... 18
2.6 Los Firmicutes como modelo de esporulación. .................................................................... 19
-
II
2.6.1 Firmicutes .............................................................................................................................................. 19
2.6.1.1 Bacilli .............................................................................................................................................. 19
2.6.1.2 Clostridia ........................................................................................................................................ 19
2.6.1.3 Negativicutes ................................................................................................................................. 20
2.6.1.4 Tissierella ....................................................................................................................................... 20
2.6.1.5 Erysipelotrichia .............................................................................................................................. 20
2.6.2 Esporulación en Firmicutes ................................................................................................................... 20
2.6.3 Cascada del inicio de la esporulación en Bacillus subtilis ..................................................................... 22
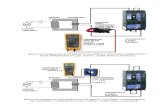
2.7 Identificación de esporas por tinción. ................................................................................. 22
3. Oceanobacillus Iheyensis .................................................................................................. 23
3.1 Oceanobacillus iheyensis aislada a una profundidad de 1050 m en la cordillera Iheya. ......... 23
3.2 Crecimiento y características morfológicas de Oceanobacillus Iheyensis .............................. 24
3.3 Aislamiento y caracterización filogenética a través del gene ribosomal 16S de Oceanobacillus
iheyensis. ................................................................................................................................ 24
3.4 Predicción computacional de la cascada del inicio de la esporulación en Oceanobacillus
iheyensis ................................................................................................................................. 25
4. Definición del problema...................................................................................................... 28
5. Justificación ......................................................................................................................... 29
6. Objetivo general .................................................................................................................. 30
6.1. Objetivos particulares ....................................................................................................... 30
7. Hipótesis ............................................................................................................................... 30
8. Metodología.......................................................................................................................... 31
-
III
8.1 Cepas utilizadas. ................................................................................................................ 31
8.2 Diseño de oligonucleótidos................................................................................................. 31
8.3 Análisis de la especificidad de los oligonucleótidos diseñados. ............................................ 32
8.4 PCR preliminar y electroforesis ........................................................................................... 32
8.5 Formulación de medios, siembra y observación en el microscopio de contraste de fases...... 33
8.6 Extracción de DNA total y PCR ............................................................................................ 34
8.7 Tinción de esporas (método de Scheaffer-Fulton) ............................................................... 35
9. Resultados ........................................................................................................................... 36
9.1 Diseño de oligonucleótidos................................................................................................. 36
9.1.1 Análisis de similitud de los oligonucleótidos OIMP1 y OIMP2 .............................................................. 38
9.2 PCR preliminar ................................................................................................................... 46
9.3 Formulación de medios ...................................................................................................... 47
9.4 Tinción de esporas con verde de malaquita (método de Scheaffer Fulton). .......................... 51
9.5. Extracción de DNA total .................................................................................................... 53
10. Discusión............................................................................................................................ 54
13. Referencias bibliográficas ............................................................................................... 58
14. Referencias bibliográficas de figuras ............................................................................. 69
-
I
Agradecimientos.
Al Programa de Apoyo a Proyectos de Investigación e Innovación Tecnológica (PAPIIT) con
número de proyecto IN202118.
A la Dra. Rosa María Gutiérrez Ríos por permitirme participar en el proyecto, por sus
enseñanzas, consejos y por su gran apoyo durante mi estancia en el equipo de trabajo.
A la M.B. María Luisa Tabche Barrera por su apoyo y consejos durante la elaboración del
proyecto.
A la M.C. Nori Castañeda Gómez por su apoyo, consejos y enseñanzas durante mi estancia
en el equipo de trabajo.
A la M.C. Josefina Guzmán Aparicio por todo el apoyo que me brindó.
A todos mis compañeros del laboratorio, por su solidaridad, su
Al Dr. Jesús Hernández Romano por su apoyo durante toda la carrera, sus enseñanzas y
consejos.
A Dios, a mi Santísima Madre, a mi familia y amigos, gracias por su apoyo.
-
II
Glosario y abreviaturas
➢ Alcalófilo: microorganismo capaz de desarrollarse en ambientes alcalinos con valores
de pH entre 8.5–12.
➢ BLAST: Basic Local Alignment Search Tool (Herramienta de búsqueda de alineación
local básica)
➢ Circulación termohalina: Circulación oceánica global impulsada por flujos de
diferenciales de calor, densidad y concentración salina, estos flujos promueven la
mezcla de agua entre las diferentes profundidades del océano. Es un mecanismo de
conducción no observacional.
➢ ddNTPs: dideoxinucleótidos trifosfato.
➢ dNTPs: deoxinucleótidos trifosfato.
➢ Dorsal oceánica: cadena continua de montañas volcánicas submarinas que rodean el
globo.
➢ Extremófilo: microorganismo capaz de desarrollarse en ambientes con condiciones
extremas.
➢ Halófilo: microorganismo capaz de desarrollarse en ambientes con un alto contenido
de sales.
➢ Humus: Conjunto de los compuestos orgánicos presentes en la capa superficial del
suelo, procedente de la descomposición de animales y vegetales.
➢ LBs: Medio de cultivo Luria Bernani suplementado con sales.
➢ NCBI: National Center for Biotechnology Information.
➢ NGS: Next generation sequencing
➢ O. iheyensis: Oceanobacillus iheyensis HTE831
➢ OIMP1: oligonucleótido en sentido directo para amplificar la región r16S en el genoma
de O. iheyensis.
➢ OIMP2: oligonucleótido en sentido reverso para amplificar la región r16S en el genoma
de O. iheyensis.
➢ Oligotrofia: Propiedad de las aguas de lagos profundos de alta montaña, con escasa
cantidad de sustancias nutritivas y poca producción de fitoplancton.
➢ pb: pares de bases
➢ PCR de colonia: técnica de PCR que utiliza células vivas obtenidas de cultivo en medio
líquido fresco o de colonia de medio sólido fresco en sustitución de DNA.
➢ PCR: Polymerase Chain Reaction (reacción en cadena de la polimerasa).
-
III
➢ Piezófilo/barófilo: microorganismo capaz de desarrollarse en ambientes con
presiones altas.
➢ Psicrófilo: microorganismos que se desarrollan en ambientes con temperaturas por
debajo de los 20 ºC, algunos pueden soportar hasta los –20 ºC.
➢ Taxón: grupo de organismos con parentesco genético agrupados de acuerdo a un
sistema de clasificación específica
➢ Termófilo: microorganismo que se desarrolla en ambientes con temperaturas por
encima de los 45 ºC.
➢ ID: carnet de identidad
-
1
1. Introducción
Las comunidades microbianas son moldeadas por las características físicas y químicas
del ambiente. Sin embargo, se ha descrito que la estructura de la comunidad microbiana, a su
vez, regula el medio ambiente y las vías biogeoquímicas en todos los ecosistemas del planeta.
Esto sucede también en el océano, donde la exportación de materia orgánica a las
profundidades oceánicas, son críticas en el ciclo del carbono y la modulación del dióxido de
carbono atmosférico (Follows and Dutkiewicz, 2011). Los ambientes oligotróficos del fondo
oceánico son el hogar de bacterias extremófilas capaces de soportar temperaturas y
concentraciones salinas extremas, carencia de nutrientes, etc. Es en este ambiente donde se
han logrado aislar e identificar bacterias marinas como Oceanobacillus iheyensis aislada de
sedimentos obtenidos de una profundidad de 1050 m (Takami et al., 2002). Oceanobacillus
iheyensis es una bacteria esporulante perteneciente al phylum Firmicutes de la cual muy poco
de su fisiología se ha descrito. No ha sido posible hasta el momento modificarla genéticamente
y las condiciones en las que esporula no se encuentran bien descritas, por lo que en este
trabajo probamos medios de cultivo que promovieron eficientemente la esporulación. El interés
del grupo de trabajo por estudiar la esporulación en este microorganismo, deriva de haber
encontrado que la cascada del inicio de la esporulación, está controlada por un fosforrelevo
que posee una fosfotrasferasa, Spo0B, con una composición de dominios diferente a las
descritas en el organismo modelo Bacillus subtilis. Por lo que encontrar las condiciones
optimas en las que Oceanobacillus iheyensis esporula y encontrar protocolos para modificarla
genéticamente serán de gran importancia a nivel experimental, esto aunado a que ha
demostrado recientemente que esta especie tiene potencial industrial (Lu et al., 2001; Takami
et al., 1999; Fragoso et al., 2014)
-
2
2. Antecedentes
2.1 Características geofisicoquímicas y división de los océanos por profundidad
El océano es una masa de agua que ocupa alrededor del 71% de la superficie del Globo
(García Gasca et al., 2007; Castro y Huber, 2007; Libes, 2009; Tarbuck y Lutgens, 2005). Esta
masa de agua es típicamente clasificada en cuatro cuencas principales: Pacífico, Atlántico,
Índico y Ártico (Castro y Huber, 2007). El océano es un lugar donde procesos biológicos,
químicos, físicos y geológicos interactúan (Libes, 2009). Las principales características
fisicoquímicas del agua marina son la salinidad, la temperatura, la presión hidrostática, la
densidad y el color (Castro y Huber, 2007). Las condiciones físicas y químicas del océano
varían dependiendo de la topografía, de la profundidad de la columna de agua y de la
composición química del agua (Castro y Huber, 2007). El océano contiene solutos, gases y
partículas que se encuentran en concentraciones variables de acuerdo a la localización y
profundidad del océano. Dichas sustancias pueden clasificarse como se muestra en la Tabla
1.1 (Libes, 2009).
Los compuestos más abundantes en el agua oceánica son los iones mayores en
proporciones casi constantes, también son conocidos como iones conservados, y constituyen
alrededor del 99.8% de solutos disueltos. El resto de los solutos en el océano no se encuentran
en concentraciones proporcionales debido a que dependen de reacciones químicas que
ocurren por procesos físicos derivados del movimiento del agua, son conocidos como
compuestos no conservados (Libes, 2009).
-
3
Tabla 1.1 Clasificación de materiales presentes en el agua oceánica y rangos de
concentraciones aproximadas (Libes, 2009)
Fase Categoría Rango de
concentración Ejemplo
Solutos
Elementos
mayores/iones
>50 mM 𝐶𝑙−, 𝑁𝑎+
10 mM a 50 mM 𝑀𝑔2+, 𝑆𝑂42−, 𝐶𝑎2+, 𝐾+
Elementos
menores
0.1 mM a 10 mM 𝐶∗, 𝐵𝑟−, 𝑁2(𝑔), 𝐵∗∗, 𝑂2(𝑔)
0.1 µM a 100 µM 𝑆𝑖, 𝑆𝑟2+, 𝐹−, 𝑁𝑂3
−, 𝐿𝑖+, 𝐴𝑟(𝑔),
𝑃𝑂43−, 𝑅𝑏+, 𝐼−, 𝐵𝑎2+
Traza de
elementos
1 nM a 100 nM 𝑉, 𝐴𝑠, 𝑈, 𝐻+, 𝑁𝑒(𝑔), 𝑁𝑖, 𝐾𝑟(𝑔), 𝑍𝑛,
𝐶𝑟, 𝐶𝑢, 𝐻𝑒(𝑔), 𝑆𝑒, 𝑆𝑏, 𝐴𝑙
-
4
El océano se divide en zonas basándose horizontalmente en la distancia a la costa
(sedimento); verticalmente en la profundidad del agua (columna); y los tipos de organismos
que viven en dicha zona. El ambiente bentónico se divide de acuerdo a la distancia, tipo y
profundidad de la plataforma continental; y el ambiente pelágico se divide en relación a la
distancia de la plataforma continental y se subdivide verticalmente de acuerdo con la cantidad
de luz que logra penetrar en la columna de agua, tal como se muestra en la Figura 1 (Castro
y Huber, 2007).
Figura 1. Principales divisiones del fondo marino (Castro y Huber, 2007)
El ambiente marino se divide en el reino pelágico (columna de agua) y béntico
(sedimento), ambos reinos caracterizándose por sus propiedades físicas, químicas y
biológicas (Zinger et al., 2011). La zona batipelágica se extiende entre los 1000 m y los 4000
m. En esta zona ya no hay luz solar, por lo que no existe producción primaria derivada de la
fotosíntesis; la fuente de alimento son los materiales orgánicos producidos en las zonas
superiores que descienden hacia las profundidades, de modo que la vida en esta zona no es
abundante; la temperatura tiende a mantenerse constante y típicamente baja, entre 4ºC y -
1ºC, a excepción de las ventilas hidrotermales dónde la temperatura llega a sobrepasar los
400 ºC. La salinidad y otras características químicas del agua en esta zona son constantes
(García-Gasca et al., 2007; Castro y Huber, 2007).
-
5
Debido a la ausencia de luz en esta zona la presencia de organismos fotosintéticos es
nula (Castro y Huber, 2007). En la Figura 2 se muestra la abundancia de plancton y luz de
acuerdo a la profundidad de la columna de agua.
Figura 2. Abundancia de plancton y luz de acuerdo a la profundidad de la columna de agua
(Castro y Huber, 2007)
-
6
Los organismos de esta zona dependen de la circulación termohalina y el gran
transporte oceánico que constantemente aportan oxígeno a las aguas profundas (Castro y
Huber, 2007; Rahmstorf, 2003; Rahmstorf, 2006; Primeau, 2005; Zinger, et al., 2011). Las
bacterias que se encuentran en esta zona son alcalófilas, termófilas, piezófilas, psicrófilas y
halófilas. Todas estas bacterias extremófilas se encuentran en lodos y sedimentos (Takami et
al., 1999; Takami et al., 2002; Lu et al., 2001).
2.2. Estudios de los ecosistemas y comunidades microbianas de los océanos.
El termino microorganismo define a formas de vida menores a 200 µm que comparten
características en común pertenecientes a cualquiera de los tres dominios incluyendo
procariotas (arqueas y bacterias) y eucariotas (algas y protistas fagótrofos), tanto autótrofos
como heterótrofos. También son incluidos por la microbiología los virus y agentes subvíricos.
Los procariotas marinos tienen morfología de cocos, bacilos y filamentos típicamente menores
de 1-2 µm con diversidad taxonómica, fisiológica y metabólica (López y Zaballos, 2005).
Un ecosistema bacteriano se compone por factores bióticos, factores abióticos y por
una comunidad bacteriana. La comunidad bacteriana se constituye por un conjunto complejo
de diversidad de especies de microorganismos que interactúan y comparten los recursos y
factores del ecosistema que habitan (Champbell y Reece, 2007). A esto se le denomina nicho
ecológico (Curtis et al., 2007). Los principales factores que determinan el tipo de comunidades
microbianas en cada locus oceánico son: la penetración de luz solar, temperatura,
disponibilidad de materia orgánica lábil, concentración de oxígeno disuelto, entre otros (Zinger
et al., 2011).
Los sedimentos marinos están compuestos de complejas comunidades microbianas.
Se reconoce que estas comunidades juegan un papel importante en la cadena trófica, ya que
son capaces de utilizar minerales abundantes en los sedimentos como sustratos
metabolizables para convertirlos en intermediarios o productos metabólicos que sustentan sus
actividades y las de otros miembros de la comunidad, estos minerales pueden ser arcillas,
carbonatos, silicatos, óxidos metálicos, etc. (Moraga et al., 2014; García Cruz y Aguirre
Macedo, 2014). Muchos de estos microorganismos son quimiótrofos caracterizados por usar
dos tipos de compuestos como fuente de energía: carbono orgánico (quimioorganótrofos) o
fuentes de energía inorgánica (quimolitótrofos) (Romero et al., 2012; Tatis y Barbosa, 2013).
Si un organismo utiliza carbono orgánico como fuente de carbono, se lo denomina heterótrofo,
-
7
mientras que si fija su carbono a partir de CO2, es un autótrofo. Las combinaciones de estos
términos aparecen así cuando se revela la versatilidad de un organismo dado, y la situación
puede ser semánticamente compleja si un organismo es capaz concentrar muchos tipos de
metabolismo; por ejemplo, algunos organismos, llamados mixótrofos, pueden ser tanto
autótrofos como heterótrofos (Alder, 2014; Toro et al., 2008).
Los microorganismos presentes en muchos de estos ecosistemas y aquellos que
forman parte de la microbiota de otros organismos, no han podido ser aislados de manera
individual. Esto debido a que identificar las condiciones en que estos puede crecer de manera
autosuficiente sigue siendo un reto, lo cual no está solamente relacionado con sus
requerimientos nutricionales y fisicoquímicos, sino porque también ahora se sabe que muchos
de ellos necesitan de la presencia de otros para su subsistencia ya que están adaptados a
vivir en consorcios (Ochoa y Montoya, 2010), por ejemplo, las bacterias Streptococcus
thermophilus y Lactobacillus spp, que se usan para elaborar quesos y yogurt; y cepas de
Saccharomyces para la producción de bebidas alcohólicas artesanales e industriales. Por ello,
su caracterización utilizando técnicas de secuenciación de nueva generación ha sido
importante para conocer el funcionamiento de las comunidades microbianas. En secciones
posteriores hablaremos de estas nuevas tecnologías y su aplicación en la caracterización de
las comunidades microbianas.
2.3 Estudio de microorganismos en la era genómica y metagenómica.
2.3.1 Comunidades microbianas ¿Cómo estudiar su estructura y composición?
Más del 90% de los microorganismos no son capaces de desarrollarse in vitro con
técnicas microbiológicas. Algunos de ellos debido a que provienen de ambientes extremos, y
de otros tantos se desconocen sus requerimientos nutricionales y condiciones fisicoquímicas
necesarias para el desarrollo, relaciones simbióticas, etc., a estos microorganismos se les
denomina no cultivables. Gracias a las técnicas y herramientas de ingeniería genética
molecular, es posible aislar y caracterizar a las comunidades microbianas. A estos estudios,
se les conoce como metagenómicos (Escalante Lozada et al., 2001).
Metagenoma se refiere al conjunto de información genética compuesta por organismos
pertenecientes a una misma comunidad (Tan et al., 2015; Jansson y Hofmockel, 2018). La
metagenómica revela la información genética de una comunidad al analizar su estructura y
-
8
dinámica génica (Jansson y Hofmockel, 2018). Utilizando técnicas de secuenciación, se puede
estudiar y analizar la composición genética de una comunidad entera en paralelo y con ello
identificar las funciones de los genes de los organismos presentes en una comunidad. Estos
estudios se han llevado acabo en muchos ambientes incluido el oceánico (Takami et al, 1999;
Takami et al, 2002; Tan et al., 2015).
Estos estudios se realizan a través de técnicas de secuenciación de alto rendimiento o
secuenciación de nueva generación (NGS), que han logrado dilucidar la composición y
diversidad de las comunidades microbianas sin la necesidad de cultivarlas (Jansson y
Hofmockel, 2018).
Oceanobacillus iheyensis HTE831 fue identificada en un estudio metagenómico donde
otras 99 bacterias fueron aisladas (Takami et al, 1999). En dicho estudio, se realizó un análisis
filogenético basado en las secuencias de los genes 16S ribosomales de los 100 organismos
aislados de aguas profundas, lo que reveló que una amplia gama de taxones estaban
representados en los sedimentos de aguas profundas de la cresta Iheya de las islas Nankai
(1050 m de profundidad: 27 ° 47.18´ 126 N, 126 ° 54.15´ E). Probando condiciones diversas
de crecimiento fue posible obtener 100 aislados incluyendo a O. iheyensis HTE831, que
posteriormente fue secuenciada (Takami et al, 2002). A continuación se explicará brevemente
el origen y características de las técnicas de secuenciación empleadas en el estudio de
genomas y metagenoma.
2.3.2 Secuenciación de genomas
La secuenciación de genomas es una herramienta para la pronta identificación de un
organismo y el análisis funcional de sus genes (Aguilar Bultet y Flanquet, 2015; Lay-Son y
León, 2015). Se compone de un conjunto de técnicas y métodos bioquímicos con el fin de
determinar el orden y orientación de los nucleótidos en una molécula de DNA (Rojas y
Jiménez, 2018). Junto con el desarrollo tecnológico, la secuenciación de genomas ha
disminuido costos, tiempos y cantidad de material genético necesarios. A fines del siglo XX y
principios del siglo XXI se han desarrollado técnicas de secuenciación que han permitido el
descubrimiento de microorganismos no reportados en la literatura, además de la
secuenciación de genomas completos de microorganismos procedentes de ambientes
extremos, hasta ahora no cultivables en condiciones de laboratorio. Las técnicas de
secuenciación se describen a continuación.
-
9
2.3.2.1 Secuenciación Sanger
La secuenciación tipo Sanger consiste en amplificar DNA un molde monocatenario,
mediante la técnica de PCR con un solo cebador, incorporando de manera aleatoria
dideoxinucleótidostrifosfato (ddNTPs) marcados fluorescentemente en el extremo 3 ’. Los
ddNTPs carecen del grupo 3’-OH impidiendo la unión del siguiente dNTP y deteniendo la
enlongación. Cada fluorocromo se encuentra asociado inequívocamente a un nucleótido
específico y emite luz con una longitud de onda específica, por lo que se generan fragmentos
de todos los tamaños posibles distinguibles entre sí por el terminador específico sin intervenir
con la reacción de la polimerasa (Voet et al., 2007; Rojas y Jiménez, 2018). Los amplicones
son separados mediante una columna electroforética capilar. La emisión de fluorescencia de
cada fragmento es detectada tras la excitación promovida mediante la luz de un laser, la cual
es transformada por un software de un equipo de secuenciación de DNA en un
electroferograma (Berg et al., 2008). En la Figura 3 se esquematiza el proceso automatizado
del método de secuenciación tipo Sanger para la obtención de un electroferograma partiendo
de una mezcla de reacción que contenga DNA molde, un oligonucleótido, DNA polimerasa,
dNTPs y ddNTPs con fluorocromos.
Figura 3. Automatización del método de secuenciación tipo Sanger [1].
-
10
2.3.3 Las tecnologías de la nueva generación (NGS)
Las tecnologías de la nueva generación (NGS, por sus siglas en inglés, “Next
Generation Sequencing”), permiten la secuenciación masiva de muestras en paralelo,
reduciendo costos y tiempo en comparación a la secuenciación Sanger (Aguilar Bultet y
Flanquet, 2015; Lay-Son y León, 2015). Las NGS pueden basarse en secuenciación por
síntesis o ligación, con o sin amplificación previa. Las NGS se describen a continuación
(Aguilar Bultet y Flanquet, 2015; Blanco, 2011; Koneman et al., 2018).
2.3.3.1 Pirosecuenciación
Pirosecuenciación o tecnología 454: fue la primer NGS en salir al mercado entre 2004
y 2005, utilizada para la secuenciación de fragmentos cortos de DNA monocatenarios que se
inmovilizan en un pocillo sobre una microplaca. La estrategia utilizada es la detección de
bioluminiscencia producida por la acción de la luciferasa al incorporarse los dNTPs en la
reacción de PCR en tiempo real. La incorporación de un dNTP libera un grupo pirofosfato (Ppi),
la ATP sulfurilasa convierte el Ppi en ATP en presencia de ADP, el ATP junto con la luciferasa
cataliza la conversión de luciferina a oxiluciferina, emitiendo luz. La cantidad de luz emitida
corresponde al número y órden de dNTPs añadidos durante la reacción. La incorporación de
los dNTPs es uno a uno (dGTP, dATP,dTTP, dCTP), por lo que los dNTPs que no son
incorporados a la hebra de DNA deben ser degradados rápidamente del medio por la enzima
apirasa (Clop et al.,2000; Pérez Pérez et al., 2006). En la Figura 4 se esquematiza como se
lleva a cabo el proceso de pirosecuenciación para obtener una secuencia de DNA.
Figura 4. Proceso de pirosecuenciación. [2]
-
11
2.3.3.2 Illumina
Illumina salió al mercado en 2006 con un método novedoso que permite realizar
secuenciación masiva en paralelo. Se basa en secuenciación por síntesis, que necesita de
amplificación previa, y adapta la familia de secuenciadores Solexa. Utiliza terminadores
marcados con fluorescencia al igual que la secuenciación Sanger, teniendo como diferencia la
posibilidad de eliminar la fluorescencia de los marcadores una vez obtenida la imagen,
desbloqueando el carbono 3’ para continuar con la secuenciación (Agu ilar Bultet y Falquet,
2015; Suárez Moya, 2017). El paso preliminar consiste en la fragmentación del DNA y ligación
de adaptadores a una superficie sólida denominada flow cell. En el pimer paso, la librería se
incrusta en la placa “flow cell” por complementariedad a los adaptadores produciendo
amplificación por puente hasta obtener un racimo de secuencias clonales del fragmento inicial,
como se muestra en la Figura 5.
Figura 5. Proceso de secuenciación masiva illumina. [3]
-
12
2.3.3.3 SOLiD
SOLiD es una técnica de secuenciación salida al mercado en 2007 basada en la
ligación de nucleótidos (Figura 6). La técnica consiste en generar fragmentos de DNA (una
biblioteca) y ligarlos a adaptadores unidos a perlas. Una solución emulsificante de agua con
aceite contiene lo necesario para una reacción de PCR, los fragmentos de DNA de las perlas
se amplifican mediante la emulsión por PCR. Terminada la reacción, se desnaturaliza el DNA
para obtener una sola cadena, y las perlas se fijan en una superficie de vidrio sólido. Una
mezcla de oligonucleótidos se hibridan con los fragmentos de DNA y se agregan a la mezcla
de ligadura. En estos, el doblete de las bases cuarta y quinta se caracteriza por una de las
cuatro etiquetas fluorescentes al final de la secuencia. Después de la detección de la
fluorescencia del marcador, se determinan las bases 4 y 5 en la secuencia. Los
oligonucleótidos ligados después de la quinta base se separan, eliminando el marcador
fluorescente, luego se repiten los ciclos de hibridación y ligadura, esta vez determinando las
bases 9 y 10 en la secuencia; en el ciclo subsiguiente se determinan las bases 14 y 15, y así
sucesivamente. El proceso de secuenciación puede continuar de la misma manera con otro
cebador, más corto en una base que el anterior, lo que permite determinar, en los ciclos
sucesivos, las bases 3 y 4, 8 y 9, 13 y 14 (Hedges et al., 2011; Huang et al., 2011; Ansorge
2009).
-
13
Figura 6. Proceso de secuenciación [4]
-
14
2.3.3.4 Ion Torrent
La tecnología de secuenciación Ion Torrent salió al mercado en 2010. Es una técnica
de secuenciación similar a la pirosecuenciación y a la tecnología Illumina, solo que no utiliza
la detección de fluorescencia o imágenes sino que se detectan los protones liberados por la
polimerasa tras la secuenciación durante el proceso de secuenciación. Al igual que en las
demás secuenciaciones, primero debe fragmentarse el DNA y acoplarlo a perlas con
adaptadores, se emulsifican y se someten a proceso de PCR. Las perlas se depositan en una
nanoplaca semiconductora, el DNA se desnaturaliza acoplándose un cebador y se une la
polimerasa. A medida que se realiza el ensayo específico dónde se adiciona nucleótido a
nucleótido (A, G, C o T), al incorporarse alguno a la cadena se liberan protones y se realiza el
registro de iones de hidrógeno. La liberación de protones resultante genera un ∆pH que
provoca la acumulación de carga positiva en la capa de detección (Figura 7 A), y el pilar
metálico conductor "vía" transmite como un cambio de voltaje en la puerta del transistor. Esto
a su vez activa la corriente del transistor, y la señal de corriente acumulada en el tiempo se
envía fuera del chip, en forma de una señal de voltaje, a través de un proceso de sondeo de
todo el chip. Estas señales de pH se muestrean desde el pozo a alta frecuencia (Figura 7 B,
curva azul), y luego se ajusta a un modelo que extrae la señal neta (Figura 7 B, curva roja).
Las señales de incorporación neta para cada flujo se convierten en la entrada principal,
reflejando ninguna incorporación, incorporación de un nucleótido, incorporación de dos
nucleótidos, etc., para cada flujo de prueba, y estos datos brutos son la entrada para el
algoritmo de llamada base que convierte la serie completa de señales de incorporación neta
para ese pozo, sobre cientos de flujos de nucleótidos de prueba, en una secuencia de lectura
correspondiente en un electroferograma (Figura 7 C). Al terminar con la incorporación de
nucleótidos y con la lectura, se efectúa un lavado y se agrega otro nucleótido distinto para
continuar con la secuenciación. (Kchouk et al., 2017; Suárez Moya, 2017; Salipante et al.,
2014; Bragg et al., 2013; Merriman et al., 2012).
-
15
Figura 7. Descripción general de la secuenciación Ion Torrent. (A) Dispositivo sensor de pH
semiconductor con perla con hebra de DNA monocatenaria cebada para la extensión y unida
con polimerasa. (B) Señales de toma de muestras de ∆pH desde el pozo a alta frecuencia
(curva azul), y luego se ajusta a un modelo que extrae la señal neta (curva roja). (C)
Electroferograma del pozo. [5]
2.3.3.5 Helicos BioSciences
Helicos BioSciences es una técnica de secuenciación salida al mercado en 2008 que
no necesita amplificación previa. Como en las demás técnicas, el DNA es fragmentado, se le
añade una cola de adeninas y se fija en una placa sólida. Los nucleótidos con fluoróforos
acoplados son añadidos uno a uno, cuando ocurre el apareamiento se genera fluorescencia y
es registrada por el detector. Los nucleótidos sin aparear libres en el medio y los fluoróforos
de las bases apareadas, son barridas al realizar el lavado. En seguida del lavado se añade
otro nucleótido para continuar con la secuenciación (Pushkarev et al., 2009; Bautista, 2010;
Orlando et al., 2011; Goren et al., 2010; Chu y Corey, 2012). En la Figura 8 A se resume el
proceso de secuenciación Helicos BioSciences hasta obtener el reporte de la secuencia, y en
la Figura 8 B se muestra el ciclo de adhesión de nucleótidos, toma de imagen y lavado que
ocurre durante la secuenciación.
-
16
Figura 8. Secuenciación Helicos BioSciences (A) esquema completo del proceso de
secuenciación.[6] (B) Ciclo de adhesión de nucleótidos, toma de imagen y lavado [7]
2.3.3.5 SMRT (Single Molecule Real Time)
SMRT Pacific Biosciences (PacBio) salió al mercado en 2010 basando su tecnología
en la secuenciación de una sola molécula de DNA en tiempo real sin la necesidad de amplificar
previamente ni preparar ningún tipo de librería (fraccionar el DNA). La técnica se basa en una
microplaca con nanopocillos bautizados como zero-mode wevwguide. Los pocillos pueden
detectar un volumen de 20 zeptolitros (10-21 litros). A través de este pocillo pasa un haz de luz
de 20 a 30 nm para inmovilizar al DNA y desnaturalizarlo. En el pocillo, la molécula de DNA
queda con una sola molécula de polimerasa, como se muestra en la Figura 9. A continuación,
se introducen los nucleótidos con diferente longitud de onda del fluoróforo, una vez que ocurre
el apareamiento de bases, el fluoróforo es retirado del carbono 3’ para incorporar la siguiente
base y continuar con la secuenciación (Chee Seng y Dimitrios, 2013; Ari y Arikan, 2013;
Rhoads y Au, 2015).
A
B
-
17
Figura 9. (A) Secuenciación SMRT en nanoporos con una sola hebra de DNA sin fragmentar
[8]. (B) Enlongación de cadena de DNA por la polimerasa y conforme ocurre la enlongación se
detecta la fluorescencia [9].
Los diferentes métodos de secuenciación han permitido la identificación de especies
tanto cultivables y no cultivables. El primer indicio de la presencia de una especie en una
mezcla de DNA de muestra ambiental es realizado a través de la utilización de marcadores de
especie. Uno de los marcadores filogenéticos mas ampliamente utilizados para el caso de
genoma bacterianos es el gene 16S ribosomal. No obstante, dada la similitud de este marcador
entre especies muy cercanas que impide en algunos casos llegar hasta la identificación
inequívoca de la especie, el uso de otros marcadores se ha propuesto (Rinke et al., 2013). A
pesar de lo anterior, el gene 16S ribosomal es una herramienta útil para la identifiación de
organimos en muestras ambientales por lo que acontinuación se describe su particularidades.
A B
-
18
2.4 Caracterización de especies bacterianas por medio del gen 16S
El gen 16S rRNA es una parte integral del ribosoma procariótico con evolución
constante, con regiones altamente conservadas entre especies y grupos bacterianos, y con
regiones hipervariables V1 a V9 que facilita la amplificación mediante cebadores universales
con alta especificidad para distinguir entre organismos (Jünemann et al., 2017).
Para la caracterización, primero debe purificarse y secuenciarse la región 16S
ribosomal con alguna técnica de secuenciación. Las secuencias obtenidas deben analizarse
mediante algún algoritmo como Chromas (Elegant Themes), un visualizar de cromatogramas
de secuenciación de ADN, que permite identificar errores en la secuenciación y al final obtener
la secuencia en formatos adecuados para su comparación con otras secuencias, a través de
programas de alineamiento. El alineamiento básico puede hacerse mediante la paquetería
Blast (Altschul et al., 1990), usando el programa BLASTn , que compara la secuencia problema
con alguna base de datos de referencia como la NR de NCBI. Los resultados obtenidos, se
alinean con algoritmos bioinformáticos como por ejemplo Clustal X
(http://www.clustal.org/clustal2/). Este alineamiento hace evidente las diferencias encontradas
entre las secuencias problema y las de referencia. Una vez analizado el alineamiento es
posible establecer un posicionamiento filogenético basado en el porcentaje de similitud.
Existen muchos desarrollos informáticos capaces de realizar este procesamiento, para este
trabajo se uso el software libre CLC Sequence Viewer 8.0.0 (https://www.qiagen.com/) (Pineda
Mendoza et al., 2011; Kumar et al, 2017).
De las técnicas descritas en esta sección la caracterización por medio del gen 16S y la
secunciación de genomas fueron herramientas fundamentales para el descubrimiento,
caracterización del genoma y clasificación filogenética de Oceanobacillus iheyensis HTE831.
El resultado de estos análsis arrojo que esta cepa es un bacilo perteneciente al phylum
Firmicutes. En la sección subsecuente describiremos algunas características de este phylum
y de la clase Bacilli a la que pertence Oceanobacillus iheyensis.
http://www.clustal.org/clustal2/https://www.qiagen.com/
-
19
2.6 Los Firmicutes como modelo de esporulación.
2.6.1 Firmicutes
Los miembros del phyla Firmicutes, son bacterias Gram positivas bacilares de entre
0.7-0.9 µm de diámetro y 3.5-6.0 µm de longitud. Las células pueden presentarse de manera
planctónica, en pares, en cadenas cortas y aglomerados. Algunas con motilidad debido a
flagelos perítricos. Varios de sus miembros tienen la capacidad de formar esporas refractarias
redondas u ovoides en esporangios con inflamación terminal o subterránea. Son
moderadamente termofílicas con un rango de temperatura optima de crecimiento entre 30 y
60 ºC. Presentan un crecimiento óptimo en salinidad marina y se desarrollan
organotróficamente en un número de sustratos protéicos y carbohidratos (Slobodkin et al.,
2003; Yang et al., 2010). El phylum Firmicute se subdivide en clases Bacilli, Tissierella,
Negativicutes, Clostridia y Erysipelotrichia (Galperin, 2013; Watanabe et al., 2015).
2.6.1.1 Bacilli
Se encuentran ampliamente dispersas por el mundo en diversos ambientes y en la
microbiota de organismos acuáticos y terrestres, aunque su mejor reservorio es el suelo
(Villarreal Delgado et al., 2017). Se han logrado secuenciar cepas cultivables y no cultivables.
Muchas de estas cepas tienen la capacidad de formar esporas, lo que está determinado por
la presencia de genes de esporulación que son compartidos con otros Firmicutes; resisten
diversos tipos de estrés y producen compuestos de interés industrial. Típicamente se
desarrollan en condiciones aerobias o pueden ser anaeróbias facultativas; son bacilares, de
entre 0.5 y 10 µm; crecen en ambientes con rangos de pH, salinidad y temperaturas robustas.
(Villarreal Delgado et al., 2017; Sosa et al., 2005; Rodas et al., 2009; Galperin et al., 2012)
2.6.1.2 Clostridia
La clase Clostridia es anaerobia estricta, por lo que carece de enzimas como la
peróxido dismutasa y la catalasa, lo que la distingue de la clase Bacilli. En la tinción de Gram
se tiñe como Gram positiva. Contiene del 22 al 55% del contenido de GC% en su genoma,
dependiendo de la especie. Se encuentra en suelos y sedimentos marinos, tractos intestinales
de animales y humanos, en desechos vegetales y animales en estado de putrefacción, y en
heridas (Hatheway, 1990; Rainey, 2015; Papoutsakis, 2008).
-
20
2.6.1.3 Negativicutes
Son los únicos organismos Gram negativos del phylum Firmicute, por lo que cuentan
con membrana externa, sin embargo, son filogenéticamente Gram positivos y su genoma
contiene bajo porcentaje de GC% (Marchandin et al., 2010; Campbell, 2015).
2.6.1.4 Tissierella
Tiene forma bacilar; no son formadoras de esporas; son anaerobios estrictos y Gram
negativos. Tienen un tamaño entre 1.0–4.0 µm. Su genoma contiene un 28% de contenido de
GC% (Alauzet et al., 2014; Collins et al., 1986; Farrow et al., 1985; Bae et al., 2004).
2.6.1.5 Erysipelotrichia
Su morfología es bacilar; su estructura celular es Gram positiva; no es móvil; no es
formadora de esporas; puede ser aerobio o anaerobio facultativo (Ludwig et al., 2009).
2.6.2 Esporulación en Firmicutes
La esporulación es uno de los fenómenos más investigados en bacterias Gram
positivas. En los géneros Bacillus y Clostridium, es detonada por el deterioro de las
condiciones ambientales (Pérez y Montoya, 2012; De Hoon et al., 2010; Castañeda Sandoval
et al., 2009). La esporulación, que es una respuesta de quorum sensing (Marquina y Santos,
2010; Dandekar et al., 2012; Castañeda Sandoval et al., 2009; Ramirez Mata et al., 2014), es
un proceso de diferenciación altamente conservado entre las bacterias y es regulado mediante
señalizaciones fisiológicas y ambientales, e involucra la regulación de la expresión de factores
de transcripción sigma (σ) (Castañeda Sandoval et al., 2009; Madigan et al., 2009). En la
esporulación se produce una espora por célula altamente resistente a condiciones adversas y
extremas por medio de señalizaciones ADN-proteína y proteína-proteína (Pérez y Montoya,
2012; De Hoon et al., 2010). La espora se compone de una envoltura protéica externa
denominada exosporium; por debajo se encuentra la cutícula o cubierta de la espora, también
formada por proteínas específicas; seguida hacia el interior se encuentra el cortex compuesta
por péptidoglicano de uniones laxas; en seguida se localiza el protopasto de la espora, que
comprende la pared celular de la célula germinal y la membrana citoplasmática; por último se
encuentra el núcleo de la espora, dónde se encuentran enzimas, ribosomas, dipicolinato de
calcio y DNA asociado a proteínas pequeñas ácido solubles (Pérez y Montoya, 2012). Para
-
21
llegar de bacteria vegetativa a espora, ambos géneros pasan por 7 etapas donde existen
procesos reversibles y procesos irreversibles, descritas a continuación y esquematizadas en
la Figura 10 (Hoch, 1976; Pérez y Montoya, 2012; De Hoon et al., 2010; Madigan et al., 2009).
Figura 10. Etapas de la esporulación de una bacteria [10].
• Etapa 1: el DNA se configura como filamento axial, esta fase es reversible.
• Etapa 2: formación de una doble membrana asimétrica.
• Etapa 3: formación de la pre-espora.
• Etapa 4: entre las dos membranas de la célula se forma la corteza formado por
peptidoglicano modificado.
• Etapa 5: formación de la cubierta de la espora de carácter proteico rica en residuos de
cisteína.
• Etapa 6: maduración de la espora y la síntesis de ácido dipicolínico.
• Etapa 7: intercalación de calcio en el DNA y liberación de la espora por medio de
enzimas líticas.
-
22
2.6.3 Cascada del inicio de la esporulación en Bacillus subtilis
Bacillus subtilis sub sp. subtilis 168 (B. subtilis) es la bacteria Gram positiva
perteneciente al phylum Firmicute considerada como el organismo modelo para el estudio de
bacilos esporulantes. El proceso de esporulación en B. subtilis es regulada por una cascada
de factores sigma (σ) que se unen a la RNA polimerasa, permitiendo la expresión espacial y
temporal de genes requeridos para dicho proceso. Esta cascada junto con el factor
transcripcional Spo0A, juegan un papel importante en la esporulacion puesto que regula varios
cientos de genes que participan en el proceso (Guerrero Zavala y Pedroza Reyes, 2015). La
proteína Spo0A es miembro de la familia de proteinas reguladoras de respuesta. Es controlada
mediante fosforilación inducida por condiciones ambientales y fisiológicas, a través de una
cascada de señalización (Castañeda Sandoval et al., 2009). La forma fosforilada de Spo0A es
Spo0AP, la cual se une al DNA para iniciar con el proceso de esporulación. Los genes diana
que involucran las primeras etapas de eporulación a los que se une Spo0AP aún son
desconocidos. Spo0AP tambien controla la transcripción de genes y operones involucrados en
la activación de proteínas reguladoras de respuesta específicas como SpoIIA, SpoIIE, SpoIIG;
además, silencia y reprime genes en cadena provocando la activación directa o indirecta de
ciertos genes, como la represión del gen regulador del estado de transición AbrB, que al
silenciarse, activa genes como sigmaH que codifica para el factor de transcripción de
esporulación temprana σH. Siguiendo con el proceso de esporulación, σF es reemplazado en
la espora por σG, y σE se reemplaza en la célula madre por σK (Faecett et al., 2000; Errington,
2003).
2.7 Identificación de esporas por tinción.
Las endoesporas no son susceptibles a ser teñidas por métodos comunes, algunos
colorantes pueden teñir la célula dejando a la espora incolora. La tinción de Scheaffer y Fulton
emplea verde de malaquita como colorante principal. Para forzar la penetración del tinte en el
cuerpo de la endoespora es necesario aplicar calor para permear las paredes de la endoespora
al tinte, normalmente se utiliza calor húmedo. Terminada la tinción, se realiza un lavado con
agua fría de grifo para eliminar el excedente y sellar los poros de la endoespora. Como
contratinción o colorante de contraste se utiliza safranina, la cual tiñe el área vegetativa. En un
preparado adecuado, las endoesporas aparecen verdes dentro de las células rojas o rosadas,
al observar la muestra en el objetivo de inmersión (100x) en un microscopio óptico (Tortora et
al., 2007; Santamaría et al., 2014; Vázquez et al., 2010).
-
23
3. Oceanobacillus Iheyensis
3.1 Oceanobacillus iheyensis aislada a una profundidad de 1050 m en la cordillera Iheya.
A partir de sedimentos marinos extraidos de expediciones realizadas en el año 1999 a
1050 m de profundidad en la cordillera Iheya, se cultivó y secuenció el gen 16S ribosomal de
una comunidad microbiana, de dónde se caracterizó, y posteriormente se secuenció su
genoma completo, la bacteria Oceanobacillus iheyensis HTE831 (O. Iheyensis), alcalófila y
halotolerante. Se ha reportado que O. iheyensis tiene la capacidad de esporular en ambientes
extremos con presiones arriba de 1 atm, y desarrollarse a 1 atm in vitro, así como
concentraciones de NaCl entre 3–15% cultivada in vitro (Lu et al., 2001; Takami et al., 1999),
lo que la apresta a ser un modelo de estudio que permita comprender como se lleva a cabo el
mecanismo de esporulación en contraste con otras Bacillales endoesporulantes tal como B.
subtillis, considerada modelo de estudio del fenomeno de esporulación.
La cordillera Iheya, de dónde se extrajo O. iheyensis, se encuentra aproximadamente
a unos 25 Km al norte de la Gran Chimenea del Norte (Jian et al., 2015). Los fluidos
hidrotermales submarinos del canal Okinawa son ricos en CO2, K, Li, NH4, H2S y He. Las
relaciones isótopicas de He y C así como las características químicas del océano, indican que
el sistema hidrotérmico se encuentra controlado por la reacción entre el agua de mar y la
riqueza de CO2 en las rocas volcánicas ácidas (Sakai et al., 1990). El canal Okinawa es una
cuenca de arco posterior ubicada detrás de la Trinchera Ryukyu y de las islas Ryukyu, contiene
diversos campos hidrotermales activos incluyendo Iheya del Norte y la cordillera Iheya. La
Trinchera Ryukyu se extiende desde Japón hasta Taiwán, el frente volcánico de igual manera,
se extiende desde Japón hasta Taiwán y se encuentra dentro del Canal Okinawa. Desde
Kyushu hasta la isla Okinawa, coinciden pequeños volcanes activos ubicados a unos 25 Km
al oeste del arco no volcánico (Lin et al, 2004). Debido a la gran actividad volcánica, las
temperaturas de las profundidades oceánicas no son bajas, al contrario, con forme se
desciende, la temperatura aumenta. Considerando lo anterior, la temperatura optima de
crecimiento de Oceanobacillus iheyensis reportada por Lu et al. (2001) es de 30 ºC.
-
24
3.2 Crecimiento y características morfológicas de Oceanobacillus Iheyensis
Oceanobacillus iheyensis es una bacteria bacilar, móvil por medio de flagelos
perítricos, con un tamaño de 0.6–0.8 x 2.5–3.5 µm, Gram positiva, perteneciente al filo
Firmicute, formadora de esporas, y aerobia estricta. Fue aislada de una muestra de sedimentos
recolectada del batipelágico a una profundidad de 1050 m de la Cordillera Iheya de las islas
Nansei, Japón. Fue nombrada como HTE831 y se caracterizó como una bacteria halófila y
halotolerante mediante secuenciación del gen ribosomal 16S, dónde se determinó que es
filogenéticamente cercana a Bacillus subtilis (Lu et al., 2001; Takami et al., 1999).
La morfología de las colonias de O. iheyensis HTE831 es circular, opaca, de un color
blanco, de aspecto cremoso, de aproximadamente de 2-3 µm de diámetro pasados 2 días de
incubación, con una temperatura óptima de crecimiento de 30 ºC y 1 atm de presión (Lu et al.,
2001). Se ha reportado que la cepa HTE831 presenta halotolerancia extrema, siendo capaz
de crecer en medios que contienen 0–21% de NaCl y pH en rangos de 7.5–9.5; las fases de
latencia y exponencial se prolongan al aumentar la concentración salina. Se ha reportado que
es capaz de crecer en medios con fuente de carbono en forma de glucosa, manosa, maltosa
y turanosa. También se reportó que es resistente a eritromicina y susceptible a ampicilina (Lu
et al., 2001).
3.3 Aislamiento y caracterización filogenética a través del gene ribosomal 16S de
Oceanobacillus iheyensis.
Conforme a lo reportado por Takami y colaboradores (1999), Oceanobacillus iheyensis
se extrajo de sedimentos de aguas profundas de la Cordillera Iheya de las Islas Nankai a 1050
m de profundidad (27º 47.18 N, 126º 54.15 E), recolectados por el sumergible Shinkai 2000
tripulado y utilizando muestreadores de lodo cilíndricos. Las muestras del lodo se diluyeron
dos veces en caldo marino estéril, y se sembró una muestra de 100-200 µL de la suspensión
en placas de agar marino. El agar marino estaba compuesto de 1% de leche descremada o
1% de almidón de papa, diferentes pH (3,4 o 9.7), y concentraciones de NaCl distintas (0%,
2%, o 15%). El medio marino alcalino contenía 1% de carbonato de sodio (𝑁𝑎2𝐶𝑂3) y el medio
marino ácido con concentración de 50 mM de ácido cítrico (𝐶6𝐻8𝑂7). Las placas de agar se
incubaron de 4 ºC a 55 ºC a 1 atmósfera de presión de 1 a 4 semanas. Se tomó una asada de
una colonia aislada clasificada como HTE831 y se resuspendió en 50 µL de Tris-HCL 25 mM,
glucosa 50 mM, EDTA 10 mM y lisozima (1 mg/mL). La resuspensión se incubó por 20 minutos
-
25
a 37 ºC, y se añadieron 5 µL de solución SDS al 10% a la suspensión celular para la posterior
extracción de DNA cromosómico con la técnica de fenol-cloroformo. Se realizó un PCR para
la amplificación del gen 16S ribosomal, y posteriormente se secuenciaron por medio de la
técnica Sanger utilizando un secuenciador LI-COR 400L. Las secuencias obtenidas se
alinearon utilizando el programa de alineación múltiple Crustal W donde se observó el
parentesco con Bacillus subtilis (Takami et al., 1999).
3.4 Predicción computacional de la cascada del inicio de la esporulación en
Oceanobacillus iheyensis
Para sobrevivir, los organismos deben adaptarse a cambios ambientales repentinos a
los que tiene que responder en forma rápida y precisa para garantizar su sobrevivencia. La
adaptación a estos cambios está estrechamente ligada a la correcta percepción,
procesamiento y transmisión de los estímulos, así como a la generación de respuestas
apropiadas a través de redes de señalización y regulación genética (Capra y Laub, 2012).
Un sistema modelo para la investigación de cómo las redes de señalización y
reguladoras determinan el destino celular, lo encontramos en la bacteria Gram positiva Bacillus
subtilis (López y Kolter, 2009). Esta bacteria es un sistema multipotencial debido a que puede
diferenciarse en distintos tipos celulares, los cuales son alcanzados a través de una compleja
red de regulación y señalización. No obstante, B. subtilis no es el único organismo que posee
una compleja red de señalización que le permite acceder a una gran variedad de destinos
celulares. Más aún, se ha observado que al igual que esta bacteria de suelo, otros organismos
pertenecientes a microbiomas (Browne et al., 2016), así como a otros aquellos que viven en
cuerpos de agua, o asociados a la rhizósfera (Cairns et al., 2014) poseen redes de señalización
y de regulación que les permiten adaptase a estos ambientes.
Una de estas bacterias, pertenecientes a cuerpos de agua, es Oceanobacillus
iheyensis, la cual es una bacteria halotolerante y clasificada como esporulante, la cual fue
aislada del lecho marino, y que fue secuenciada en el año 2001 (Cong et al., 2014). Para ella,
aunque se ha descrito que es una bacteria que esporula, el medio especifico en laboratorio no
se ha determinado, ni la vía de transducción de señales que induce el proceso de esporualción.
-
26
En nuestro grupo de trabajo, estudios computacionales previos hechos a través de
genómica comparativa lograron predecir la presencia de un fosforrelevo en Oceanobacillus
iheyensis, en donde la proteínas Spo0B presentó un arreglo de dominios estructurales como
se muestra en la Figura 11. La búsqueda se realizó identificando secuencias de amino ácidos
llamadas dominios los cuales se conservan dentro de las proteínas homologas, es decir
aquellas que son susceptibles de tener un origen común. La idea detrás de esto es el de usar
perfiles construidos con secuencias sobre las que se presume son homologas y que servirán
para identificar a proteínas con orígenes similares. Este trabajo se hizo para las proteínas del
fosforrelevo de 400 Firmicutes (Martinez-Amador, tesis 2017), encontrando que
Oceanobacillus iheyensis tiene un fosforrelevo en donde la proteína Spo0B presenta la
arquitectura alternativa SpOB_a, en tanto que B. subtilis contiene a los dominio SpOB_ab,
SpOB_a, y que en su modelo alternativo carece del dominio SpOB_ab y conserva solo el
SpOB_a descrito con función fosfostransferasa, que pudimos observar en especies de la clase
Bacilli como también en algunas especies de Clostridia (Figura 12). Por los que determinar si
esta variante es funcional se torna de especial interés, en particular en O. iheyensis en donde
se han aislado proteínas como lipasas y la presencia de pigmentos, que podrían estar
produciéndose en condiciones no esporulantes. Por lo que tener un control del proceso a nivel
molecular puede ser un factor importante para mejorar la producción de estas moléculas. De
modo que un primer paso es establecer las condiciones de crecimiento en el laboratorio que
favorecen el control de la esporulación, tema de la tesis presentada.
Figura 11. Arquitecturas de dominios identificadas en Firmicutes. Spo0B presenta dos
arquitecturas de domino SPOB_a y SPOB_a-SPOB_ab
HisKA HATPase_cPAS
Cache_1
5 TM -5 TM R_LYT
DUF3149
HisK_N
DUF4118
Peripla_BP_3
HisKA HATPase_c
HisKA HATPase_c
HisKA HATPase_c
HisKA HATPase_c
HisKA HATPase_c
HisKA HATPase_c
HisKA HATPase_c
HisKA HATPase_cPAS PAS
HisKA HATPase_cPAS PAS PAS
HisKA HATPase_cPAS
HisKA HATPase_cResponse_r eg
Response_r eg
Response_r eg
Spo0A_C
SPOB_a
SPOB_ab
Sda
ASH1
TPR_12 Spo0E- like
C
N
Spo0F Spo0ASpo0B
Rap
KipI
Sda
Spo0E
1
2
3
4
5
6
7
8
9
10
11
12
PAS
TPR_12
PASPASPAS
-
27
Figura 12. Arbol filogéntico que muestra la cascada de señalización del inicio de la
esporulación en Firmicutes. Oceanobacillus presenta un fosforrelevo con un modelo
alaternativo de la proteína Spo0B
Bacillus subt ilis subsp. subtilis 168
Bacillus anth racis A0248
Syntrophobotulus glycolicus
Solibacillus silvest ris
Geobacillus the rmoglucosidasius
Desulfotomaculum nigrifican s
Clostridium sacch aroperbutylacetonicum
Bacillus cellulosilyticus
Bacillus cyto toxicus
Kyrpidia tusc iae
Bacillus megate rium WSH-002
Acidaminococ cus intestini
Brevibacillus brevis
Bacillus coagu lans 36D1
Acidaminococ cus fermentans
Halobacillus halop hilus
Bacillus licheniformis ATCC 14580
Thermobacillus compo sti
Exiguobacterium ant arcticum
Clostridium acidurici
Thermoanaerobacterium thermosaccha rolyticum DSM 571
Paenibacillus sp. Y412MC10
Oscillibacter valericigenes
Thermincola pot ens
Bacillus thuringien sis serovar finitimus YBT-020
Clostridium novyi
Desulfitobacterium hafniense DCB-2
Clostridium cf. sacc harolyticum K10
Desulfitobacterium dehalogena ns
Clostridium acet obutylicum ATCC 824
Clostridium botu linum E3
Paenibacillus mucilaginosus K02
Geobacillus the rmoleovorans
Clostridium sterco rarium subsp. stercorarium DSM 8532
Bacillus cereus ATCC 14579
Paenibacillus terraePaenibacillus polymyxa E68 1
Mageeibacillus indolicus
Desulfosporosinus orientis
Anaerostipes hadrus
Halothermothrix orenii
Clostridium beijerinckii NCIMB 805 2
Peptoclostridium dif ficile 630
Bacillus thuringien sis Bt407
Exiguobacterium sibiricum
Geobacillus sp. Y412MC61
Clostridium cellulolyticum
Symbiobacterium thermophilum
Amphibacillus xylanu s
Acetohalobium arabat icum
Clostridium kluyveri DSM 555
Ammonifex deg ensii
Ethanoligenens harbinense
Bacillus amyloliquefa ciens DSM 7
Macrococcus caseolyticus
Thermaerobac ter marianensis
Bacillus megate rium DSM 319
Bacillus cereus B4 264
Bacillus sp. 1NLA3 E
Lysinibacillus sph aericus
Bacillus thuringien sis BMB171Bacillus anth racis Sterne
Carboxydothermus hydrogenoformans
Clostridium perfringen s 13
Clostridium lentoc ellum
Desulfotomaculum reduc ens
Alicyclobacillus acido caldarius subs p. acidocaldarius DS M 446
Clostridium botu linum BKT01592 5
Ruminiclostridium thermoce llum ATCC 27405
Clostridium cellulovorans
Bacillus subt ilis BEST761 3
Eubacterium rectale ATCC 33656
Geobacillus sp. WCH70
Clostridium tet ani E88
Thermoanaerobacter wiegelii
Syntrophomonas wolfei
Bacillus thuringien sis MC28
Bacillus atroph aeus 1942
Pelotomaculum thermopropion icum
Ruminococcus albus
Erysipelothrix rhusiopath iae SY1027
Faecalibacterium prausnitzii SL3 /3
Bacillus thuringien sis serovar kurst aki HD73
Exiguobacterium sp. AT1b
Bacillus velezens is FZB42
Sulfobacillus acidophilus DS M 10332
Bacillus clausii
Desulfotomaculum gibso niae
Veillonella parvula
Natranaerobius thermophilus
Selenomonas ruminantium
Alkaliphilus metalliredigens
Bacillus pumilus SAFR -032
Thermosediminibact er oceani
Faecalitalea cylindroides
Tepidanaerobacter acetatoxydans Re1
Bacillus haloduran s
Clostridium sp. BNL1 100
Desulfotomaculum ace toxidans
Ruminococcus champanellensis
Clostridium botu linum A3 Loch Maree
Thermoanaerobacterium saccharolyticu m
Roseburia intestinalis M5 0/1
Bacillus megate rium QM B1551
Clostridium ljungdahlii
Caldicellulosirupto r bescii
Oceanobacillus iheyensis
Heliobacterium modesticaldum
Lachnoclostridium phyt ofermentans
Halanaerobium praevalens
Clostridium past eurianum BC1
Bacillus paralichenif ormis
Bacillus cereus biov ar anthracis CI
Clostridium clariflavum
Bacillus anth racis H9401
Bacillus selenitiredu cens
Paenibacillus sp. JDR-2
Candidatus Arthromitus sp . SFB-rat-Yit
Candidatus Desulforudis auda xviator
Geobacillus the rmodenitrificans
Anoxybacillus flavithe rmus
Bacillus pseud ofirmus
Phosphorelay's elements
H-kinase
Spo0F
Spo0B
SPOB_a
Spo0A
SPo0A_C
KipI
Rap
Spo0E
Sda
Spore former
-
28
4. Definición del problema
En el año 2001, Lu y colaboradores publicaron en su artículo Oceanobacillus iheyensis gen.
nov., sp. nov., a deep-sea extremely halotolerant and alkaliphilic species isolated from a depth
of 1050 m on the Iheya Ridge el medio y las condiciones en las que Oceanobacillus iheyensis
esporula. Sin embargo, pese a que se replicó el medio PY (Peptone Yeast Extract broth)
suplementado junto con las condiciones reportadas por Lu et al. (2001) en el laboratorio de
Genómica computacional del IBT-UNAM Camus Morelos, Oceanobacillus iheyensis no obtuvo
crecimiento alguno.
Por tal motivo se formularon tres medios alternos con la finalidad de obtener las condiciones
para fomentar el crecimiento e inducir a esporulación de manera más rápida y eficiente, ya que
esto permitirá diseñar experimentos que puedan controlar la respuesta de las vías de
señalización que O. iheyensis emplea para esporular. Los tres medios formulados fueron LB
suplementado con sales, Agua del golfo de México y Sales marinas. La formulación de los tres
medios se encuentra detallada en la metodología de este documento.
-
29
5. Justificación
La cascada del inicio de la esporulación ha sido estudiada a nivel experimental ampliamente
en pocos bacilos como B. subtilis, así como en algunas Clostridias. Estudios iniciales indicaron
que sólo los bacilos tienen un sistema de fosforrelevo para inducir al regulador maestro de la
esporulación Spo0A. El reciente descubrimiento de nuestro grupo Martinez- Amador et al.
2019 y lo reportado por Davidsons et al., 2018, proponiendo la presencia de un fosforrelevo
en especies de Clostridias, incentivaron a ambos grupos a demostrar si este fosforrelevo es
funcional en las especies que lo poseen. Motivados por esto y dado que la Oceanobacillus
iheyensis HTE831 posee este fosforrelevo con una versión reducida de dominios de proteína,
que identifican a la proteína Spo0B, nuestro interés es encontrar en primera instancia las
condiciones que promueven la esporulación en este organismo halotolerante para
eventualmente implementar técnicas de clonación que permitan modificar genéticamente a
esta especie. Adicionalmente, este bacillo como otros formadores de esporas son de gran
interés industrial por producir enzimas de alta demanda entre las que se encuentran las
proteasas alcalinas (Purohit y Singh, 2013), y otras como nicotinamidasas (Sánchez Carrón et
al., 2013), amilasas, celulasas, fitasas, esterasas, fosfolipasas y DNAsas (Fragoso et al.,
2014), que en el caso de organismos marinos se ha visto que toleran mejor condiciones
extremas. En este trabajo se analizarán los medios formulados para evaluar el crecimiento y
esporulación de Oceanobacillus iheyensis HTE831. La identificación de estas condiciones
permitirá establecer limitantes del crecimiento, factor importante tanto para su manipulación
molecular, así como para la producción de metabolitos de interés industrial, en condiciones de
esporulación o de crecimiento vegetativo.
-
30
6. Objetivo general
• Establecer las condiciones de crecimiento y esporulación para la bacteria marina
Oceanobacillus iheyensis.
6.1. Objetivos particulares
• Estandarizar al menos un medio de cultivo dónde pueda crecer Oceanobacillus
iheyensis y se observen colonias.
• Estandarizar al menos un medio de cultivo dónde Oceanobacillus iheyensis entre en
fase de esporulación en un periodo menor a 72 horas.
7. Hipótesis
La esporulación en Oceanobacillus iheyensis se puede inducir de manera mas rápida y
eficiente en condiciones de laboratorio cultivándola en medios distintos al de Peptone Yeast
Extract Broth (PY).
-
31
8. Metodología
8.1 Cepas utilizadas.
La cepa utilizada fue Oceanobacillus iheyensis HTE831, que fue donada al grupo de Genómica
Computacional del IBT-UNAM Campus Morelos por el grupo del Doctor Jie Lu en 2005. Desde
entonces, la cepa se ha preservado en glicerol al 15% en crioconservación (-75 ºC). .El objetivo
de la crioconservación, es lograr reducir su metabolismo, como temperatura y nutrientes .Esto
nos permite al menos tener una sobrevivencia del 70% al 80% de células vivas y permanezcan
genéticamente estables. Por ello cuando se requiere hacer uso de las cepas en estas
condiciones, no se descongela sino se toma una alícuota congelada, y esto se lleva a cabo
con una asa de siembra incandecente. De la muestra preservada Oceanobacillus iheyensis,
se tomó una alícuota congelada con ayuda de un asa de siembra incandescente. Esto se
realiza con el objetivo de no descongelar el glicerol, ya que ciclos repetidos de congelación y
descongelación pueden reducir la viabilidad de las células. La alícuota congelada se sembró
en cajas Petri con medio LBs como en medio de cultivo Sales marinas sin antibiótico, las cuales
se incubaron a 30 ºC durante 72 horas. Se tomaron tres muestras por un periodo de 24, 48 y
72 horas. El tamaño de la muestra fue de 5 µL en cada tiempo y se observó in vivo al
microscopio de contraste de fases (OLYMPUS BX41). Para hacer la observación al
microscopio se utilizó el objetivo de inmersión (100x). Para ello se coloca sobre el cubre
objetos una gota de aceite de inmersión. Para corroborar la ausencia de contaminación por
otros microorganismos, la cepa se tipificó utilizando la técnica de PCR con oligonucleótidos
diseñados en este trabajo y descritos a continuación.
8.2 Diseño de oligonucleótidos.
Para verificar que Oceanobacillus iheyensis fuera el único organismo presente, se diseñó un
par de oligonucleótidos específicos, capaces de ser usados para amplificar el gen ribosomal
16S. Para ello, se descargó el genoma completo de O. iheyensis HTE831, así como su gen
ribosomal 16S, del Centro Nacional de Información Biotecnológica (National Center
Biotechnology Information, NCBI), en formato GeneBank. El diseño de los oligonucleótidos se
realizó manualmente, utilizando el programa SnapGene Viewer 4.3.10 para determinar la Tm.
-
32
8.3 Análisis de la especificidad de los oligonucleótidos diseñados.
Para evaluar la especificidad de los oligonucleótidos diseñados, se realizó un análisis
bioinformático usando el programa Nucleotide BLAST (Altschul et al., 1990), para encontrar
las regiones de similitud entre las secuencias nucleotídicas contenidas en la base de datos de
NCBI. Una vez realizada la búsqueda y la alineación, se descargó y analizó la Hit Table (text)
en cada uno de los casos.
8.4 PCR preliminar y electroforesis
Con los oligonucleótidos específicos diseñados, mediante la técnica de PCR se llevó a cabo
la obtención del amplicón. Esta muestra fue tomada del cepario de Oceanobacillus iheyensis
de nuestro laboratorio en crioconservación. Se colocó una alícuota preservada en
crioconservación en un tubo de PCR y se preparó la reacción para obtener un volumen final
de 30 µL. La mezcla contenía lo siguiente:
Tabla 2.1 Concentraciones, volúmenes y sustancias del PCR preliminar
Sustancia Volumen Concentración
MgCl2 3 µL 2.0 mM
Buffer de reacción 3 µL 10X
dNTPs 1 µL 10 mM
Taq Polimerasa 1 µL 1U/µL
Oligonucleótido directo OIMP1 1 µL 10 µM
oligonucleótido reverso OIMP2 1 µL 10 µM
Agua 20 µL --
Todos los reactivos se colocan en un tubo específico para la técnica y junto con las condiciones
adecuadas que se necesite, se somete a ciclos repetidos de calentamiento enfriamiento que
permitan la síntesis de DNA. mezcla se colocó en la zona media de la placa de calentamiento
del termociclador y se sometió a las condiciones indicadas en la tabla 2.2.
-
33
Tabla 2.2 Condiciones del PCR preliminar
Temperatura Tiempo
94 ºC 4 minutos
94 ºC 30 segundos
25 X 60 ºC 30 segundos
72 ºC 2 minutos
72 ºC 10 minutos
Se preparó una solución de agarosa al 1%, se almacenó en un horno a 65 ºC, con la finalidad
de mantener fundida la agarosa. En un tubo Falcon de 50 mL, se vertieron 30 mL de la agarosa
líquida y se adicionaron 2 µL de HYDRA Green. Una vez obtenidos los productos de PCR, se
realizó una electroforesis en un gel de agarosa al 1% por una hora a 250 mA, se utilizó el
marcador de peso molecular GeneRulerTM DNA Ladder Mix de Thermo Fisher Scientific (cat.
SM0334). Las muestras se prepararon en una placa, colocando 2 µL de tampón de carga por
14 µL de muestra de cada uno de los productos de PCR, y se depositaron una por pocillo. Una
vez que ha terminado la separación de las muestras, el gel previamente teñido con el
intercalador de DNA, se coloca bajo la luz UV. Los fragnmentos de DNA brillan por lo nos
permite observar los tamaños esperados.
8.5 Formulación de medios, siembra y observación en el microscopio de contraste de
fases
Se formularon cuatro medios diferentes: 1) medio PY suplementado (Lu et al., 2001) (peptona
1%, NaCl 3%, extracto de levadura 0.5%, K2HPO4 0.01%, MgSO4 ∗ 7H2O 0.02%, pH=8); 2) LB
suplementado (LBs) (triptona 1%, NaCl 3%, extracto de levadura 0.5%, 𝐾2𝐻𝑃𝑂4 0.01%,
MgSO4 ∗ 7H2O 0.02%, pH=8); 3) Sales marinas (triptona 0.5%, extracto de levadura 0.5%,
Sales marinas, 1/10 v/v de sulfatos [stock 130 mM], 1/100 v/v de NH4Cl [stock 50mM]), se filtró
antes de su inoculación y posterior esterilizado debido a la formación de cristales; 4) Agua del
Golfo de México (Agua del Golfo de México filtrada con un filtro de 0.05 µm, extracto de
levadura 0.05%, 1/10 v/v de sulfatos [stock 130 mM], 1/100 v/v de NH4Cl [stock 50mM]). Se
prepararon 125 mL de cada uno de los medios y se esterilizaron en autoclave a 121 ºC y 21
psi durante 21 minutos. Cuando se requirió medio sólido, a la mezcla se añadieron 15 g de
agar por litro de medio.
-
34
Para el crecimiento bacteriano en medio líquido, se utilizó una campana de flujo laminar, junto
a un mechero Fisher, se tomó una alícuota de la cepa de interés, Oceanobacillus iheyensis,
en previa crioconservación perteneciente al cepario del IBT-UNAM campus Morelos, y se
inocularon 50 mL de cada uno de los medios por triplicado. Se incubaron a 30ºC con 250 rpm
durante 24 y 48 horas. Se tomó una alícuota de los medios LB suplementado, Sales marinas
y Agua del Golfo de México y se observó bajo el microscopio de contraste de fases in vivo,
con el objetivo de inmersión (100x). Con la finalidad de evaluar el efecto de los diferentes
medios en la morfología bacteriana, así como descartar posible contaminación, una vez que
habían pasado las 48 horas, del cultivo LBs se tomó 1 mL y se inocularon 125 mL de medio
fresco de Sales marinas. De igual manera, se tomó 1 mL de cultivo de Sales marinas y se
inocularon 125 mL de LBs. Pasadas 24 horas seguidas a la inoculación, se tomaron 5 µL de
ambos cultivos y se observaron en el microscopio óptico de contraste de fases con el objetivo
de inmersión (100x). Así mismo, se tomó otra alícuota de ambos cultivos para confirmar que
la bacteria Oceonobacillus iheyensis fuese la presente en los medio medios y se procedió a
hacer nuevamente la técnica de PCR para obtener el amplicón con los oligonucleótidos
específicos.
La siembra en medio sólido se llevó a cabo en una campana de flujo laminar, se tomó una
alícuota congelada de la cepa Oceanobacillus iheyensis en crioconservación con un asa de
siembra incandescente, y se estrió en la superficie de las placas de los medios sólidos de
Sales marinas y LBs. Las cajas se incubaron por 48 horas a 30 ºC.
8.6 Extracción de DNA total y PCR
Con un cultivo fresco de 24 horas de los medios LBs, Agua del Golfo de México y Sales
marinas, se realizó una extracción de DNA total con el kit GeneJet Genomic DNA Purification
de Thermo Scientific. Con el DNA extraído se preparó una mezcla para una reacción de PCR
con las mismas concentraciones y condiciones del PCR previamente descrito. Los productos
de PCR obtenidos se corrieron en un gel de agarosa al 1% por 1 h a 250 mA, utilizando el
marcador de peso molecular GeneRulerTM DNA Ladder Mix de Thermo Fisher Scientific
-
35
8.7 Tinción de esporas (método de Scheaffer-Fulton)
De los medios Sales minerales y LBs, incubados a 30 ºC por 48 y 72 horas, se tomó una
alícuota de 1mL, se centrifugó y se resuspendió en 1 mL de Tween 20 al 97%, repitiendo este
proceso 3 veces, de esa muestra se tomó una alícuota para realizar una dilución hasta
alcanzar una DO600 de 0.03 en Tween 20 al 97%. Se realizaron 3 lavados con Tween 20 al
97%, se resuspendió en Tween 20 al 97%. Se tomaron 2 µL de cada muestra y se colocaron
en un portaobjetos limpio. Se dejó secar a temperatura ambiente. La parrilla de calentamiento
se ajustó a 80 ºC, se colocó un recipiente alto con un poco de agua de grifo y con una rejilla
sobre de él. Una vez que el agua inició el proceso de evaporación, se colocó el portaobjetos
con las muestras, impidiendo durante todo el proceso la ebullición. La muestra se cubrió por
completo con solución de verde de malaquita al 5%, se dejó reposar 15 minutos en el vapor,
sin permitir que la muestra se secase, por lo que se añadió por medio de goteo, solución de
verde de malaquita en el porta objetos cuando era necesario. Una vez transcurridos los 15
minutos, el portaobjetos se retiró del baño de vapor y se enjuagó el exceso de colorante con
agua de grifo y se dejó enfriar. Una vez que alcanzó. La temperatura ambiente, se tiñó con
solución de safranina (la misma utilizada para la tinción de Gram), se dejó actuar con el
colorante por 3 minutos, se retiró el exceso con agua de grifo, se dejó secar y se observó la
muestra al microscopio óptico de contraste de fases con el objetivo de inmersión (100x).
-
36
9. Resultados
9.1 Diseño de oligonucleótidos
El gene 16S ribosomal de Oceanobacillus iheyensis HTE831 tiene un tamaño de 1565 pb,
cuenta con el 53% de GC% y presenta 7 copias en el genoma bacteriano, 6 copias en la
cadena directa y una en la cadena reversa, según el análisis realizado en el programa
SnapGene Viewer 4.3.10 (GSL Biotech LLC). En la Figura 13 se aprecia el número de copias
del gene 16S ribosomal, así como la localización de los oligonucleótidos diseñados dentro del
genoma de O. iheyensis HTE831. El oligonucleótido directo se nombró como OIMP1 (5’– GTC
AGA AGT TGA CTT CTG AAG CAC AAG AAA CAC AAC TTT TAT GG–3’), y el oligonucleótido
reverso se nombró como OIMP2 (5’– CAA CCA AGT ACG ATT CCG TAA TAA TCC TTA GAA
AGG AGG TG –3’).
Figura 13. Localización de los oligonucleótidos OIMP1 Y OIMP2, y las siete copias del gene
16S ribosomal, seis en la cadena directa y una en la cadena reversa en el genoma de
Oceanobacillus iheyensis HTE831. La figura se generó con el software SnapGene Viewer
4.3.10.
-
37
En la Figura 14 A se observa como los oligonucleótidos OIMP1 y OIMP2 flanquean una de las
siete regiones del 16S ribosomal dentro del genoma de O. iheyensis. En las figuras 14 B y 14
C, se aprecia el sitio de hibridación de los oligonucleótidos al DNA sin ningún mistmach.
Figura 14. (A) Sitio de hibridación del par de oligonucleótidos diseñados en los flancos del gen
16S ribosomal. (B) Sitio de unión al gen 16S ribosomal del oligonucleótido OIMP1. (C) Sitio de
unión al gen 16S ribosomal del oligonucleótido OIMP2.
A
B
C
-
38
9.1.1 Análisis de similitud de los oligonucleótidos OIMP1 y OIMP2
El análisis de similitud del oligonucleótido OIMP1 utilizando la herramienta BLAST (Altschul et
al., 1990), presentó homología con el genoma de un solo organismo, Oceanobacillus iheyensis
HTE831, en siete distintos sitios dentro del cromosoma. En la Figura 15 se muestran los
alineamientos correspondientes a cada uno de los homólogos encontrados. Se observa que
el locus inicial de cada una de los homólogos es el mismo al locus del oligonucleótido OIMP1
anotado en el genoma en SnapGene Viewer 4.3.10. Se observa que la identidad es del 100%
en 6 de los alineamientos, y en uno de ellos la identidad es de 98% debido a la presencia de
un mistmach. El valor esperado (e-value) que presentan los alineamientos es menor a cero,
por indicando que el resultado es estadísticamente significativo.
-
39
Figura 15. Alineamiento de la secuencia de OIMP1 con los hits 1 a 7 del análisis de similitud.
-
40
Para el análisis se utilizó el programa BLAST, el análisis del oligonucleótido OIMP2 tuvo
valores de identidad con el genoma de dos microorganismos, Oceanobacillus iheyensis
HTE831 y con Sporosarcina psychrophila strain DSM 6497; presentó dos homólogos del gen
16S ribosomal, en Virgibacillus salexigens; y homología con una secuenciación parcial de una
bacteria no cultivable. En la figura 15 se muestran los alineamientos del oligonucleótido OIMP2
con los cinco resultados obtenidos por el algoritmo con el genoma de Oceanobacillus ihyensis
HTE831, en todos los hallazgos, el porcentaje de identidad es del 100%, no presenta gaps y
los valores esperados fueron iguales a 10-11, siendo estos resultados estadísticamente
significativos. Se observa por otro lado, diferencias en los valores de cobertura. En la Figura
16 se observan los alineamientos de OIMP2 contra el genoma de Sporosarcina psychrophila
strain DSM 6497, en donde únicamente 33 pb de las 41 pb del oligonucleótido fueron
alineadas, presentado un gap.
Figura 16. Alineamiento de la secuencia de OIMP2 contra las coincidencias 1 a 5 del genoma
de Oceanobacillus iheyensis HTE831
En las figura 17 se observan los alineamientos de OIMP2 frente al genoma de Sporosarcina
psychrophila strain DSM 6497, en donde únicamente se complementa 33 pb de las 41 pb del
oligonucleótido, encontrando en todos los alineamientos un gap. El e-value es cercano a cero,
por lo que los hallazgos no se deben al azar.
-
41
Figura 17. Alineamiento de la secuencia de OIMP2 con los hits 1 a 10 del genoma de
Sporosarcina psychrophila strain DSM 6497
El oligonucleótido OIMP2 obtuvo dos coincidencias de reportes de Virgibacillus salexigens de
la secuencia parcial y completa de los genes 16S y 23S ribosomales. En las figura 18 se
muestran las coincidencias encontradas por el algoritmo. En ambas, la identidad es del 100%,
sin embargo únicamente las pares de bases del oligonucleótido que se alinean con la
secuencia de Virgibacillus salexigens son 28, las secuencias complementa sin gaps; el valor
esperado es igual a 10-5, por lo que puede considerarse como estadísticamente significativo.
Figura 18. Alineamiento de las secuencias de OIMP2 contra las coincidencias 1 y 2 del genoma
de Virgibacillus salexigens con la secuencia con ID EU723666.1
-
42
La última coincidencia fue con la clona no cultivable SWFe-06 con un solo alineamiento (Figura
19). Las pares de bases del oligonucleótido que coinciden con la secuencia del genoma de la
clona no cultivable SWFe-06 fueron 29 de 41. La identidad de las 29 pares de bases fue del
100%, sin gaps, y con un valor esperado igual a 10-5 lo que refiere que la búsqueda no se
debió al azar. Es importante destacar que los valores esperados son estadísticamente
significativos, para todos los resultados el valor de cobertura indica que nuestros diseños se
corresponde a una identidad completa con la bacteria Oceanobacillus iheyensis HTE831.
Figura 19. Alineamiento de la secuencia de OIMP2 contra la con el hit del genoma de la clona
no cultivable SWFe-06
Las tablas 3.1 y 3.2 contienen los datos de la Hit Table (text) descargada de la página de
BLAST de los a análisis bioinformáticos de OIMP1 y OIMP2. La tabla brinda información de
cada uno de los alineamientos realizados por el algoritmo como: nombre de la secuencia
problema; el ID de la secuencia con la que el algoritmo alineó la secuencia problema; el
porcentaje de similitud entre ambas secuencias; el número de pares de bases de la secuencia
problema que se alineó con la secuencia encontrada por el algoritmo; las inserciones o
deleciones detecta