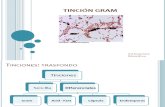
Cocos Gram Negativos Curso AulaMIR 2011 Pedro Alarcón Blanco.
Tinción gram 2011
Transcript of Tinción gram 2011

METODOS DE METODOS DE OBSERVACION DE LOS OBSERVACION DE LOS MICROORGANISMOSMICROORGANISMOS
DEPARTAMENTO DE DEPARTAMENTO DE MICROBIOLOGIAMICROBIOLOGIA

Observación microbiana
• En vivo: exámen en fresco de una suspensión bacteriana, se usa principalmente para visualizar Hongos unicelulares, protozoos y helmintios.
• Ayuda a observar movimiento y forma de los Mo,s

•Preparado coloreado: frotis o extendido que al ser teñido permite visualizar la forma, tamaño y disposición de los diferentes tipos de bacterias o la observación de elementos no habituales (flagelos, cápsula ó esporas).

Técnica (observación in vivo)
• Colocar parafina o vaselina en los bordes del cubreobjeto.
• Depositar una gota en el cubreobjetos
• Cubrir con el cubreobjetos primero desde una arista al total de la superficie.
• Observación.
• Desventajas: falta de contraste y resolución,

Técnica ( observación coloreada)
• Con un portaobjeto limpio y desgrasado y con el asa y la pipeta se le coloca una gota de agua destilada estéril.
• Se toma con el asa y se coloca en el portaobjeto y se le homogeniza con el agua estéril,
• Se extiende la muestra sin tocar los cuatro bordes del cubreobjetos
• Se deja que el portaobjeto se seque al aire o se le mantiene a 40 cm de la llaman y se fija
• La fijación tiene el objeto de que las bacterias queden adheridas al vidrio.

fijación
• Existen dos métodos:• 1. Método de Koch (físico):• Consiste en hacer tres pasajes lentos sobre
el mechero dejando enfriar entre cada uno de ellos.
• 2. Metanol (químico): • Extendido con alcohol metílico por 5
minutos y despues colorear

Colorantes
• Productos químicos derivados del Alquitrán, especialmente el benceno
• La molécula del colorante está formada por dos segmentos el Cromóforo y el auxócromo, el primero tiene color y el segundo la afinidad
• La afinidad esta dada por la disociación electrolítica de este segmento y la formación de sales insolubles con las proteínas, glucoproteínas y lipoproteinas de los tejidos y paredes.

• El grupo auxocromo determina que se los clasifique en básicos o catiónicos, ácidos o aniónicos.
• Colorantes Básicos: violeta de Genciana, Fucsina básica, rojo neutro, etc.
• Colorantes Acidos: Fucsina ácida, eosina
• Neutros: eosianato de azul de metileno.

Coloración Simple
• Son las que emplean un solo colorante y tiñen todos los elementos por igual.
• Técnica: fijar, cubrir, lavar y observar
• Ventajas: Observ. Rápida y sencilla de la morfología bacteriana.
• Desventajas: no es posible diferenciar si la muestra es monoespecífica o mixta.

Compuestas o diferenciales
• Usan dos colorantes lo que permite teñir de distintos modos las diversas clases de bacterias, los métodos más empleados son:
• Tinción de Gram. y de Ziehl-Neelsen
• En estas coloraciones se usan cuatro componentes de manera progresiva:

• 1. Colorante principal o primario: colorante básico que al entrar en contacto con las células cargadas negativamente las colorea
• 2. Mordiente: le da mas intensidad y más fijación (sales metálicas, solución yodada o lugol, taninos y fenol)

• 3. Agente decolorante: Disolvente orgánico como el alcohol, ácido o alcohol acetona
• 4. Contracolor o colorante secundario:
• Colorante básico de distinto color que el primero.

Tinción de Gram
• Utilizada más habitualmente
• Facilita la observación bacteriológica
• Permite diferenciar entre gram positivo y gram negativo.

Fundamento
• La afinidad por el color depende en gran medida de la composición química de la pared celular
• Después de realizar los primeros cuatro pasos, todas las bacterias se ven color violeta.
• Al finalizar la técnica las que conservan el color violeta se denominan Gram Positivas
• Y las que no lo conservan Gram Negativas.

Cont. fundamento
• Los decolorantes orgánicos utilizados abren los poros de la membrana externa de las bacterias gram negativas (constituidas principalmente por lipoproteínas y lipopolisacáridos) y permiten la salida del colorante principal quedando desprovistos de color.
• Al agregar el contracolor éstos quedan teñidos de rojo (fucsina o safranina).

Diferencias estructurales

Técnica
1. Una vez fijado el extendido cubrir la superficie con cristal violeta (colorante primario) y dejar en contacto un minuto
2. Lavar con agua abundantemente.
3. Cubrir con Lugol(mordiente) por 1 minuto.
4. Lavar con abundante agua

Cont. Tinción de gram.
• Inclinar el portaobjeto y dejar gotear el alcohol acetona (decolorante) hasta que el preparado deje de perder color.
• Lavar con agua
• Agregar el (contracolor) fucsina básica por 1 minuto
• Lavar, secar al aire, observar.







Ventajas y desventajas
• Es un método rápido y sencillo
• Permite observar: forma, tamaño y disposición.
• Hace diferenciación entre biota mixta o monoespecífica
• Proporciona orientación terapéutica.
• Se conservan los preparados.
• Gram. + vrs. Gram -
• Algunas micobacterias y hongos pueden no tomar la coloración
• Bacterias sin pared las tiñe débilmente (mollicutes)
• La técnica es más laboriosa que la técnica simple.

Otras tinciones
• Coloración de Zielh Nielsen:• Bacterias del género Mycobacterium, la
especie Nocardia, las especies Corynebacterium y ocasionalmente actinomicetos no se tiñen con la coloración Gram.
• Estas bacterias tiene la capacidad de resistir la decoloración por ácidos y alcohol

Cont. Otras tinciones
• Esta propiedad se debe al alto contenido de lípidos complejos (ácidos micólicos) y ceras que poseen algunos microorganismos en su pared celular.
• Acido Alcohol resistentes (AAR): Mo,s que resisten la decoloración se ven de color rojo.
• No Acido Alcohol resistentes (No AAR):• No resisten la acción de los decolorantes y se ven
de color azul.


Coloración de Giemsa
• Utilizada para la diferenciación intra y extracelular de parásitos en sangre circulante. (plasmodium y especies de Leishmania, Candida, Hisptoplasma capsulatum, y Pneumocystis carinii, inclusiones virales, Mollicutes, Rickettsia y Chlamydia.
• Se observan también los elementos celulares de la respuesta inflamatoria.

• La Cápsula: Por sus características químicas no se tiñe con colorantes básicos para ello se utiliza la Tinción negativa o indirecta.
• No tiñe sino que se deposita alrededor resaltando los contornos.
• Se utiliza Tinta china (suspensión de partículas de carbón coloidal) Moléculas grandes que no entran en la cápsula.
• La utilidad de esta técnica es que revela cápsulas bacterianas y micóticas.




Tinción de endosporas
• Sin teñir se ven como estructuras refringentes intracelulares
• Con la tinción de gram se ven como zonas incoloras dentro de las células teñidas
• Con calor + verde de malaquita y safranina. (El calor permite la penetración del del colorante).


Tinción de flagelos y cilios
• Fuera del poder de resolución del microscopio óptico común por delgadas.
• Para verlos se agrega una suspensión coloidal de sales de ácido tánico (mordiente)
• Formara un precipitado que engrosara el tamaño de las estructuras
• Se aplica fucsina ácida y se visualizan como estructuras rojas.