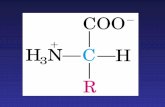
Valina Histidina y Arginina
-
Upload
anicama-perez-brenda -
Category
Documents
-
view
116 -
download
0
Transcript of Valina Histidina y Arginina

AMINOÁCIDOS: VALINA, HISTIDINA Y ARGININA 2010
Dedicatoria:
A los profesionales de la Salud, que día a día contribuyen y velan por el bienestar de la
población peruana.
Bioquímica 1

AMINOÁCIDOS: VALINA, HISTIDINA Y ARGININA 2010
Los aminoácidos (aa) son moléculas orgánicas pequeñas con un grupo amino (NH2) y un grupo carboxilo (COOH). La gran cantidad de proteínas que se conocen están formadas únicamente por 20 aa diferentes. Se conocen otros 150 que no forman parte de las proteínas.
Generalmente, el número de AA que forman una proteína oscila entre 100 y 300. Los enlaces que participan en la estructura primaria de una proteína son covalentes: son los enlaces peptídicos. El enlace peptídico es un enlace amida que se forma entre el grupo carboxilo de una AA con el grupo amino de otro, con eliminación de una molécula de agua. Independientemente de la longitud de la cadena polipeptídica, siempre hay un extremo amino terminal y un extremo carboxilo terminal que permanecen intactos.
Para el presente trabajo, hablaremos únicamente de 3 aminoácidos: La Valina, Histidina y Arginina. Esperamos que tomen mucha atención a las siguientes páginas para mayor conocimiento y avance en nuestra carrera profesional.
Bioquímica 2

AMINOÁCIDOS: VALINA, HISTIDINA Y ARGININA 2010
DESCRIPCIÓN:
La valina (abreviada Val o V) es uno de los 20 aminoácidos naturales más comunes en la Tierra, cuya fórmula química es HO2CCH(NH2)CH(CH3)2. En el ARN mensajero, está codificada por GUA, GUG, GUU o GUC. Nutricionalmente, en humanos, es uno de los aminoácidos esenciales. Forma parte integral del tejido muscular, puede ser usado para conseguir energía por los músculos en ejercitación, posibilita un balance de nitrógeno positivo e interviene en el metabolismo muscular y en la reparación de tejidos).
Estructura química de la valina.
La Valina es la responsable de una enfermedad genética conocida como Anemia falciforme, la persona que la padece tiene un tipo de hemoglobina especial llamada Hemoglobina S, que hace que los glóbulos rojos tengan una forma de hoz en vez de tener la tradicional forma de plato, y que tengan una vida media entre 6 y 10 veces menor, causando anemia y otras complicaciones.
La anemia falciforme se produce por una mala codificacion de la hemoglobina, sustituyendo por valina el Ácido glutámico que debería ir.
Bioquímica 3

AMINOÁCIDOS: VALINA, HISTIDINA Y ARGININA 2010
BIOSÍNTESIS.
Valina es un aminoácido esencial, por lo que debe ser digerido, normalmente como un componente de proteínas. Es sintetizado en plantas a través de muchos pasos a partir del Ácido pirúvico. La cascada inicial también termina en Leucina. El intermediario, ácido α-oxoisovalerianico, pasar por una aminación con glutamato. Enzimas involucradas en la biosintesis incluyen:1
Acetolactato Sintasa Ácido acetohidroxi isomeroreductasa Dihidroxi-ácido deshidratasa Valina aminotransferasa
Es un aminoácido hidrofóbico de cadena alifática, ramificado con grupo R isopropilo no polar (Ruta 12). La valina, junto con la isoleucina, se sintetiza por medio de reacciones que las llevan a cabo el mismo grupo de enzimas. Es considerado como un aminoácido esencial. Una de sus ramas está formada por un grupo metilo. Tiene una estructura tan similar a la leucina e isoleucina que incluso se ha comprobado que en ocasiones se reemplazan entre sí en determinadas posiciones.
Esquema tridimensional de la Valina.
Bioquímica 4

AMINOÁCIDOS: VALINA, HISTIDINA Y ARGININA 2010
Las rutas biosintéticas de estos tres aminoácidos comparten determinados pasos en plantas y microorganismos y las primeras reacciones catabólicas en los mamíferos se realizan por los mismos enzimas, luego las reacciones son diferentes y es entonces cuando se producen los diferentes productos que van a determinar el tipo de degradación, que en el caso de la valina es glucogénica.
El compuesto insaturado derivado de la valina, el metilacrilil-CoA se hidrata y forma b-hidroxiisobutiril CoA, éste se hidroliza de la CoA y el hidroxilo resultante se oxida a aldehido por medio de una enzima deshidrogenasa, formándose el semialdehído metilmalónico. El aldehido se oxida por una deshidrogenasa dependiente de NAD, formándose un tioéster. En esta reacción se produce propionil CoA.
La valina aminotransferasa, enzima que interviene en el catabolismo de la valina, está sobre todo en tejidos extrahepáticos, en especial en el tejido muscular.
PATOLOGÍAS RELACIONADAS CON LA VALINA
Cuando estos aminoácidos se encuentran en exceso en función de la síntesis proteica, son transaminados con a-cetoglutarato para dar lugar a a-cetoácidos ramificados. Si este primer paso no ocurre con normalidad pueden darse algunos trastornos que en neonatos se suele manifestar como acidosis, por ejemplo, hipervalinemia cuya causa principal es la deficiencia del complejo enzimático de la deshidrogenasa de cetoácidos ramificados.
Bioquímica 5

AMINOÁCIDOS: VALINA, HISTIDINA Y ARGININA 2010
DESCRIPCIÓN:
Aminoácido cuya cadena lateral R tiene una naturaleza polar hidrófila básica (ver Ruta 20). La histidina es un aminoácido proteinogénico esencial en los animales, sin embargo en el hombre sólo se detectan alteraciones producidas por su déficit cuando éste se prolonga en el tiempo, por lo tanto es no esencial. En niños es necesario el aporte por alimentación.
Estructura química de la histidina.
La ruta principal de su degradación da lugar al glutamato. En su primer paso de degradación aparece el amoniaco con formación de doble enlace.
La descarboxilación de este aminoácido da lugar a la histamina, su amina correspondiente que tiene lugar sobre todo en los mastocitos. Ésta se segrega en diferentes situaciones.
Bioquímica 6

AMINOÁCIDOS: VALINA, HISTIDINA Y ARGININA 2010
Existen dos péptidos que contienen histidina: la carnosina y la anserina, no obstante, se desconoce el papel que juegan estos péptidos en el músculo, donde se encuentran.
BIOSÍNTESIS DE LA HISTIDINA.
La síntesis de la L-hbistidina es un proceso complejo que involucra nueve enzimas, en el se forma el anillo imidazol, cuya síntesis parte del ATP y de fosforribosilpirofosfato. Suele admitirse que la L-histidina es un aminoácido esencial para el adulto.
Mediante medición del equilibrio del nitrógeno en un periodo coro, se ha concluido que no lo es; resulta posible que compuestos derivados de la L-histidina (carnosina y anserina) se utilicen para satisfacer las necesidades de L-histidina a corto plazo.
Cinco de los seis átomos de la histidina derivan del 5-fosforribosil--pirofosfato (PRPP) un intermediariop también implicado en la biosíntesis del triptófano. El sexto carbono de la histidina se origina del ATP. Los átomos del ATP que no se incorporan a la histidina son
Bioquímica 7

AMINOÁCIDOS: VALINA, HISTIDINA Y ARGININA 2010
eliminados como 5-aminoimidazol-4-carboxamida ribonucleótido, que es también un intermediario en la biosíntesis de las purinas.
Catabolismo de la Histidina
El catabolismo de la histidina comienza con la liberación del grupo α-amino catalizado por la histidasa, introduciendo un doble enlace en la molécula. Consecuentemente, el producto deaminado, urocanato, no es el usual α-cetoácido asociado con la pérdida de α-amino nitrógenos. El producto final del catabolismo de la histidina es glutamato, haciendo a la histidina uno de los aminoácidos glucogénicos.
Otra característica dominante del catabolismo de la histidina es que sirve como fuente de nitrógeno para combinarse con el tetrahidrofolato (THF), produciendo el intermediario 1-carbono THF conocido como N5-formimino THF. La última reacción es una de las dos rutas a N5- formiminoTHF.
La principal deficiencia genética asociada con el metabolismo de la histidina es la ausencia o deficiencia de la primera enzima de la vía, la histidasa. La histidinemia resultante es relativamente benigna. La enfermedad, que es de relativa alta incidencia (1 en 10.000), es más fácilmente detectada por la ausencia de urocanato de la piel y del sudor, donde se encuentra normalmente en abundancia relativa.
La decarboxilación de la histidina en el intestino por las bacterias da lugar histamina. Igualmente, la histamina se presenta en muchos tejidos por la decarboxilación de la histidina, que causa en exceso constricción o dilatación de varios vasos sanguíneos. Los síntomas generales son asma y varias reacciones alérgicas.
Bioquímica 8

AMINOÁCIDOS: VALINA, HISTIDINA Y ARGININA 2010
PATOLOGÍAS RELACIONADAS CON LA HISTIDINA.
La enzima que degrada la histidina para dar lugar al urocanato es la histidasa y su deficiencia se asocia con una enfermedad llamada histidinemia.
La histidina es uno de los 22 aminoácidos derivados de los alimentos con alto contenido de proteínas, así como ciertos granos. Es uno de los aminoácidos aromáticos que comienzan siendo un aminoácido esencial en los niños humanos, pero más tarde convertido en un aminoácido no esencial que el cuerpo empieza a sintetizar a partir de imidazol, un compuesto orgánico y el componente del anillo aromático en el ácido de la estructura química. La histidina es también un precursor de ciertas aminas y péptidos de aminoácidos, como la histamina y la carnosina. El nombre químico completo para esta sustancia se escribe como 2-amino-3-(1H-imidazol-4-il) del ácido propanoico, pero esto es a menudo abreviado a la L-histidina, la suya, o simplemente “H.”
Al igual que otros aminoácidos, la histidina se encuentra en casi todas las células del cuerpo, y está implicado en diversas funciones biológicas. Es clave para la formación de la vaina de mielina, la barrera protectora que rodea las células nerviosas y apoya la transmisión de las señales del cerebro a diferentes partes del cuerpo. También participa en la desintoxicación de metales pesados y otros residuos celulares para la eliminación a través del hígado y los riñones. Esta sustancia es necesaria para que el cuerpo para la
Bioquímica 9

AMINOÁCIDOS: VALINA, HISTIDINA Y ARGININA 2010
fabricación de blancos y glóbulos rojos. Por último, ya que este ácido está involucrado en la producción de histamina, que desempeña un papel en la toma de las enzimas gástricas necesarios para una buena digestión, ayudando al sistema inmunológico en respuesta a la presencia de alérgenos, y la promoción de la función sexual normal.
L-histidina es necesaria para permitir al cuerpo a metabolizar muchos minerales, como hierro, zinc, cobre y manganeso. Por ejemplo, en términos de utilización de hierro, es necesaria para producir ferritina y “Fur”, también conocida como la proteína de almacenamiento de hierro y la proteína de regulación de la absorción de hierro, respectivamente. La histidina es también necesaria para producir una variedad de enzimas, como la superóxido dismutasa antioxidante.
Hay pruebas que sugieren que los bajos niveles de histidina, o alteración del metabolismo, puede estar vinculado a una variedad de trastornos. Por ejemplo, los investigadores sospechan que una deficiencia puede llevar a un mayor riesgo para el desarrollo de la artritis reumatoide en algunas personas. Niveles anormalmente bajos también han sido relacionados con la pérdida de audición después de una lesión debida a la mielina especializados células de la vaina, llamados “células de Schwann,” no se haya iniciado la reparación de nervios dañados. Por el contrario, los altos niveles de este aminoácido se han relacionado con una mayor prevalencia de la depresión y los trastornos de ansiedad, así como la esquizofrenia.
Mientras que la suplementación con este aminoácido puede beneficiar a ciertos individuos, está contraindicado en otros. Por un lado, sus efectos sobre el sistema nervioso central y la regulación de la histamina sugieren que las personas con trastornos depresivos se debe evitar a menos que sea bajo instrucciones de un médico. Además, las personas con trastornos del riñón o del hígado no deben tomar este aminoácido en forma de suplemento.
Bioquímica 10

AMINOÁCIDOS: VALINA, HISTIDINA Y ARGININA 2010
LA HISTIDINA COMO TRATAMIENTO
Se encuentra abundantemente en la hemoglobina; se ha utilizado en el tratamiento de artritis reumatoide, enfermedades alérgicas, úlceras y anemia. Su deficiencia puede causar deficiencias en la audición.
En combinación con la hormona de crecimiento y otros aminoácidos, contribuye a la reparación de los tejidos, especialmente en el sistema cardiovascular.
DESCRIPCIÓN.
La arginina es uno de los 20 aminoácidos que se encuentran formando parte de las proteínas. En tejidos extrahepáticos, la arginina puede ser sintetizada en el ciclo de la ornitina (o ciclo de la urea). Se clasifica, en población pediátrica, como un aminoácido esencial. Este aminoácido se encuentra involucrado en muchas de las actividades de las glándulas endocrinas.
EMPLEO
La arginina es un aminoácido esencial, y puede estimular la función inmunológica al aumentar el número de leucocitos. La arginina está involucrada en la síntesis de creatina, poliaminas y en el ADN. Puede disminuir el colesterol para mejorar la capacidad del aparato circulatorio,2 así como estimular la liberación de hormona de crecimiento (somatropina),3 reducir los niveles de grasa corporal y facilitar la recuperación de los deportistas debido a
Bioquímica 11

AMINOÁCIDOS: VALINA, HISTIDINA Y ARGININA 2010
los efectos que tiene de retirar amoníaco (residuo muscular resultante del ejercicio anaeróbico) de los músculos y convertirlo en urea que se excreta por la orina.4 Se emplea en la biosíntesis de la creatina. Se suele encontrar en ciertos productos ergogénicos que contienen Óxido Nítrico (NO) ya que potencia los efectos vasodilatadores. Se ha comprobado que un exceso de L-arginina provoca problemas de páncreas en ratas.
La arginina es un aminoácido que se incluye en las dietas equilibradas de los gatos, su ausencia puede provocar serios trastornos relacionados con exceso de amoníaco en sus tejidos.
HISTORIA.
La arginina fue aislada por primera vez de extracto de semillas de lupino, en 1886 por el químico suizo Ernst Schulze. La arginina es un aminoácido que se utiliza en ingredientes de muchas cremas cosméticas, con la falsedad paradigmática de suponer que su aplicación epidérmica sería capaz de estimular la proteína y trasformarla en músculo. Muchos estudios han intentado sustraer de diversos modos la arginina de forma pura o en aceites, pero resulta complicado, ya que al igual que la Vitamina C y otros muchos sustratos, se destruye con el calor, entre 39 y 50 °C.
La arginina se encuentra en la gran mayoría de productos del mar, pescado, mariscos, crustáceos, grandes mamíferos acuáticos como lasballenas hacen un aceite con ellas, ese aceite es demandado por diversas empresas cosméticas por su contenido en arginina.
Bioquímica 12

AMINOÁCIDOS: VALINA, HISTIDINA Y ARGININA 2010
SÍNTESIS
La arginina se sintetiza de citrulina por acción secuencial de las enzimas citosólicas argininosuccinato sintetasa (ASS) y de laargininosuccinato liasa (ASL). Esto es energéticamente costoso, ya que la síntesis de cada molécula de argininosuccinato requiere la hidrólisis de adenosín trifosfato (ATP) a adenosín monofosfato (AMP); i.e., dos ATP equivalentes.
La Citrulina puede proveerse de múltiples fuentes:
De la arginine vía óxido nítrico sintetasa (NOS); De la ornitina vía catabolismo de la prolina o de la
glutamina/glutamato; De la dimetilarginina asimétrica (ADMA) vía DDAH.
Los caminos de enlaces arginina, glutamina, prolina son bidireccionales. O sea, la utilización neta o producción de esos aminoácidos es altamente dependiente del tipo de célula y del estadio de desarrollo.
Bioquímica 13

AMINOÁCIDOS: VALINA, HISTIDINA Y ARGININA 2010
En el cuerpo, la síntesis de arginina ocurre principalmente vía el eje intestinal–renal, donde los epitelios del intestino delgado, que produce citrulina primariamente desde la glutamina y de glutamato, colabora con las células tubulares proximales del páncreas, que extrae citrulina de la circulación y la convierte en arginina, que es colocado en la circulación. Consecuentemente, anomalías intestinales o de función renal puede reducir la síntesis endógena de arginina, haciendo necesario subir el requerimiento del aminoácido en la dieta.
La síntesis de arginina desde la citrulina ocurre a bajo nivel en muchos otros tejidos, y la capacidad tisular de sintetizar arginina puede incrementarse marcadamente bajo circunstancias que también inducen la sintetasa óxido nítrico (iNOS). Así, la citrulina, un coproducto de la reacción NOS-catalizada, puede reciclarse a arginina en el camino bioquímico citrulina-NO o camino arginina-citrulina.
Bioquímica 14

AMINOÁCIDOS: VALINA, HISTIDINA Y ARGININA 2010
La Valina es uno de los aminoácidos esenciales que nuestro organismo no fabrica por lo que tenemos que obtenerlo a través de una buena alimentación. Este aminoácido es el único usado por los músculos como combustible.
Al igual que otros aminoácidos, la histidina se encuentra en casi todas las células del cuerpo, y está implicado en diversas funciones biológicas. Es clave para la formación de la vaina de mielina, la barrera protectora que rodea las células nerviosas y apoya la transmisión de las señales del cerebro a diferentes partes del cuerpo.
El aminoácido arginina tiene varias funciones en el organismo; por ejemplo, ayuda a la cicatrización de heridas, ayuda a eliminar el exceso de amoníaco del organismo, estimula la función inmunológica, y favorece la secreción de varias hormonas, como el glucagon, la insulina y la hormona de crecimiento.
Bioquímica 15

AMINOÁCIDOS: VALINA, HISTIDINA Y ARGININA 2010
http://www.vitonica.com/musculacion/la-valina-un-aminoacido-
necesario-para-aumentar-el-volumen-muscular
http://es.wikilingue.com/ca/Valina
http://es.wikipedia.org/wiki/Histidina
http://www.puritan.com/vf/healthnotes/hn75_spanish/Es-Supp/
Histidine.htm
http://www.sexovida.com/medicina_natural/larginina.htm
http://www.alfinal.com/Salud/arginina.php
Bioquímica 16