Antibióticos inhibidores de traduccion -...
Transcript of Antibióticos inhibidores de traduccion -...

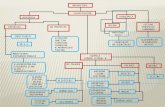
Antibióticos inhibidores de traduccion
Antibiótico/Toxina Organismo Función Tetraciclina Procarionte Sitio A subunidad 30S Cloramfenicol Procarionte Centro PTC subunidad 50S Puromicina Procarionte/Euca-
rionte Centro PTC subunidad 50S
Eritromicina Procarionte Tunel de salida del péptido naciente
Acido fusídico Procarionte EF-G Ricina Procarionte Modifica el RNA en el centro
activador de GTPasa Toxina de difteria Eucarionte Modifica EF-1A Cicloheximida Eucarionte Translocación del ribosoma
durante elongación

Conociendo la estructura del ribosoma se pueden diseñar nuevos antibióticos...

Modificaciones Co- y Post- traduccionales de las proteínas
Eliminación de residuos N-terminales (f-Met en bacteria; Met en eucariontes)
Modificación de aminoácidos • Acetilación (Lys, Arg en histonas; cambia la función) • Fosforilación (Ser, Thr, Tyr; transducción de señales, actividad) • Metilación (Lys, Arg en histonas; cambia función) • Carboxilación (Lys, Pro en colágeno, estabilidad estructural) • Glicosilación (Asn; Thr; receptores de hormonas, anticuerpos) • Nucleotidilación (Tyr; adición de AMP regula actividad) • Lipidación (Gly, Cys; localización en membrana) • Ubiquitinación (Lys; degradación localización, función)
Proteólisis (pro-insulina a insulina; actividad) Adición de grupos prostéticos (grupo hemo, hemoglobina)

De la proteína sintetizada a una proteína funcional

En algunas proteínas los dominios estructurales se forman durante su síntesis

Las chaperonas moleculares son necesarias para el plegado correcto de las proteínas
Las chaperonas asisten el plegamiento de las proteínas, en caso de que un mal plegamiento no se pueda corregir, dirigen a la proteína a degradación.

Existen dos sistemas de chaperonas
Chaperonas individuales
Chaperonas oligoméricas

Mecanismo de las chaperonas moleculares individuales (HSP70)

Mecanismo de la chaperona oligomérica HSP60/HSP10 (GroEL/GroES en bacteria)

Ayuda en la formación de puentes disulfuro correctos
PDI: proteína disulfuro isomerasa

Direccionamiento a la localización celular adecuada
Las proteínas nucleares, mitocondriales, de cloroplasto o peroxisoma (plantas) y las del citosol son sintetizadas por ribosomas libres en el citoplasma y pos-traduccionalmente dirigidas a su destino.

Las proteínas que pertenecen al sistema endomembranoso (retículo endoplásmico, aparato de Golgi, lisosomas o vacuola en plantas), son integrales de membrana plasmática, o tienen un destino extracelular son dirigidas al lúmen del retículo endoplásmico (RE) co-traduccionalmente y los ribosomas que las sintetizan se encuentran anclados a la membrana de RE.

El destino de las proteínas se determina por secuencias señal en la proteína
KDEL
Las secuencias señal son amino-terminales (RE, mitocondria, cloroplasto), internas (núcleo) ó carboxilo-terminales (residentes RE)

Direccionamiento co-traduccional a RE de proteínas del sistema endomembranoso, integrales de membrana o extracelulares
La secuencia señal (amino-terminal) emerge del ribosoma Complejo SRP•GDP reconoce la secuencia señal El complejo se ancla al receptor de SRP en la membrana de RE unión a GTP, hidrólisis y liberación de SRP

Una vez que cumple su función, el péptido señal es cortado

Glicosilación co-traduccional de proteínas destinadas a Retículo Endoplásmico

Glicosilación pos-traduccional de proteínas en Aparato de Golgi y tráfico vesicular
RER
Golgi
cis-Golgi
media-Golgi
trans-Golgi
lisosoma
membrana
vesícula secretora

Biochem. J. (2004) 379 (513–525)
Ubiquitinación de proteínas
Participan tres tipos de enzimas: E1: enzima activadora E2: enzima conjugadora E3: enzima ligadora (ubiquitin ligasa)
La ubiquitina (Ub) es una proteína de 76 aa que contiene varias Lys. Durante la poli-ubiquitinación, cada Ub es enlazada con otra sobre una Lys.

Degradación en el proteosoma
Una vez que el polímero de Ub es reconocido por el proteosoma, entrega a este solo la proteína blanco, mientras que las Ub se reciclan.

Relevancia del sistema Ubiquitina - Proteosoma






![Novel (2-amino-4-arylimidazolyl)propanoic acids and ... · 1032 Novel (2-amino-4-arylimidazolyl)propanoic acids and pyrrolo[1,2-c]imidazoles via the domino reactions of2-amino-4-arylimidazoles](https://static.fdocuments.co/doc/165x107/5f896017e11ee52ec432b706/novel-2-amino-4-arylimidazolylpropanoic-acids-and-1032-novel-2-amino-4-arylimidazolylpropanoic.jpg)