Esquizofrenias en Esquemas 2009
-
Upload
dorismilke -
Category
Documents
-
view
3.788 -
download
5
Transcript of Esquizofrenias en Esquemas 2009

1
Esquizofreniasen esquemas, 2.ª ed
C. ArangoM. T. BascaránM. BousoñoG. FlórezM. P. García-PortillaP. A. SáizJ. Bobes

2
Índice
1. Concepto........................................................................
32. Epidemiología..............................................................
..
103. Factores etiológicos y/o de
riesgo...................................
194. Criterios
diagnósticos.....................................................
615. Formas prodrómicas y de
inicio......................................
716. Manifestaciones
clínicas................................................
1027. Evaluación...................................................................
1168. Estado de salud general en pacientes
esquizofrénicos. Sobremorbilidad y sobremortalidad...............................
2319. Evolución y pronóstico.................................................
34810. Terapéuticas biológicas y
psicológicas...........................
36611. Prevención de recaídas y comportamientos
suicidas......................................................................
51112. Impacto de la enfermedad...........................................
53013. Aspectos médico-
legales..............................................
557

3
1. Concepto
Desarrollo del concepto de esquizofrenia.............. 4-7
Modelos conceptuales de esquizofrenia................... 8
Clasificación de las esquizofrenias según criterios.... 9

4
Desarrollo del concepto de esquizofrenia
Siglo XIX: psicosis única 1852 Morel: démence précoce 1871 Hecker: hebefrenia 1874 Kahlbaum: catatonía 1899 Kraepelin
— Demencia precoz: hebefrenia, catatonía, paranoide
— Paranoia— Psicosis maníaco-depresiva
Continúa

5
Desarrollo del concepto de esquizofrenia (cont.)
1911 E. Bleuler— Esquizofrenias— Síntomas primarios y secundarios— Síntomas fundamentales y accesorios— Esquizofrenia simpleK. Jaspers— Fenomenología. Jerarquía de los
síntomas— Proceso/desarrollo
1937 Langfeldt— Psicosis esquizofreniforme— Esquizofrenia verdadera
Continúa

6
Desarrollo del concepto de esquizofrenia (cont.)
1943 Jung: esquizofrenia como regresión del yo
1950 K. Schneider: síntomas de primer rango
C. Schneider: visión dimensional de la enfermedad
1972 Feighner: criterios diagnósticos 1978 Spitzer y cols.: RDC (criterios
diagnósticos de investigación)
Continúa

7
Desarrollo del concepto de esquizofrenia (cont.)
1980 Crow: esquizofrenias tipos I y IIHuber
— Síntomas básicos— Frankfurt Complaint Questionnaire
1982 Kay y Andreasen: SANS y SAPS

8
Modelos conceptuales de esquizofrenia
Neurodegenerativo o kraepeliniano— J. Lieberman
Neurodesarrollo— D. Weinberger
Cognitivo/social— Tarrier, J. van Os
Integradores— R. Murray— Llopis

9
Clasificación de las esquizofrenias según criterios
Clínicos (Pinel) Evolutivos (Keller) Etiopatogénicos (Kraepelin) Matemáticos (Cluster) Categoriales-dimensionales Organización neurológica (Jackson) Respuesta al tratamiento Criteriológicos (Kay, Andreasen...)

10
2. Epidemiología
Epidemiología de la esquizofrenia ..................... 11-13
Epidemiología comparada.................................... 14
Relación con el abuso de sustancias................. 15-18

11
Epidemiología de la esquizofrenia
Las tasas de incidencia de las esquizofrenias aparecen estables, a lo largo del tiempo, en diferentes culturas y países
La incidencia anual se considera en torno a 1/10.000, con un rango entre el 0,3 y el 3,7%
En mujeres se presenta con un retraso medio de 3-4 años, probablemente a causa del efecto protector de los estrógenos
Häfner y cols., 1997 Continúa

12
Epidemiología de la esquizofrenia (cont.)
Dos terceras partes de las psicosis esquizofrénicas evolucionan hacia la cronicidad
El número total de personas con esquizofrenia aumenta con la edad de las muestras estudiadas
El número de nuevas esquizofrenias varía con la edad de la muestra
Lieberman Continúa

13
Epidemiología de la esquizofrenia (cont.)
Lieberman
0
200
400
600
800
1.000
5 10 15 20 25 30 35 40 45 50 55 60 > 60
Incidencia acumulada de esquizofrenia en una cohorte de 100.000 personas
Edad de la cohorte
N.º
de e
squ
izofr
en
ias

14
Epidemiología comparada
Trastornos mentales y neurológicos
N.º de casos
(millones)
Trastorno depresivo mayor
Problemas de alcohol
Retraso mental
Esquizofrenia
Epilepsia
Demencias
340
288
60
45
40
29
OMS. Abril, 1999

15
Abuso de sustancias y primer episodio de esquizofrenia
De los pacientes con primer episodio de esquizofrenia, aproximadamente el 34,7% han tenido una historia de abuso de sustancias
En pacientes con abuso de sustancias la edad de inicio es menor
Existe diferencia de géneros: 18,10% mujeres y 44,44% hombres
Los pacientes con abuso de sustancias tienden a mostrar «contenido de pensamiento inusual» y «hostilidad», pero menos «humor depresivo»
McMauri y cols., 2006

16Combinación de sustanciasen pacientes con primer episodio
de esquizofrenia
McMauri y cols., 2006
Abuso de sustancias
combinadas%
Cannabis + cocaína 38,24
Cannabis + alcohol 35,29
Alcohol + alucinógenos 11,76
Cannabis + opioides 15,88
Alcohol + opioides 15,88
Cannabis + anfetaminas
12,94

17
Evidencia de asociación entre cannabis y esquizofrenia
El 20-40% de los pacientes psicóticos han utilizado cannabis en su vida (Menezes y cols., 1996; Grech y cols., 1998; Duke y cols., 2001)
Cifras menores en zonas rurales (4-7%) (McCreadie, 2002) Se duplica el riesgo sin considerar el ámbito de estudio
(Regier y cols., 1990; Tien y Anthony, 1990; Robins y Regier, 1991; Hall y Degenhardt, 2000; van Os y cols., 2002; Grech y cols., 1998; McCreadie, 2002)
Retrospectivo de 232 esquizofrenias (Hambrecht y Hafner, 1996) — 1/3 consumo de drogas al menos 1 año antes del inicio— 1/3 dentro del año posterior al consumo— 1/3 consumo de cannabis tras el inicio de los síntomas
El 37% refiere uso de sustancias/alcohol previo al primer episodio psicótico (Cantwell, 1999)

18Prevalencia del abuso de sustancias por diagnóstico,
género y sustancia
Rabinowitz, 1998
Trastorno bipolar EsquizofreniaOtras psicosis
no orgánicas
Hombres
N = 76 (%)
MujeresN = 77
(%)
HombresN = 146
(%)
MujeresN = 78
(%)
Hombres
N = 29 (%)
MujeresN = 36
(%)
Alcohol 66,7 30,7 47,1 18,9 37,0 14,7
Cannabis 48,7 21,6 37,5 15,8 25,9 18,8
Estimulantes y cocaína
28,9 16,9 13,7 17,7 24,1 11,1
Alucinógenos 17,6 12,6 19,9 12,6 10,7 10
Sedativos 13,9 16,7 13,5 12,6 10,3 12,9
Opiáceos 15,3 11,3 12,8 13,9 13,4 12,9
Otra y polisustancias
15,4 15,2 10,7 12,6 17,2 12,9
Abuso de cualquier sustancia
72,4 37,7 54,8 29,5 44,8 22,2

19
3. Factores etiológicos y/o de riesgo
Etiopatogenia: neurodesarrollo frente a neurodegeneración ...................................... 20-23
Factores de riesgo neurobiológicos y genéticos. 24-59

20
Neurodesarrollo
El cerebro sufre una alteración en su desarrollo normal, principalmente en el segundo trimestre intraútero, que da lugar a síntomas que se manifiestan sólo cuando tienen que utilizarse las áreas disfuncionantes (adolescencia) (Weinberger, 1987; Murray, 1997)
Continúa

21
Neurodesarrollo (cont.)
Indicios a favor de la hipótesis del neurodesarrollo:— Falta de gliosis (señal de procesos atróficos
en el cerebro)— Falta de migración neuronal normal
intraútero en pacientes con esquizofrenia— Cambios dermatoglíficos y anomalías
físicas que suceden intraútero en personas que desarrollan esquizofrenia
— Presencia de alteraciones cognitivas y signos neurológicos menores en niños y adolescentes prepsicóticos
Continúa

22
Neurodesarrollo (cont.)
Indicios a favor de la hipótesis del neurodesarrollo:— Estudios de neuroimagen en los que las
alteraciones cerebrales están presentes en el primer episodio y son estáticas
— Lesiones cerebrales en el segundo trimestre del embarazo (hambrunas, infecciones víricas, estrés emocional grave) aumentan el riesgo de presentar esquizofrenia en el futuro

23
Neurodegeneración
Trabajos longitudinales recientes muestran que al menos un subgrupo de pacientes presenta una disminución del volumen cerebral mayor de lo esperado en los primeros años de enfermedad (Gur y cols., 1998; Lieberman y cols., 2001; Mathalon y cols., 2001; Thompson y cols., 2001)
Factores indirectos como el cortisol secundario al estrés pueden producir muerte neuronal o disminución de la neurogénesis en áreas cerebrales como el hipocampo (Arango y cols., 2001)

24
Factores de riesgo para el desarrollo de esquizofrenia
Murray, 2002
Genéticos Sociales Tóxicos Lesionales ¿Infecciosos
? Otros
0 10 20 30 40 50
Familiar esquizofrénico
Migración
Estrés social
Ciudad
Drogas
Obstétricos
Fecha de nacimiento

25
Factores genéticos
Tasas de concordancia
Cardno y cols., Arch Gen Psychiatry 1999; 56: 162-168
Múltiples genesde pequeño efecto, interactuando entre ellos y el ambiente
Incrementanla vulnerabilidad
05
1015202530354045
Monocigóticos Dicigóticos
Continúa

26
Factores genéticos (cont.)
Embarazo Parto Nutrición Virus Alteraciones
cognitivas Ansiedad
social Aislamiento Ideas
abstractas Estrés Drogas Otros
Gen 1
Gen 2
Gen 3
Gen 4
Gen 5
Gen 6
GenotipoB
GenotipoC
GenotipoD
Genotipo
AEsquizofrenia
Trastornobipolar
Psicosiscicloide
Esquizoafectivos

27
Volumen ventricular
Esquizofrenia
Esquizofrenia
Posible portador
Esquizofrenia
Posibleportador
Controles Portadores

28
Complicaciones obstétricas
Con complicaciones
Controles
Todos los familiares
Esquizofrenia familiar
Volumen del hipocampo izquierdo
Sin complicaciones
Cannon, 2002
La sensibilidad a la hipoxia se transmite familiarmente y se correlaciona con la esquizofrenia

29
Volumen del hipocampo izquierdo
El volumen del hipocampo izquierdo se correlaciona con la memoria verbal
La memoria verbal es el déficit cognitivo más importante en la esquizofrenia
El déficit en el volumen del hipocampo se correlaciona con la aparición de esquizofrenia
Esquizofrénicos
ControlesFamiliares

30
Riesgo de desarrollo de psicosis
Mortenson, 1999
0 1 2 3 4 5
Rural
Pequeña ciudad
Gran ciudad
Suburbio
Copenague
Riesgo relativo
Copenhague
El riesgo de psicosis es mayor en función del hábitat

31
Factores de protección
Antecedentes familiares de psicosis afectivas (Fowler, 1972)
Ausencia de complicaciones obstétricas (Verdoux, 1997; Jones, 1999)
Buen apoyo social (Done, 1994; Jones, 1994; van Os, 1997)
Buen nivel de inteligencia (coeficiente intelectual) (Goldman, 1993)
Buena memoria verbal y vigilancia (Green, 1996)

32
Factores de riesgo
Sexo masculino (Castle, 1993) Comienzo precoz (Andreasen, 1990; Yang,
1995; Hoff, 1996) Mal ajuste premórbido (Bromet, 1974; Ciompi
1980) Abuso de drogas (Turner, 1990) Nivel socioeconómico bajo (Cooper, 1961;
Myers 1968; Eaton, 1975; Gift, 1985)

33
Factores de riesgo y mal pronóstico
Riesgo Mal pronóstico
Ajuste premórbido deficiente
Disfunción cognitiva
Sexo masculino
Complicaciones obstétricas
Comienzo precoz
Tamaño ventricular aumentado
Nivel socioeconómico bajo
Consumo de drogas
Larga duración del período previo al tratamiento

34
¿Es la esquizofrenia una enfermedad genética?
Epidemiología genética— Estudios familiares— Estudios de gemelos— Estudios de adopción
Genética molecular— Estudios de ligamiento— Estudios de asociación

35
Estudios familiares
Frecuencia de distintos trastornos en familiares de individuos afectados— Establecer si existen factores hereditarios
en la etiología— Grado de solapamiento entre distintos
síndromes clínicos o aspectos biopsicosociales asociados
— Estudiar la interacción de factores familiares y factores sociales y ambientales

36
Estudios familiares y gemelares en esquizofrenia
0 10 20 30 40 50 60
Población general
Primos
Tíos
Sobrinos
Nietos
Hermanastros
Padres
Hermanos
Hijos
Gemelos dicigóticos
Gemelos monocigóticos
Riesgo de desarrollar esquizofrenia
Pare
nte
sco c
on e
l paci
ente
esq
uiz
ofr
énic
o
Genes compartidos:
0% población general
12,5% familiar de tercer grado
25% familiar de segundo grado
50% familiar de primer grado
100% gemelo monocigótico
Gottesman, 1991

37
Estudios en gemelos
Comparar la incidencia de un trastorno en gemelos idénticos respecto a la incidencia en gemelos no idénticos— Hermanos criados juntos desde el
nacimiento— Monocigóticos criados aparte— Hijos de monocigóticos discordantes

38
Estudios en gemelos
0
10
20
30
40
50
60
70
80
Japón Dinamarca Finlandia Alemania Gran Bretaña
Dicigóticos Monocigóticos
Tasa de concordancia

39
Estudios de adopción
Distinguir entre factores etiológicos genéticos y no genéticos— Comparar el riesgo de padecer enfermedad
en familiares biológicos y adoptivos

40
Estudios de adopción y esquizofrenia
Porcentaje de hijos con esquizofrenia
0
5
10
15
20
25
30
35
Heston Rosenthal Kety Tienari
Padres + Controles
%

41
Heredabilidad de distintos trastornos mentales
TrastornoHeredabilidad
(%)
Trastorno de ansiedad generalizada
Depresión mayor
Fobias
Trastorno de angustia
Suicidio
Alcoholismo
Esquizofrenia
Trastorno bipolar
30
30-35
30
40
45
60
60
70

42
Enfermedades genéticamente complejas
Claro componente genético No presentan un patrón de herencia que se
ajuste al modelo mendeliano
Genes de susceptibilidad
Factores ambientales
+ Enfermedad
Continúa

43
Enfermedades genéticamente complejas (cont.)
No existe correspondencia genotipo-fenotipo— Mismo genotipo: distintos fenotipos— Diferentes genotipos: mismo fenotipo
Edad de inicio variable Posibilidad de cambio diagnóstico Validez de categorías diagnósticas

44
Modelos de umbral de susceptibilidad
Modelo poligénico multifactorial
Umbral de susceptibilidad
Riesgo en población general
Umbral de susceptibilidad
Riesgo en familiares

45
Estudios de ligamiento: regiones cromosómicas implicadas en la esquizofrenia
Bray y Owen, 2001

46Genes de vulnerabilidad de esquizofrenia: candidatos
actuales
Modificado de Weinberger y cols., 2004
Vínculos genómicos1q, 2p, 5q, 6p, 6q, 8p, 10p, 11q, 13q, 15q, 22q
Mapa ajustado
Asociación SNPDisbindina (6p) (7)*
Neurorregulina (8p) (6)*G72 (13q) (3)*
MRDS1 (6p) (4)*
Candidatos funcionalesCOMT (22q) (8)*GRM3 (7q) (4)*GAD 1 (2q) (4)*
CNRNA7 (15q) (2)* PPP3CC (8p) (2)*
Akt1 (2)FOXP2 (7q) (1)*
Traslocación cromosómicaDISC1 (1q) (3)*
PRODH (22q) (2)
Perfil de expresiónRGS4 (1q) (four)*
*N.o de muestras positivas mundiales.

47Coagregación familiarentre trastornos psicóticos
y trastornos afectivos
Osby y cols., 2001
Probandos
Ratios de incidencia estandarizados
Hermanos Hermanastros
EsquizofreniaTrastorno
bipolar EsquizofreniaTrastorno
bipolar
Esquizofrenia (13.870)
7,4 13,6 4,4 2,8
Trastorno bipolar (5.400)
4,4 12,8 2,2 8,1

48Coagregación familiarentre trastornos psicóticos
y trastornos afectivos (cont.)
Bramon y Sham, 2004 Continúa
Probandos
77 cogemelos monocigóticos 89 cogemelos dicigóticos
Esquizofrenia
Trastorno esquizo-afectivo Manía Esquizofrenia
Trastorno esquizo-afectivo Manía
Esquizofrenia 40,8 18,2 18,2 5,3 5,3 0
Trastorno esquizoafectivo
26,1 39,1 26,1 4,5 4,5 0
Manía 13,6 31,8 36,4 3,7 3,7 7,4
Ac Ec
Esquizofrenia
As1 Es1 Es2 As3
0,7 0,2440,825 0,293
0,923
0,574 0,306 0,386 0,441 0,258
Ac/Ec, influencias genéticas/ambientales comunes a los tres diagnósticos; As/Es, efectos genéticos/ambientales específicos para cada diagnóstico
Trastorno esquizoafectivo Manía
Es3

49Coagregación familiarentre trastornos psicóticos
y trastornos afectivos (cont.)
Bramon y Sham, 2004
Metaanálisis Esquizofrenia Trastorno bipolar Conclusiones
Badner y Gershon, 2002
8p (MM 50)13q (MM 85)22q (MM 32)
13p (MM 79)22q (MM 32)
13q (MM 85) y 22q (MM 36)
regiones comunes
Lewis y cols., 2003 2p12-q22.19p22.3-22.1
10q11.21-22.114q24.1-32.12
No regiones comunes
Segurado y cols., 2003
5q, 3p, 11q, 6p, 1q,22q, 8p, 20q, 14p,
16q, 18q, 10p, 15q,6q, 17q
9p, 18p-q, 14q,8q
8p ligamiento con la esquizofrenia en dos
metaanálisis

50
Genes de susceptibilidad para trastornos psicóticos y del humor
Kennedy, 2003
Esquizofrenia
Neurorregulina
Disbindina
COMT
PRODH
RGS4
CHRNA7
Trastorno bipolar
G72
G30
DAAO
Trastorno esquizoafectivo
Depresión mayor
BDNF

51Polimorfismos de riesgo en estudios de amplio genoma (WGS)
en psicosis: genes candidatos
PALB2, implicado en la estabilidad de estructuras nucleares
DCTN5/dynactin 5, implicado en el transporte intracelular
NDUFAB1, implicado en la cadena respiratoria mitocondrial
PLXNA2, implicado en la plasticidad y regeneración neuronal
MYO5B, miosina 5b DGKH, diacilglicerol cinasa TSPAN8, tetraspanina 8

52
Uso de endofenotipos en investigación
La identificación de subtipos biológicos permite estudios genéticos concluyentes en la insuficiencia coronaria (Lander, Nature 1988)
El estudio de familias con las cifras más altas de glucosa permite descubrir la deficiencia genética responsable de la diabetes tipo II (Mathani y cols., Nature Gen 1996)
El empleo de endofenotipos permite identificar múltiples genes implicados en el síndrome de prolongación del QTc (Keating y cols., Cell 2001)

53
Endofenotipos
Los endofenotipos biológicos aumentan el poder estadístico. Si se considera la esquizofrenia como un fenotipo, al no saber si los padres o hermanos están afectados y no la expresan se pierde poder estadístico en los estudios genéticos. Se necesitarían, en este caso, cientos de familias para estudios de ligamiento (NIMH Genetic Workshop, 1997). Sin embargo, si se considera un endofenotipo como A se podría detectar una transmisión autosómica dominante con un lod score de 3,0 más del 90% de las veces con 20 familias
A N
A AN A

54
Endofenotipos en esquizofrenia
Inhibición prepulso (Braff y cols., AGP 1992) Movimiento fino ocular de los ojos (Holzman y
cols., AGP 1998) Déficit de atención (Cornblatt, Am J Med Gen
2001) Memoria de trabajo (COMT) (Egan y cols., PNAS
2001) Potencial evocado P50 (Freedman y cols., PNAS
1997) Signos neurológicos menores (Bombín y cols.,
Schiz Bull 2006)

55
Endofenotipos: onda P50
Genes candidatos: ligamiento positivo con el gen que codifica el receptor colinérgico 7 nicotínico. Locus 15q14 (Freedman y cols., PNAS 1997)
Mejoría de P50 con nicotina en pacientes y familiares no afectos (Potter y cols., Schiz Bull 2006)
Mejoría de P50 con agonista 7 nicotínico en la esquizofrenia (Olincy y cols., AGP 2006)

56Afectación morfométrica
en el primer episodio: esquizofrenia frente a
psicosis afectivas Lóbulo temporal
— Similitud1:• Pérdida de asimetría en
ambos grupos de pacientes en el lóbulo temporal
• Reducción del volumen de sustancia gris en el polo temporal
— Especificidad en la esquizofrenia2:• Reducción de la
sustancia gris de la circunvolución temporal superior posterior izquierda
1Kasai y cols., Arch Gen Psychiatry 2003; 60: 1069-10772Hirayasu y cols., Am J Psychiatry 1998; 115: 1384-1391 Continúa

57Afectación morfométricaen el primer episodio: esquizofreniafrente a psicosis afectivas (cont.)
Complejo amígdala-hipocampo— Similitud1: pérdida de
asimetría en ambos grupos de pacientes en el complejo amígdala-hipocampo1
— Especificidad2:• Esquizofrenia: reducción
del volumen del hipocampo
• Psicosis afectivas: incremento del volumen de la amígdala
1Hirayasu y cols., Am J Psychiatry 1998; 155: 1384-13912Velakoulis y cols., Arch Gen Psychiatry 2006; 63: 139-149 Continúa

58Otras alteraciones morfométricas específicas de
la esquizofrenia
Reducción del volumen de la sustancia gris prefrontal1
Reducción del volumen de la sustancia gris en la ínsula2
1Hirayasu y cols., Cereb Cortex 2001; 11: 374-3812Kasai y cols., Arch Gen Psychiatry 2003; 60: 1069-1077

59Volumen ventricular lateral comoposible marcador endofenotípico
de esquizofrenia
El grupo de pacientes con esquizofrenia presentó también un incremento significativo del volumen del tercer ventrículo frente a los pacientes bipolares (p<0,05)
a Diferencias significativas con grupo controles sanos (B=0,37, p=0,002)b Diferencias significativas con grupo controles sanos (B=0,23, p<0,04)
McDonald y cols., Am J Psychiatry 2006; 163: 478-487
Pacientes con esquizofrenia
(N=42)a
Log
tota
l d
el volu
men
ven
tric
ula
r la
tera
l (m
l)
Pacientes con trastorno bipolar familiar (N=38)
4,5
4,0
3,5
3,0
2,5
2,0
1,5
Parientes de pacientes con esquizofrenia
(N=32)b
Parientes de pacientes con
esquizofrenia no familiar (N=25)
Sujetos comparados (N=54)
Parientes de pacientes con
trastorno bipolar familiar
(N=52)

60
Volumen del hipocampo en pacientes con esquizofrenia
a Diferencias significativas con el grupo de controles sanos (B=–0,28, p<0,02). En este caso, a diferencia del volumen de los ventrículos, no aparecen diferencias entre los familiares y los controles sanos, lo que aboga por la menor importancia de este volumen como marcador endofenotípico frente a los volúmenes cerebrales
McDonald y cols., Am J Psychiatry 2006; 163: 478-487
Pacientes con esquizofrenia
(N=42)a
Volu
men
tota
l d
el h
ipoca
mp
o (
ml)
Pacientes con trastorno bipolar familiar (N=38)
7,0
6,5
6,0
5,0
4,5
4,0
3,5
Parientes de pacientes con esquizofrenia
(N=32)
Parientes de pacientes con
esquizofrenia no familiar
(N=25)
Sujetos comparados (N=54)
Parientes de pacientes con
trastorno bipolar familiar (N=52)
5,5

61
4. Criterios diagnósticos
CIE-10........................................................... 62-64
DSM-IV.......................................................... 65-70

62
Esquizofrenia en la CIE-10:criterios básicos
Síntomas característicos durante un mes Si está presente un trastorno afectivo, debe ir
precedido de síntomas característicos durante un mes
No atribuible a enfermedad orgánica cerebral ni abuso de sustancias
OMS

63
Esquizofrenia en la CIE-10: síntomas característicos
Al menos uno de los siguientes:— Eco, bloqueo o difusión del pensamiento— Delirios de control, influencia o pasividad;
percepción delirante— Voces comentando o discutiendo, voces
que proceden de algún lugar del cuerpo— Delirios persistentes que sean
culturalmente inapropiados y completamente imposibles, como los de identidad religiosa o política, o los poderes sobrenaturales
OMS Continúa

64
Esquizofrenia en la CIE-10: síntomas característicos (cont.)
O, al menos, dos de los siguientes:— Alucinaciones persistentes de cualquier
modalidad cuando se acompañan de delirios
— Neologismos, bloqueos o interrupciones del desarrollo del pensamiento, que dan lugar a incoherencia o a lenguaje divagatorio
— Conducta catatónica— Síntomas «negativos», como apatía
importante, empobrecimiento del lenguaje y aplanamiento o incongruencia de las respuestas emocionales
OMS

65
Esquizofrenia en el DSM-IV:criterios básicos
Síntomas característicos durante un mes Disfunción social u ocupacional Duración total superior a 6 meses No atribuible a trastornos del humor No atribuible a uso de sustancias o enfermedad
médica general
APA

66
Criterio A: síntomas característicos
Al menos dos de los siguientes, presente cada uno de ellos durante un intervalo de tiempo significativo en un período de un mes (o menos si se trató con éxito)1. Ideas delirantes2. Alucinaciones3. Lenguaje desorganizado (descarrilamiento
frecuente o incoherencia)4. Conducta catatónica o desorganizada5. Síntomas negativos (aplanamiento
afectivo, alogia o abulia)
APA

67
Criterio B: disfunción social u ocupacional
Una o más áreas de funcionamiento notablemente por debajo del nivel previo — Trabajo— Relaciones interpersonales— Cuidado personal
Comienzo en la infancia o adolescencia: si no se alcanza el nivel de desarrollo que cabría esperar— Interpersonal— Académico— Ocupacional
APA

68
Criterio C: duración global
Signos continuos del trastorno al menos durante 6 meses
Este período de 6 meses debe incluir al menos un mes con síntomas que cumplan criterios A (síntomas de fase activa) y puede incluir períodos de síntomas prodrómicos o residuales
Durante estos períodos prodrómicos o residuales, los signos del trastorno pueden manifestarse como síntomas negativos sólo, o dos o más síntomas de los enumerados en el criterio A si se presentan de forma atenuada (creencias extrañas o experiencias perceptivas insólitas)
APA

69
Criterio D: exclusión de trastornos afectivos o esquizoafectivos
Se descartan los trastornos esquizoafectivos y los afectivos con rasgos psicóticos porque:1. No ha habido episodios depresivos
mayores o maníacos simultáneamente a los síntomas de fase activa, o
2. Si los episodios afectivos han ocurrido durante los síntomas de fase activa, su duración total ha sido breve en relación con la duración de los períodos activo y residual
APA

70Criterio E: exclusión de consumo de sustancias y enfermedad
médica
El trastorno no se debe a los efectos directos de:— Una sustancia (drogas de abuso,
medicación) o— Una enfermedad médica
APA

71
5. Formas prodrómicas y de inicio
Formas prodrómicas….....................................72-81
El paso a la psicosis........................................82-89
Formas de inicio........................................... 90-101

72
Formas prodrómicas: concepto
Pródromo es un término que se emplea para describir los síntomas y signos tempranos de una enfermedad que preceden a las manifestaciones característicasde ésta cuando se ha desarrollado por completo;por tanto, siempre es retrospectivo
En el caso de la esquizofrenia, el pródromo implica todos los cambios que se presentan en el individuo con respecto a su funcionamiento premórbido y que se mantienen de forma constante en el tiempo, aunque con intensidad variable, hasta que surge la clínica francamente psicótica

73
Formas prodrómicas: duración
Basándose en los distintos trabajos publicados hasta el momento, la duración media de los pródromosdel primer episodio psicótico es de unos 2 años,con una mediana de un año (medida más fiable dada la dispersión de los resultados obtenidos en los estudios)
Esta duración es muy superior a la de los pródromos de las recaídas
McGlashan y Johannessen

74
Formas prodrómicas: clínica
Clínica neurótica: ansiedad, irritabilidad, inestabilidad, cólera e inquietud
Clínica afectiva: depresión, anhedonía, sentimientos de culpabilidad, falta de confianza, ideas suicidas y estado de ánimo inestable
Trastornos de la voluntad: apatía, aburrimiento, pérdida de intereses, fatiga y pérdida de energía
Alteraciones cognitivas: trastornos de la atención y de la concentración, pérdida de capacidad de abstracción, bloqueo del pensamiento, excesivas preocupaciones y conductas de ensimismamiento
Yung y Jackson Continúa

75
Formas prodrómicas: clínica (cont.)
Síntomas físicos: pérdida de peso, pérdida de apetito, trastornos del sueño y quejas somáticas
Trastornos del comportamiento: deterioro laboral, aislamiento social, impulsividad, comportamientos extravagantes o agresivos
Otros síntomas: fenómenos obsesivo-compulsivos, fenómenos disociativos, aumento de la sensibilidad interpersonal, alteraciones de la motricidad, alteraciones del lenguaje, alteraciones perceptivas, suspicacia, cambios en el afecto y cambio en los sentimientos con respecto a uno mismo, a los otros y al mundo
(En negrita, los más frecuentes)Yung y Jackson Continúa

76
Formas prodrómicas: clínica (cont.)
McGorry demostró en población juvenil la elevada inespecificidad de la sintomatología prodrómica— 51% fenómenos de ideación mágica— 45,6% percepciones inusuales— 41,1% alteraciones intensas del funcionamiento social— 39,7% anergia— 25,2% comportamientos inadecuados— 21,7% afecto inapropiado y alteraciones del pensamiento— 18,4% aislamiento social— 8,1% deterioro importante de la higiene personal
Lo fundamental es, por tanto, la constelación de síntomas que presenta cada paciente y su evolución
McGorry y cols.

77Formas prodrómicas: secuencias de evolución de
síntomas
Yung y McGorry
Síntomas psicóticos atenuados
Cambios en el comportamiento
Síntomas inespecífico
s
Síntomas psicóticos
Secuencia uno
Continúa

78
Formas prodrómicas: secuencias de evolución de síntomas (cont.)
Yung y McGorry
Trastornos del comportamiento
Síntomasreactivos
Síntomaspsicóticos
Síntomas específicos
Trastornosde la atención
Cambios perceptivos
Trastornos del lenguaje, bloqueos
Trastornos del movimiento
Continúa
Secuencia dos

79
Formas prodrómicas: secuencias de evolución de síntomas (cont.)
Yung y McGorry
Outpost* Pródromo Psicosis
*Síntomas de tipo prodrómico, de duración breve y resolución espontánea
Continúa
Secuencia tres

80Formas prodrómicas: secuencias de evolución de síntomas
(cont.)
Yung y McGorry
Asintomático
Síntomas inespecífico
s
Síntomas psicóticos
Síntomas psicóticos atenuados
Trastornos del comportamiento
Secuencia cuatro: modelo interactivo

81
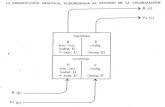
Esquizofrenia: interacción de factores
Deficit de sustancias y otras alteraciones biológicas a nivel límbico-paralímbico
Alteracionesen la atención yen el procesamiento de la información medibles de forma experimental
Susceptibilidada experimentar alteraciones cognitivo-afectivas(síntomas básicos)
Interacción
Factores de vulnerabilidad
Ruptura del procesamiento normal de la información
Alteraciones funcionales, electrofisiológicas y neurobioquímicas, y otras correlaciones a nivel cerebral
Fases intermedias
Pródromos(síntomas básicos)
Clínicapsicóticaesquizofrénica
Resultado
Red sociofamiliar crítica o sobreimplicada
Habilidades de afrontamiento, personalidad premórbida, ambiente social
Estresores diarios, sucesos vitales críticos
Factores psicosociales

82
El paso a la psicosis
En algún punto de la trayectoria vital del individuo surgen los síntomas psicóticos. Estos síntomas se van acumulando de forma más o menos rápida hasta que adquieren suficiente envergadura para ser definidos como un episodio psicótico esquizofrénico que cumple criterios diagnósticos DSM o CIE. Es difícil determinar con exactitud en qué momento se produce este cambio, ya que se trata de un proceso dinámico, flexible, cuantitativo y cualitativo.
Continúa

83
El paso a la psicosis (cont.)
Grivois establece que las relaciones diarias entre los individuos son espontáneas, recíprocas y elementales, y se rigen por mecanismos sensoriales y motores inconscientes.
En la fase prodrómica, estos mecanismos elementales se alteran y provocan cambios en las competencias sociales, los comportamientos y las vivencias subjetivas. Surgen sentimientos de extrañeza o familiaridad que pueden alternarse, produciendo una gran inestabilidad. En estos momentos, el individuo experimenta el concernimiento, una percepción que implica una diferenciación del sujeto frente al resto del grupo social y que trae consigo incertidumbre, perplejidad, preocupación y desconfianza. Ante esta experiencia, el individuo está perplejo, inquieto y puede aislarse o sentir un júbilo increíble.
Grivois y Grosso Continúa

84
El paso a la psicosis (cont.)
Esta sensación avanza de forma fluctuante hasta abarcar a toda la sociedad; en ese momento, entra en la psicosis a través de la centralidad —sentimiento de estar en el centro de la humanidad y de toda realidad—; junto a ella, y de forma fluctuante, surgen comportamientos imprevisibles, sensaciones de fuerza y debilidad, sensaciones de adivinación, de interpretación y luego alucinaciones auditivas. De los intentos de explicar esa centralidad surgirán las ideas delirantes.
Grivois y Grosso Continúa

85
El paso a la psicosis (cont.)
Irritación basal: alteraciones cognitivas del manejo de la información provocan alteraciones perceptivas y de la comprensión de los mensajes verbales, y dificultades para establecer distinciones, con las consiguientes dificultades en la vida diaria. Todo esto se acompaña de trastornos afectivos. Trastornos aislados del movimiento y de la acción generan percepciones inquietantes de pérdida de control de las propias acciones y movimientos
Klosterkötter, Hellmich, Steinmeyer y Schultze-Lutter Continúa
Otros autores, como Klosterkötter, explican el paso a la psicosis por fases:

86
El paso a la psicosis (cont.) Fase de externalización: si avanza la inestabilidad
cognitivo-afectiva, surge una atmósfera de cambio en la que el individuo siente que todo lo sucedido y experimentado tiene que ver con él. Las experiencias inquietantes son vividas «como si» no fuesen ejecutadas por el propio individuo, sino por una fuerza externa; más adelante se viven como auténticamente ejecutadas por esa fuerza extraña
Fase de concretización: los cambios percibidos en la externalización son concretados en una estructura delirante. El individuo descubre o explica el porqué de ese intento de controlar sus acciones y movimientos
Klosterkötter, Hellmich, Steinmeyer y Schultze-Lutter Continúa

87
El paso a la psicosis (cont.)
La aparición de la sintomatología psicótica estaría en relación con alteraciones en el sistema dopaminérgico mesolímbico, en concreto con una hiperactividad de este sistema.
El sistema dopaminérgico mesolímbico media la «atribución de preponderancia» (proceso a través del cual los acontecimientos y los pensamientos recaban la atención, impulsan la acción e influyen en el comportamiento centrado en un objetivo dada su relación con una recompensa o un castigo). Cada estímulo produce una liberación determinada de dopamina que media la adquisición y expresión de las oportunas preponderancias motivacionales en respuesta a las experiencias y predisposiciones del individuo.
Kapur Continúa

88
El paso a la psicosis (cont.)
Cuando el sistema dopaminérgico mesolímbico se altera, lo primero que se produce es una asignación aberrante de preponderancia a objetos externos y a representaciones internas, surgiendo las alteraciones propias de la fase prodrómica (el concernimiento de Grivois y la fase de externalización de Klosterkötter).
Si se mantiene ese estado de hiperactividad dopaminérgica, el paciente comenzará a buscar explicaciones a las asignaciones de preponderancia aberrantes que realiza; esto dará lugar a la aparición de ideas delirantes, que estarán en relación con las experiencias previas y con las ideas culturales propias de cada paciente. Estas ideas delirantes crean un esquema cognitivo que tiende a autoconfirmarse y autoperpetuarse con el tiempo.
Kapur Continúa

89
El paso a la psicosis (cont.)
En cuanto a las alucinaciones, su causa sería una preponderancia anómala de la representación interna de percepciones y recuerdos.
Kapur

90
Formas de inicio
Formas de aparición de la enfermedad— Brusca: síndrome delirante-alucinatorio— Insidiosa
• Obsesiva• Depresiva• Evitación social• Disminución de los rendimientos• Alteraciones comportamentales

91
Formas de inicio (cont.)
Formas de toma a cargo asistencial— Expectativa armada— Intervención psicosocial inmediata— Intervención psicofarmacológica inmediata

92Formas de inicio: fase de psicosis sin tratar. Concepto
de DUP
Si la fase prodrómica ya implica una disfunción sociolaboral considerable, la irrupción de la sintomatología psicótica implica una ruptura con la realidad que dificulta en grado sumo las relaciones sociales, familiares y laborales. Dificultades tan intensas deberían hacer que los pacientes fuesen rápidamente identificados como tales y envíados a los servicios de psiquiatría con la máxima celeridad posible. Sin embargo, ya autores como Harry Stack Sullivan se quejaban del gran retraso que se producía entre el inicio de la clínica psicótica y el inicio del tratamiento adecuado. Este período se ha denominado duration of untreated psychosis (DUP) o fase de psicosis sin tratar
Sullivan Continúa

93Formas de inicio: fase de psicosis sin tratar. Concepto de DUP
(cont.)
Inconsistencia en los tipos de síntomas utilizados para definir el inicio de la psicosis
Arbitrariedad a la hora de considerar cuándo un síntoma deja de ser prodrómico y pasa a ser psicótico
La naturaleza tan privada, ya comentada, de los síntomas psicóticos, que hace que pacientes y observadores den fechas diferentes
Norman y Malla Continúa
Estimar la DUP es un proceso complejo, y a la hora de comparar los resultados obtenidos por los distintos trabajos hay que tener en cuenta las siguientes dificultades indicadas por Norman y Malla:

94Formas de inicio: fase de psicosis sin tratar. Concepto de DUP
(cont.)
Las dificultades del análisis retrospectivo: alteraciones cognitivas en los pacientes; capacidad perceptiva, tolerancia a la excentricidad, negación de la enfermedad y presencia o no de comportamientos extraños son factores que influirán en la capacidad del entorno del paciente para detectar la psicosis
La DUP finaliza cuando se administra el tratamiento antipsicótico adecuado. Los criterios utilizados por los distintos estudios para definir «adecuado» son diferentes. En algunos casos, basta con el inicio de la medicación; en otros, la pauta tiene que cumplir unos requisitos: dosis, tiempo de administración, etc.
Norman y Malla Continúa

95Formas de inicio: fase de psicosis sin tratar. Concepto de DUP
(cont.)
Distintos instrumentos usados para medir la DUP: la IRAOS de Häfner, el RPMIP de McGorry, el CASH de Andreasen o la entrevista estructurada de Beiser. No se han realizado estudios comparativos entre estos diferentes instrumentos
Uso de diferentes técnicas estadísticas Uso de diferentes modelos de estudio
Norman y Malla

96
Formas de inicio: fase de psicosis sin tratar. Duración
Desde los inicios de la década de 1990 se han realizado numerosos trabajos para determinar la DUP.
En conjunto, y tal como indica McGlashan, la DUP tiene una duración media de 2 años, con una mediana (medida más fiable debido a la dispersión de los resultados) de un año. Estas cifras sorprenden por su larga duración y se muestran muy estables en diferentes medios y países.
McGlashan

97Formas de inicio: fase de psicosissin tratar. Implicaciones
pronósticas
Continúa
Autor/año nDUI
mediaDUP
media Resultados pronósticos
Loebel, 1992 70 150,8semana
s
51,9 semana
s
La DUP se asocia con la rapidez y el grado de remisión de la clínica psicótica. La DUP es independiente de la edad de inicio, el modo de inicio o la gravedad de la clínica al inicio del estudio
Larsen, 1996 43 — 114,2 semana
s
La DUP es un factor pronóstico independiente con respecto a la edad de inicio y al ajuste premórbido, y se correlaciona con el nivel de síntomas negativos
Haas, 1998 103
— — La DUP es un factor pronóstico independiente con respecto al ajuste premórbido y se correlaciona con clínica negativa más grave al ingreso y al alta, y clínica positiva más grave al ingresoDUI: duration of untreated illness. DUP: duration of untreated psychosis.

98Formas de inicio: fase de psicosis sin tratar. Implicaciones pronósticas
(cont.)
Continúa
Autor/año nDUI
mediaDUP
media Resultados pronósticos
Edwards, 1998
227
— 209,5 semana
s
La DUP es un factor pronóstico independiente del ajuste premórbido y se correlaciona con la respuesta de la clínica positiva al tratamiento
De Haan, 2000
205
— — No se encuentra correlación entre la DUP y la evolución a largo plazo
Hoff, 2000 32 3,4 años
11,4 meses
La DUP no se correlaciona ni con alteraciones volumétricas cerebrales ni con alteraciones cognitivas en el momento de la valoración inicial
Drake, 2000 248
— 38 semana
s
La DUP es el factor pronóstico individual más significativo tras 6-12 meses de evolución
Browne, 2000
46 — 22,7 meses
La DUP es un factor pronóstico independiente a la hora de determinar la calidad de vida

99Formas de inicio: fase de psicosis sin tratar. Implicaciones pronósticas
(cont.)
Continúa
Autor/año nDUI
mediaDUP
media Resultados pronósticos
Barnes, 2000
53 104 semana
s
26 semana
s
No se observa correlación entre la DUP/DUI y la evolución clínica
Ho, 2000 74 130,5 semana
s
60,8 semana
s
No se halló una correlación significativa entre la DUP y la evolución (medida a través de la calidad de vida)
Norman, 2001
113
39,4 meses
14,6 meses
No se halló correlación entre la DUP y el rendimiento de los pacientes en una batería cognitiva
Malla, 2001 41 42,4 meses
17 meses
No se halló una correlación significativa entre la DUP y la evolución (medida a través de la calidad de vida)

100Formas de inicio: fase de psicosis sin tratar. Implicaciones pronósticas
(cont.)
Autor/año nDUI
mediaDUP
media Resultados pronósticos
Amminger, 2002
42 — 246,3 días
Se halló correlación entre la DUP y el rendimiento de los pacientes en una batería cognitiva
Malla, 2002 88 124 semana
s
44,6 semana
s
La DUP es un factor pronóstico independiente del ajuste premórbido y de la DUI en lo referente a la evolución de la clínica positiva
Ho, 2003 156
— 74,3 semana
s
No se halló correlación entre la DUP y el rendimiento de los pacientes en una batería cognitiva y con las medidas volumétricas cerebrales

101
Diagnóstico diferencial ante un primer episodio psicótico
Esquizofrenia Trastorno
esquizofreniforme Trastorno
esquizoafectivo Trastorno bipolar Depresión psicótica Trastorno psicótico
breve Trastorno psicótico
debido a una afección médica
Psicosis tóxica Trastorno delirante Psicosis posparto Cuadros psicóticos
específicos en ciertas culturas
Trastornos psicóticos atípicos

102
6. Manifestaciones clínicas
Introducción ............................................... 103-104
Síntomas positivos............................................. 105
Síntomas negativos ..................................... 106-109
Disfunción cognitiva .................................... 110-112
Síntomas afectivos ..................................... 113-114
Necesidades en la esquizofrenia.......................... 115

103
Manifestaciones clínicasen la esquizofrenia
Sufrimiento del paciente y su familia Pérdida de productividad Menor calidad de vida Trastornos orgánicos y mentales
concomitantes Riesgo de suicidio Riesgo de conductas antisociales-agresividad Coste sanitario elevado
La esquizofrenia es una de las enfermedades que más discapacidad produce durante la adolescencia y la edad adulta, lo que se traduce en:

104
Síntomas centrales de la esquizofrenia
II.Negativos
EmbotamientoApatíaAnhedonía
I.Positivos
Delirios/alucinacionesDesorganizaciónCatatonía
Alteraciones de la conducta
Disfunción sociolaboral,familiar e interpersonalPérdida de autonomía
III.Cognitivos
AtenciónMemoriaFunciones ejecutivas
IV.Afectivos
DisforiaDepresiónAutólisis

105
Síntomas positivos
Delirios, alteraciones sensoperceptivas y desorganización conductual
No son los síntomas nucleares en la esquizofrenia La discapacidad del paciente depende más de otros
tipos de síntomas (negativos, cognitivos, etc.) Son útiles para detectar las fases agudas o brotes Suponen un mal pronóstico sólo cuando persisten a
pesar de los tratamientos Su presencia está ligada a hiperfunción
dopaminérgica en el sistema límbico y el núcleo accumbens

106
Definición de síntomas negativos
Aunque las definiciones son variables, existe un grupo de síntomas negativos aceptados por la mayoría:— Embotamiento afectivo— Retraimiento emocional— Apatía— Alogia— Desmotivación— Anhedonía
Tandon y cols., 1995

107
Esquema de síntomas negativos
Asociados con síntomas
extrapiramidalesAsociados con privación ambiental
Asociados con síntomas afectivos
Asociados con síntomas positivos
Deterioro o defecto
Premórbidos
Secundarios
Déficit o primarios
persistentes

108
Perfiles de síndromes negativos
Año Autor Manifestaciones clínicas
1980 Crow Aplanamiento afectivoPobreza del lenguaje
1988 Carpenter Concepto de síndrome deficitario:— Restricción afectiva— Conducta social deficiente— Estrechamiento del pensamiento— Respuesta emocional deficiente— Pérdida de la finalidad o propósitos
1993 Kibel 18 síntomas en 5 categoríasPérdida de espontaneidad (PANSS): define la esencia

109Discapacidad en el paciente esquizofrénico: variables
influyentes
Síntomas positivos:— Breier, 1991— O’Connor y Herman,
1993— Montero, 1998
Síntomas negativos:— WHO, 1979— Möller, 1982— Kay, 1987— Carpenter,
1988— Goodman, 1989— Breier, 1991— Hwu, 1995— Shankar, 1995— Bailer, 1996

110
Disfunción cognitivaen la esquizofrenia
Kraepelin definió la esquizofrenia como una demencia
Posteriormente, el déficit neurocognitivo se ha considerado un componente central de la enfermedad y afecta sobre todo a:— Lenguaje— Funciones ejecutivas— Memoria de trabajo— Atención
Los cambios inducidos por los fármacos y por la institucionalización sólo pueden explicar una parte del déficit
Continúa

111
Disfunción cognitiva en la esquizofrenia (cont.)
El funcionamiento cognitivo determina la adaptación social independientemente de la gravedad de los síntomas negativos (McGurk, 2000)
La conciencia de enfermedad y de la necesidad de tratamiento se asocia con mejores rendimientos cognitivos (Marks, 2000)
Las experiencias subjetivas de las que a menudo se quejan los esquizofrénicos son verdaderos trastornos cognitivos (Cuesta y Peralta, 1996)
Continúa

112
Disfunción cognitiva en la esquizofrenia (cont.)
La disfunción cognitiva predice el mantenimiento de la situación laboral del esquizofrénico (Meltzer, 1999)
Los antipsicóticos atípicos combinados con las intervenciones psicosociales mejoran la funcionalidad laboral (McGurk, 1999)

113
Síntomas afectivos y esquizofrenia
Prevalencia del 30 al 60% de síntomas depresivos (mediana, 25%)
Asociado a importante sufrimiento de los pacientes y familiares
Predice una evolución desfavorable y la aparición de recaídas
Disminuye la actividad y la calidad de vida Tasa de suicidios del 10%

114
Depresión y calidad de vida del esquizofrénico
La autoestima y el estado de ánimo condicionan la satisfacción general respecto a la vida (Kemmler, 1997)
La depresión disminuye la percepción subjetiva de calidad de vida (Carpiniello, 1997)
La disforia inducida por neurolépticos repercute negativamente en la calidad de vida (Browne, 1998)

115
Necesidades en la esquizofrenia
Hospitalización: tratamiento agudo (15-20% de su vida)
Cuidados ambulatorios: prevención de las recaídas y rehabilitación80-85% del tiempo fuera del hospital
Maurer y Biehl, 1988

116
7. Evaluación
Evaluación psicométrica............................... 117-211
Monitorización somática .............................. 212-213
Evaluación neurofisiológica e iconográfica......214-230

117
Evaluación psicométrica
Psicopatología— Pródromos............................................
118-138— Formas establecidas...............................
139-159 Evaluación neuropsicológica ........................
160-186 Evaluación del tratamiento
— Tolerabilidad.........................................
187-197— Actitud hacia la
medicación............................
198 Evaluación del impacto de la enfermedad
— Nivel de funcionamiento/discapacidad......
199-202— Calidad de vida ..................................... 203-
211

118
Psicopatología: pródromos
SPI-A (Schultze-Lutter y Klosterkötter, 1999)— Instrumento de predicción de la
esquizofrenia SIPS-SOPS (McGlashan, Miller y Woods, 2001)
— Entrevista estructurada para los síndromes prodrómicos (SIPS)
— Escala de síntomas prodrómicos (SOPS)

119
Instrumento de predicción de la esquizofrenia (SPI-A)
Derivada de la Bonn Scale for the Assessment of Basic Symptoms (BSABS)
Generada basándose en el concepto de síntomas básicos (Huber, 1960):— Déficit que los propios pacientes
esquizofrénicos percibían y que comunicaron retrospectivamente
Continúa

120
Instrumento de predicción de la esquizofrenia (SPI-A) (cont.)
Evalúa la presencia de «síntomas básicos»:— Fatiga (7 ítems)— Déficit dinámicos (3 ítems)— Impedimentos cognitivos (4 ítems)— Alteraciones cognitivas (6 ítems)— Alteraciones en la percepción corporal (9
ítems)— Distanciamiento y alteraciones motoras y
de la percepción (12 ítems)— Ítems adicionales (20 ítems)
Continúa

121
Instrumento de predicción de la esquizofrenia (SPI-A) (cont.)
Para cada ítem se tiene en cuenta a la hora de puntuar:— Su frecuencia y número de veces que ocurre— Su gravedad— Ser percibido como algo nuevo o diferente— Cuánto esfuerzo adicional es necesario para
contrarrestarlo— Su efecto en el comportamiento, en el grado de
funcionamiento o en el ambiente, y sobre todo si induce al paciente a buscar ayuda médica
— Las situaciones en las que se presenta— Las áreas de la vida afectadas por él
Escala Likert de 7 grados:— 0 = ausente, 6 = extremo/grave y psicótico
Continúa

122
Instrumento de predicción de la esquizofrenia (SPI-A) (cont.)
Fatiga— Tolerancia disminuida al estrés normal— Aumento de la reactividad emocional ante
interacciones sociales rutinarias que afecten a personas significativas para el paciente o al propio paciente
— Aumento de la indecisión— Aumento de la autorreflexión, disminución
de la espontaneidad
Continúa

123
Instrumento de predicción de la esquizofrenia (SPI-A) (cont.)
Déficit dinámicos— Cambios en el estado de ánimo y la
sensibilidad emocional— Disminución de la sensibilidad emocional
positiva hacia los demás— Dificultades de concentración
Continúa

124
Instrumento de predicción de la esquizofrenia (SPI-A) (cont.)
Impedimentos cognitivos— Dificultades en la memoria inmediata— Dificultades en la memoria a corto plazo— Pensamiento enlentecido— Falta de «energía del pensamiento»
o pensamientos dirigidos hacia un objetivo
Continúa

125
Instrumento de predicción de la esquizofrenia (SPI-A) (cont.)
Alteraciones cognitivas— Incapacidad para dividir la atención— Interferencia del pensamiento— Presión del pensamiento— Alteraciones en la recepción del lenguaje— Alteraciones en la producción del lenguaje— Ideas de referencia inestables
(«centralidad»)
Continúa

126
Instrumento de predicción de la esquizofrenia (SPI-A) (cont.)
Alteraciones en la percepción corporal— Sensaciones inusuales de
rigidez/entumecimiento— Despersonalización corporal somatopsíquica— Sensaciones inusuales de dolor— Sensaciones corporales migratorias— Sensaciones corporales eléctricas— Sensaciones corporales de movimiento— Sensaciones corporales de extensión,
reducción, etc.— Sensaciones vestibulares— Crisis disestésicas
Continúa

127
Instrumento de predicción de la esquizofrenia (SPI-A) (cont.)
Distanciamiento y alteraciones motoras y de la percepción— Disminución de la capacidad para diferenciar
entre distintos tipos de emociones— Perseverancia del pensamiento— Bloqueo del pensamiento— Visión parcial— Hipersensibilidad a la luz o a ciertos
estímulos ópticos— Fotopsia— Macropsia, micropsia— Alteración en la percepción de la cara
Continúa

128
Instrumento de predicción de la esquizofrenia (SPI-A) (cont.)
Ítems adicionales— Disminución de la habilidad para
discriminar entre ideas y percepciones, entre fantasías y recuerdos verdaderos
— Concretismo— Otras alteraciones perceptivas visuales
(metamorfopsias, cambios en la visión del color, etc.)
— Otras alteraciones de la percepción acústica (acoasmas, «ecos acústicos», etc.)
— Otros

129
SIPS-SOPS
Dos entrevistas semiestructuradas complementarias para la evaluación de los pródromos de la esquizofrenia— La SIPS incluye a la SOPS y recoge
información sobre:• Demografía• Riesgo genético (personalidad
esquizotípica y/o familiar de primer grado con trastorno psicótico)
• Nivel de funcionamiento global actual• Psicopatología: SOPS

130
SIPS-SOPS: recomendaciones de uso
Evaluación inicial: orientación sobre el diagnóstico— Utilizar la SIPS
Seguimiento: evolución de la psicopatología— Utilizar la SOPS

131Entrevista estructurada para los síndromes prodrómicos
(SIPS) Objetivo principal: orientación diagnóstica
— Descartar la presencia de psicosis pasada o actual
— Identificar la presencia de uno o más de los 3 síndromes prodrómicos:A. Síndrome psicótico breve intermitente:
presencia clara de síntomas psicóticos breve y recientemente
B. Síndrome con síntomas positivos atenuados: síntomas psicóticos atenuados recientes
C. Síndrome de riesgo genético y disfunción global
— Evaluar la gravedad de los síntomas prodrómicos
Continúa

132Entrevista estructurada para los síndromes prodrómicos (SIPS)
(cont.)
Recoge información sobre:— Demografía— Riesgo genético— Funcionamiento global actual— Psicopatología
• Síntomas positivos• Síntomas negativos• Síntomas de desorganización• Síntomas generales
Continúa
SOPS

133Entrevista estructurada para los síndromes prodrómicos (SIPS)
(cont.)
Riesgo genético— Presencia de trastorno esquizotípico de la
personalidad (DSM-IV), y/o— Tener un pariente de primer grado con un
trastorno psicótico Funcionamiento global
— Actual: evaluación del funcionamiento global (GAF) en el último mes
— Disfunción global: 30% de reducción en la puntuación en la GAF en el último mes respecto de la puntuación de hace un año

134
Escala de síntomas prodrómicos (SOPS)
Objetivos de la entrevista— Evaluar la gravedad y la evolución de los
síntomas y signos prodrómicos de la esquizofrenia• Positivos (5 ítems)• Negativos (6 ítems)• De desorganización (4 ítems)• Generales (4 ítems)
Cada síntoma se puntúa mediante una escala Likert de intensidad de 7 grados— De 0 (ausente) a 6 (extremo/grave y
psicótico) Continúa

135
Escala de síntomas prodrómicos (SOPS) (cont.)
0Ausente
1Presencia dudosa
2Leve
3Moderado
4Moderadamen
tegrave
5Grave perono psicótico
6Grave
y psicótico
Escala de síntomas positivos
Síntomas positivosP1. Contenido del pensamiento inusual/ideas delirantes 0 1 2 3 4 5 6P2. Suspicacia/ideas persecutorias 0 1 2 3 4 5 6P3. Ideas de grandiosidad 0 1 2 3 4 5 6P4. Percepciones anómalas/alucinaciones 0 1 2 3 4 5 6P5. Comunicación desorganizada 0 1 2 3 4 5 6
Continúa

136
Escala de síntomas prodrómicos(SOPS) (cont.)
0Ausente
1Presencia dudosa
2Leve
3Moderado
4Moderadamen
tegrave
5Grave perono psicótico
6Grave
Escala de síntomas negativos
Síntomas negativosN1. Anhedonía social o aislamiento 0 1 2 3 4 5 6N2. Abulia (apatía) 0 1 2 3 4 5 6N3. Expresión emocional disminuida 0 1 2 3 4 5 6N4. Expresión emocional y del yo disminuida 0 1 2 3 4 5 6N5. Pensamiento empobrecido 0 1 2 3 4 5 6N6. Deterioro en el funcionamiento global 0 1 2 3 4 5 6
Continúa

137
Escala de síntomas prodrómicos(SOPS) (cont.)
0Ausente
1Presencia dudosa
2Leve
3Moderado
4Moderadamen
tegrave
5Grave perono psicótico
6Grave
Escala de síntomas de desorganización
Síntomas de desorganizaciónD1. Apariencia o comportamiento raro 0 1 2 3 4 5 6D2. Pensamiento extraño 0 1 2 3 4 5 6D3. Problemas de atención y concentración 0 1 2 3 4 5 6D4. Higiene personal/habilidades sociales 0 1 2 3 4 5 6
Continúa

138
Escala de síntomas prodrómicos(SOPS) (cont.)
0Ausente
1Presencia dudosa
2Leve
3Moderado
4Moderadamen
tegrave
5Grave perono psicótico
6Grave
Escala de síntomas generales
Síntomas generalesG1. Alteraciones del sueño 0 1 2 3 4 5 6G2. Humor disfórico 0 1 2 3 4 5 6G3. Alteraciones motoras 0 1 2 3 4 5 6G4. Tolerancia disminuida al estrés normal 0 1 2 3 4 5 6

139
Psicopatología:formas establecidas
BPRS (Overall y Gorham, 1962). Escala breve de evaluación psiquiátrica
SANS y SAPS (Andreasen, 1983 y 1984). Escalas de valoración de síntomas negativos y positivos
PANSS (Kay, Fiszbein, Opler, 1987). Escala para el síndrome positivo y negativo de la esquizofrenia
SDS (Kirkpatrick, Buchanan, McKenney, Alphs y Carpenter, 1989). Escala para el síndrome deficitario de la esquizofrenia
SUMD (Amador, Strauss, Yale, Flaum, Endicott y Gorman, 1993). Escala de evaluación del insight

140
Escala breve de evaluación psiquiátrica (BPRS)
Escala heteroaplicada para la evaluación de la gravedad de los síntomas y subtipificación —positivo o negativo— del trastorno esquizofrénico— Cluster de síntomas positivos: ítems
4 (desorganización conceptual), 11 (suspicacia), 12 (alucinaciones) y 15 (contenidos inusuales del pensamiento)
— Cluster de síntomas negativos: ítems 3 (retraimiento emocional), 13 (enlentecimiento motor), 16 (aplanamiento afectivo) y 18 (desorientación)
Continúa

141
Escala breve de evaluación psiquiátrica (BPRS) (cont.)
Consta de 18 ítems que se evalúan mediante una escala Likert de intensidad de 5 grados— 0 = ausente, 4 = muy grave
Puntos de corte propuestos:— 0-9: ausencia de trastorno— 10-20: trastorno leve— > 20: trastorno grave
Continúa

142
Escala breve de evaluación psiquiátrica (BPRS) (cont.)
Preocupaciones somáticas
Ansiedad (psíquica) Retraimiento
emocional Desorganización
conceptual Sentimientos de
culpabilidad Ansiedad (somática) Manierismos y
posturas Grandiosidad Humor depresivo
Hostilidad Suspicacia Alucinaciones Enlentecimiento
psicomotor Falta de colaboración Contenidos inusuales
del pensamiento Afectividad embotada
o inapropiada Agitación psicomotora Desorientación

143Escalas de valoración de síntomas positivos y negativos (SANS y
SAPS)
SANS— Pobreza afectiva
(8 ítems)— Alogia (5)— Abulia-apatía (4)— Anhedonía-
insociabilidad (5)— Atención (3)
SAPS— Alucinaciones
(7 ítems)— Ideas delirantes
(13)— Comportamiento
extravagante (5)— Trastornos
formales del pensamiento (9)Puntuación: 0 (síntoma ausente) a 5 (grave)

144Escala para el síndrome positivo y negativo de la esquizofrenia
(PANSS)
Evalúa el síndrome esquizofrénico de forma:— Dimensional: la gravedad del síndrome positivo,
negativo y de la psicopatología general — Categorial: clasifica el trastorno esquizofrénico
en positivo, negativo o mixto Entrevista semiestructurada heteroaplicada, con
criterios operativos para la evaluación y puntuación Consta de 30 ítems agrupados en tres escalas:
— Positiva: ítems 1 a 7— Negativa: ítems 8 a 14— Psicopatología general: ítems 15 a 30
Continúa

145Escala para el síndrome positivo y negativo de la esquizofrenia (PANSS)
(cont.)
Puntuación de los ítems según una escala Likert de intensidad de 7 grados:— 1 = ausente, 7 = gravedad extrema
Proporciona puntuaciones en 4 escalas:— Positiva (de 7 a 49)— Negativa (de 7 a 49)— Psicopatología general (de 15 a 112)— Compuesta: sustraer la puntuación de la
escala negativa a la de la escala positiva (de –42 a +42)

146
PANSS. Subescalas La escala positiva
(PANSS-P) incluye:— P1. Delirios— P2. Desorganización
conceptual— P3. Comportamiento
alucinatorio— P4. Excitación— P5. Grandiosidad— P6.
Suspicacia/perjuicio— P7. Hostilidad
La escala negativa (PANSS-N) incluye:— N1. Embotamiento afectivo— N2. Retraimiento emocional— N3. Contacto pobre— N4. Retraimiento social— N5. Dificultad de
pensamiento abstracto— N6. Ausencia de
espontaneidad y fluidez en la conversación
— N7. Pensamiento estereotipado
Continúa

147
PANSS. Subescalas (cont.)
— G1. Preocupaciones somáticas
— G2. Ansiedad— G3. Sentimientos
de culpa— G4. Tensión motora— G5. Manierismos
y posturas— G6. Depresión— G7. Retardo motor— G8. Falta de colaboración
— G9. Contenidos inusuales del pensamiento
— G10. Desorientación— G11. Atención deficiente— G12. Ausencia de juicio y
conciencia de enfermedad— G13. Trastornos de la
volición— G14. Control deficiente
de los impulsos— G15. Preocupación— G16. Evitación social activa
La escala de psicopatología general (PANSS-PG) incluye:
Continúa

148
PANSS. Subescalas (cont.)
Lindenmayer y cols. (1994) obtuvieron un modelo de 5 factores vigente en la actualidad— Negativo: ítems N2, N4, N6, N3, N1 y G16— Excitación: ítems P4, G14, P7 y G4— Cognitivo: P2, G10, N5, G5 y G11— Positivo: P1, G9, P5 y P6— Depresión/ansiedad: G2, G3, G6, G1 y G15
Lindenmayer y cols. (2004) propusieron una variación de la escala de excitación — Excitación tipo manía: ítems P4, G14, P7 y
G8
Continúa

149
Andreasen y cols., 2005
PANSS. Subescalas (cont.)
Criterio de remisión del episodio psicótico del Grupo de Trabajo sobre Remisión en la Esquizofrenia. Obliga a que simultáneamente se cumplan los 2 criterios siguientes:— Criterio de intensidad de síntomas:
puntuaciones 1, 2 o 3 (síntoma ausente o presente con intensidad mínima o ligera) en los siguientes 8 ítems simultáneamente: P1, P2, P3, N1, N4, N6, G5 y G9
— Criterio temporal: las puntuaciones en los 8 ítems anteriores no deberán exceder de 3 (intensidad ligera) durante al menos 6 meses

150Escala para el síndrome deficitario
de la esquizofrenia (SDS)
Instrumento diseñado para evaluar el criterio 1 (síntomas negativos) del síndrome deficitario de la esquizofrenia de Carpenter y cols.
El clínico ha de puntuar cada uno de los 6 síntomas negativos utilizando una escala Likert que oscila de 0 (síntoma ausente) a 4 (muy grave)— Aplanamiento afectivo— Rango emocional disminuido— Alogia— Pérdida de interés— Falta de objetivos— Pérdida de interés en actividades socialesContinúa

151
Escala para el síndrome deficitario de la esquizofrenia (SDS) (cont.)
Para puntuar, el clínico deberá considerar:— Observación directa durante la entrevista— Información proveniente de fuentes
relevantes— Información longitudinal, no sólo la
valoración de la situación del paciente en el momento de la evaluación
Continúa

152
Escala para el síndrome deficitario de la esquizofrenia (SDS) (cont.)
Interpretación de las puntuaciones:— El criterio 1 del síndrome deficitario de la
esquizofrenia está presente si al menos 2 de los 6 síntomas negativos han recibido una puntuación de 2 (moderado), 3 (grave) o 4 (muy grave)
La misma escala de puntuación (0 = ausente a 4 = muy grave) se utiliza para obtener una puntuación global de la gravedad del síndrome deficitario si está presente

153
Carpenter, Heinrichs y Wagman, 1988
Síndrome deficitario de la esquizofrenia
Descrito por Carpenter y cols. en 1988 Consta de los 4 criterios siguientes:
1. Presencia de al menos 2 de los 6 síntomas negativos siguientes:a. Aplanamiento afectivob. Rango emocional disminuidoc. Alogiad. Pérdida de interesese. Falta de objetivosf. Pérdida de interés en actividades
socialesContinúa

154
Carpenter, Heinrichs y Wagman, 1988
Síndrome deficitario de la esquizofrenia (cont.)
2. Alguna combinación de 2 o más de esos síntomas negativos ha estado presente durante los últimos 12 meses, y ha estado siempre presente durante períodos de estabilidad clínica— Estos síntomas pueden o no ser
detectables durante episodios transitorios de desorganización o descompensación psicótica aguda
Continúa

155
Carpenter, Heinrichs y Wagman, 1988
Síndrome deficitario de la esquizofrenia (cont.)
3. Los síntomas negativos son primarios, es decir, no secundarios a otros factores que no sean los de la enfermedad— Dichos factores incluyen: ansiedad,
efectos de la medicación, desconfianza, trastornos formales del pensamiento, alucinaciones o delirios, retraso mental y depresión
4. El paciente cumple los criterios DSM-III, DSM-III-R o DSM-IV para esquizofrenia

156
Escala de evaluación del insight (SUMD)
Diseñada para evaluar la conciencia de enfermedad de los pacientes psicóticos multidimensionalmente
La versión más utilizada consta de 15 ítems que se agrupan en 2 partes1. Evaluación global de la conciencia de
enfermedad: los 3 primeros ítems, que evalúan la conciencia de:• Padecer una enfermedad mental• Efectos de la medicación• Consecuencias sociales de la
esquizofreniaContinúa

157
Escala de evaluación del insight (SUMD) (cont.)
2. Evaluación de la conciencia de los síntomas: 12 ítems que evalúan para cada uno de estos 6 síntomas la conciencia y la atribución:• Alucinaciones• Delirios• Trastornos del pensamiento• Embotamiento afectivo• Anhedonía• Asociabilidad
Continúa

158
Escala de evaluación del insight (SUMD) (cont.)
Para puntuar el clínico dispone de una escala Likert de 6 grados que oscilan entre 0 (ítem no relevante), 1 (conciencia/atribución) y 5 (no hay conciencia/no hay atribución)— Para puntuar la atribución de un síntoma es
necesario que el paciente tenga conciencia de él
— Por ello la atribución sólo se puntuará cuando la puntuación del síntoma sea <4
Continúa

159
Escala de evaluación del insight (SUMD) (cont.)
Proporciona tres puntuaciones:— Global de conciencia de enfermedad: suma
de las puntuaciones en los 3 primeros ítems— Conciencia de los síntomas: suma de los
ítems 4 a 9 dividido por el número de ítems relevantes (ítems con puntuación >0)
— Atribución de los síntomas: suma de los ítems 4 a 9 dividido por el número de ítems con puntuación entre 1 y 3
En los tres casos, a mayor puntuación mayor gravedad

160
Evaluación neuropsicológica
General ...................................................... 161-172
Atención........................................................... 173
Funciones ejecutivas ................................... 174-182
Fluidez verbal.................................................... 183
Memoria verbal................................................. 184
Memoria de reconstrucción visual........................ 185
Función motriz.................................................. 186

161
Evaluación neuropsicológica general
WAIS-III (Escala de inteligencia para adultos de Wechsler, 3.a ed.)
Miniexamen cognoscitivo (MEC-30 y MEC-35) Programa MATRICS

162
WAIS-III
Escala de Inteligencia para Adultos de Wechsler, 3.a ed.— 13 tests que evalúan las capacidades
intelectuales generales— Proporciona medidas de inteligencia total
(CIT), verbal (CIV) y manipulativa (CIM)— También proporciona índices de:
• Comprensión verbal• Memoria de trabajo• Organización perceptiva• Velocidad de procesamiento
Continúa

163
WAIS-III (cont.)
CI verbal (CIV)— Índice de comprensión verbal (CV)
• Vocabulario (V)• Semejanzas (S)• Información (I)
— Comprensión (C)— Índice de memoria de trabajo (MT)
• Aritmética (A)• Dígitos (D)• Letras y números (L)
Continúa

164
WAIS-III (cont.)
CI manipulativo (CIM)— Índice de organización perceptiva (OP)
• Figuras incompletas (FI)• Cubos (CC)• Matrices (MA)
— Historietas (HI)— Índice de velocidad de procesamiento (VP)
• Clave de números (CN)• Búsqueda de símbolos (BS)
Continúa

165
WAIS-III
Organización jerárquica
CIT
CIV CIM
CV MT OP VP
V S I C A D L FI CN BSHMC

166
MEC
Miniexamen cognoscitivo (MEC-30 y MEC-35)— Evaluación breve del funcionamiento
cognitivo general— 30 o 35 ítems que evalúan las capacidades
de:• Orientación temporoespacial• Concentración y cálculo• Memoria• Lenguaje• Praxias
— Puntuación total de aciertos

167
MATRICS Programa MATRICS: Measurement And Treatment
Research to Impove Cognition in Schizophrenia— Objetivo general: proveer a los clínicos de
herramientas para mejorar la cognición en la esquizofrenia
— Objetivos específicos:• Establecer un consenso sobre cómo debe
medirse la cognición en la esquizofrenia• Determinar las aproximaciones
farmacológicas más prometedoras en este campo
• Desarrollar la infraestructura de investigación necesaria para realizar ensayos clínicos con los fármacos prometedores Continúa

168
MATRICS (cont.) Dado el papel de la psicopatología sobre la
cognición en pacientes con esquizofrenia, se recomiendan las siguientes mejoras metodológicas en los ensayos clínicos sobre la eficacia cognitiva de los antipsicóticos: — Reducción de la gravedad de los síntomas
psicopatológicos previa a la inclusión del paciente en el ensayo clínico
— Permanencia durante un período de tiempo suficiente en la dosis prefijada del antipsicótico de estudio antes de la evaluación inicial
— Exclusión del ensayo de aquellos sujetos con medidas de sintomatología positiva y negativa superior a una gravedad «moderada» Continúa

169
MATRICS (cont.)
Áreas cognitivas de evaluación— Velocidad de procesamiento — Atención/vigilancia— Memoria de trabajo— Aprendizaje verbal— Aprendizaje visual— Razonamiento y solución de problemas— Cognición social
Tiempo estimado de aplicación de la batería cognitiva provisional: 63,5 minutos
Continúa

170
MATRICS (cont.)
Programa MATRICS— Grado de afectación: entre –1,0 y –1,5 DE— Relevancia clínica, pronóstica y funcional— Validez como endofenotipos— Actualmente en fase de estudio de las
propiedades psicométricas de la batería de evaluación cognitiva
— Financiado por el NIMH, División de Trastornos Mentales, Investigación Comportamental y SIDA. Investigador principal: S.R. Marder, UCLA (EE.UU.)
Continúa

171
MATRICS (cont.)
Continúa
Área cognitivaBatería Cognitiva de Consenso Provisional
Instrumentos Tiempo
Velocidad de procesamiento
- Fluencia por categorías- BACS (Evaluación Breve de Cognición en la Esquizofrenia): código de símbolos- Trail Making Test A
2 min3 min
12,1 min
Atención/vigilancia - CPT-IP (Test de Rendimiento Continuo-Pares Idénticos)
13,4 min
Aprendizaje verbal - HVLT (Test de Aprendizaje Verbal de Hopkins revisado)
14,1 min

172
MATRICS (cont.)
Área cognitivaBatería Cognitiva de Consenso Provisional
Instrumentos Tiempo
Memoria de trabajo - Verbal: Dígitos-Letras de la Universidad de Maryland- No verbal: WMS (Escala de Memoria de Wechsler) III Espacial
15,9 min
15,1 min
Aprendizaje visual BVMT (Test de Memoria Visuoespacial Breve revisado)
14,7 min
Razonamiento y solución de problemas
NAB (Batería de Evaluación Neuropsicológica-Laberintos)
11,2 min
Cognición social MSCEIT (Test de Inteligencia Emocional de Mayer-Salovey-Caruso-Manejo de Emociones)
12,0 min

173
Evaluación de la atención
Rastros A y B (Trail Making Test A y B) — Evaluación de la atención, flexibilidad
mental y secuenciación— Trail Making Test A: relacionar en orden
numérico 25 números dispersos en una hoja (1, 2, 3, 4,…)
— Trail Making Test B: relacionar alternativamente en orden numérico y afabético 13 números y 12 letras dispersas en una hoja (1, A, 2, B, 3, C, 4,…)
— Los resultados se expresan en función del tiempo

174
Evaluación de funciones ejecutivas
Prueba de ordenación de tarjetas de Wisconsin Test de colores y palabras de Stroop Laberintos Torre de Londres

175
Wisconsin Card Sorting Test WCST: prueba de ordenación de tarjetas de Wisconsin Desarrollada originalmente por Berg y Grant (1948) para
evaluar el razonamiento abstracto y la capacidad para cambiar estrategias cognitivas en respuesta a los cambios del entorno
Medida de las funciones ejecutivas (LF) (Luria, 1973; Shallice, 1982)— Planificación de estrategias— Búsqueda organizada— Utilización del feedback ambiental para cambiar las
pautas cognitivas— Conducta dirigida a obtener un objetivo— Modulación de las respuestas impulsivas
Continúa

176
Wisconsin Card Sorting Test (cont.) 4 tarjetas con 3 estímulos
— Forma: triángulos, estrellas, cruces y círculos— Color: rojo y verde, amarillo y azul— Número de figuras: 1, 2, 3 y 4
2 juegos de 64 tarjetas de respuesta, también con las formas, colores y números, y numeradas en el reverso
No hay límite de tiempo Finaliza cuando se han completado 6 categorías o
agotado los 2 juegos de tarjetas de respuesta

177
Test de Colores y Palabras de Stroop
Diseñado por Stroop (1935); la versión normalizada corresponde a Golden (1975)
Administración— Preferentemente individual— Población: entre 7 y 80 años
Tiempo de aplicación: 5 minutos Baremos de población general española (TEA,
1994)
Continúa

178
Test de Colores y Palabras de Stroop (cont.)
Los estímulos del test de Stroop afectan a la capacidad del sujeto para clasificar información de su entorno y reaccionar selectivamente a ella
Mide la capacidad del individuo para separar los estímulos de nombrar colores y palabras— Suprimir la respuesta de lectura— Concentrarse en la tarea de nombrar colores
Continúa

179
Test de Colores y Palabras de Stroop (cont.)
3 láminas DIN-A4 Estímulos
— Palabras (nombres de colores)— Colores (rojo, azul y verde)
Cada lámina: 5 columnas de 20 elementos Puntuación: número de elementos realizados
en 45 segundos
Continúa

180
Test de Colores y Palabras de Stroop (cont.)
Lámina 1: lectura de palabras— Palabras «rojo», «verde» y «azul»
ordenadas al azar e impresas en tinta negra Lámina 2: identificación de colores
— «XXXX» impresas en tinta azul, verde o roja Lámina 3: interferencia color-palabra
— Las palabras de la lámina 1 impresas en los colores de la lámina 2, mezclados 1 a 1

181
Laberintos
La capacidad del individuo para planificar es desafiada por la tarea de imaginarse un camino entre la entrada y la salida

182
Torre de Londres
Prueba de planificación que requiere el desarrollo de una estrategia para mover bolas alineadas en palos desde una posición inicial hasta un objetivo final

183
Evaluación de la fluidez verbal
Fluidez verbal fonológica— El individuo debe nombrar tantas palabras
como le sea posible que comiencen por una letra determinada en un tiempo determinado (1 minuto)
Fluidez semántica— El individuo debe nombrar tantas palabras
como le sea posible que pertenezcan a una categoría semántica específica (p. ej., frutas, animales, etc.) en un tiempo determinado (1 minuto)

184
Evaluación de la memoria verbal
Subtest de memoria lógica de la escala clínica de memoria de Wechsler— Evaluación de la memoria inmediata e intermedia— El individuo escucha una historia coherente y debe
recordar tantos detalles como le sea posible Aprendizaje auditivo-verbal de Rey
— Capacidad del individuo para aprender una lista de palabras de memoria
— Evalúa la memoria inmediata e intermedia y establece una curva de aprendizaje
Aprendizaje de asociación por parejas— El individuo debe aprender una lista de palabras
asociadas con un conjunto de palabras clave

185
Evaluación de la memoria de reconstrucción visual
Figura compleja de Rey-Osterreith— Copia de un diseño complejo— Evaluación de niveles elevados de
habilidades espaciales Test de retención visual de Benton
— Reproducción de figuras geométricas— Puntuación: número total de aciertos y de
errores

186
Evaluación de la función motriz
Oscilaciones de los dedos— Mide la velocidad de repiqueteo de los
dedos con las manos derecha e izquierda— Evalúa las asimetrías laterales de la función
motora Test de clavijas y tableros de Purdue
— Tarea de motricidad fina; examina la destreza manual
— Número de clavijas colocadas en 30 segundos
— Medida útil de lateralización

187
Evaluación del tratamiento: tolerabilidad
BARS (Barnes, 1989)— Escala de acatisia de Barnes
SAS (Simpson y Angus, 1970)— Escala de acatisia de Simpson-Angus
AIMS (Guy, 1976)— Escala de movimientos involuntarios
anormales UKU (Lingjaerd y cols., 1987)
— Escala de efectos secundarios

188
Escala de acatisia de Barnes (BARS)
Escala heteroaplicada que evalúa la presencia y gravedad de la acatisia inducida por fármacos
Consta de 4 ítems— 1 ítem objetivo observacional de los
movimientos del paciente— 2 ítems subjetivos
• Conciencia de la inquietud• Malestar relativo a la inquietud
— 1 ítem de valoración clínica global de la acatisia
Continúa

189
Escala de acatisia de Barnes (BARS) (cont.)
Los tres primeros ítems se puntúan con una escala Likert de 4 grados, con claros criterios operativos de puntuación— De 0 (ausencia) a 3 (grave)
El ítem 4, de valoración clínica global, oscila entre 0 = ausente y 5 = acatisia grave— Claros criterios operativos de puntuación
que tienen en cuenta los 3 ítems anteriores

190
Escala de acatisia de Simpson-Angus (SAS)
Escala heteroaplicada para la evaluación de síntomas extrapiramidales
Consta de 10 ítems— Parkinsonismo (9 ítems)
• Deambulación• Rigidez• Reflejo glabelar• Temblor• Salivación
— Acatisia (1 ítem)
Continúa

191
Escala de acatisia de Simpson-Angus (SAS) (cont.)
Existe una versión abreviada de 6 ítems que evalúa:— Parkinsonismo (4 ítems)
• Expresión facial• Rigidez• Temblor• Acinesia
— Acatisia (1 ítem)— Distonía (1 ítem)
Continúa

192Escala de acatisia de Simpson-Angus (SAS)
(cont.)
Criterios operativos de evaluación y de puntuación
Puntuación de los ítems según la escala Likert de intensidad de 5 grados— De 0 = ausente a 4 = grado extremo
Continúa

193
Escala de acatisia de Simpson-Angus (SAS) (cont.)
Ítems— Forma de andar— Caída de brazos— Movimiento de hombros— Rigidez de codos— Rigidez de muñecas— Rotación de la cabeza— Golpeo de la glabela— Temblor— Salivación— Acatisia

194Escala de movimientos involuntarios anormales
(AIMS)
Consta de 12 ítems que evalúan la existencia y gravedad de movimientos anormales— Faciales y orales: músculos de expresión
facial, labios y área perioral, mandíbula, lengua
— De las extremidades superiores e inferiores— Del tronco— Juicio global sobre los movimientos
anormales: gravedad de éstos, incapacidad que producen, conciencia del paciente
— Estado dental
Continúa

195Escala de movimientos involuntarios anormales (AIMS)
(cont.)
Escala de puntuación tipo Likert de intensidad de 5 grados— De 0 = ausente a 4 = grave

196
Escala de efectos secundarios (UKU)
Consta de 54 ítems que evalúan:— Presencia e intensidad de síntomas o
signos (efectos secundarios)— Relación causal con la medicación
4 subescalas— Efectos secundarios psíquicos (9 ítems)— Efectos secundarios neurológicos (8 ítems)— Efectos secundarios autonómicos (11
ítems)— Otros efectos secundarios (25 ítems)
Continúa

197
Escala de efectos secundarios (UKU) (cont.)
2 ítems finales que evalúan:— Interferencia de los efectos secundarios en
el funcionamiento diario— Consecuencias de la interferencia en el
cumplimiento terapéutico Cada ítem se puntúa según una escala Likert
de intensidad de 4 grados— De 0 = no o dudosamente presente a 3 =
grave Existen versiones para el clínico y para el
paciente

198
Evaluación del tratamiento: actitud hacia la medicación
Inventario de actitudes hacia la medicación (DAI) (Hogan, Awad y Eastwood, 1983)— Evalúa la respuesta subjetiva a los
neurolépticos— Existen dos versiones
• Larga (30 ítems)• Breve (10 ítems): efecto percibido de la
medicación Escala autoaplicada Ítems de respuesta dicotómica (sí/no) No existen puntos de corte definidos: a mayor
puntuación, efecto percibido de la medicación más positivo

199Evaluación del impacto
de la enfermedad: nivel de funcionamiento/discapacidad
EEAG (APA, 1994)— Escala de evaluación de la actividad global
WHODAS-II, 36 ítems (OMS, 2001)— Cuestionario de evaluación de
discapacidades

200
Escala de evaluación de la actividad global (EEAG)
Evalúa el funcionamiento general de los pacientes a lo largo de un hipotético continuum de salud-enfermedad
El único ítem, actividad global del paciente, se puntúa mediante una escala que oscila entre:— 100: actividad satisfactoria— 1: expectativa manifiesta de muerte
Crítica: en los criterios operativos de puntuación incorpora síntomas junto con la discapacidad
Marco de referencia temporal: momento actual

201Cuestionario de evaluaciónde discapacidades
(WHODAS-II, 36 ítems)
36 ítems que evalúan el nivel de funcionamiento del paciente en 6 áreas— Comprensión y comunicación— Capacidad para moverse en su
alrededor/entorno— Cuidado personal— Capacidad de relación con otras personas— Actividades de la vida diaria— Participación en la sociedad
Continúa

202Cuestionario de evaluaciónde discapacidades
(WHODAS-II, 36 ítems) (cont.)
Cada ítem se evalúa teniendo en cuenta:— Grado de dificultad— Grado de dependencia del individuo
Puntuación con una escala Likert de 5 grados:— De 1 = ausencia de dificultad a 5 =
dificultad extrema Proporciona:
— Perfil objetivo de funcionamiento en las 6 áreas
— Percepción subjetiva del paciente sobre el impacto que le producen las dificultades en cada área

203
Evaluación del impacto de la enfermedad: calidad de vida
Instrumentos específicos:— Escala de calidad de vida (QLS)
(Heinrichs y cols., 1984)— Entrevista de calidad de vida (QOLI)
(Lehman, 1994)— Cuestionario Sevilla de calidad de vida
(CSCV) (Giner y cols., 1997) Instrumentos genéricos:
— Cuestionario de salud SF-36 (Ware y Sherbourne, 1992)
— WHOQOL-100 (OMS, 1995)

204
Escala de calidad de vida (QLS)
Modelo conceptual: evaluación por parte del clínico del defecto esquizofrénico
Dimensiones:— Funciones intrapsíquicas— Relaciones interpersonales— Rol instrumental— Uso de objetos comunes y actividades
cotidianas Administración: heteroadministrada N.o de ítems: 21

205
Entrevista de calidad de vida (QOLI)
Modelo conceptual: sentimiento de bienestar personal influido por características personales e indicadores objetivos y subjetivos de calidad de vida
Entrevista semiestructurada Dimensiones:
— Satisfacción global— 8 áreas de la vida: lugar de residencia,
actividades cotidianas, relaciones familiares, relaciones sociales, ingresos, trabajo/estudio, situación legal, salud
Continúa

206
Entrevista de calidad de vida (QOLI) (cont.)
— Cada una de las 8 áreas de la vida se evalúan:• Objetivamente: medidas de
funcionamiento y acceso a recursos• Subjetivamente: medidas de satisfacción
(Andrews y Whithey, 1976)
N.º de ítems: core: 78; versión original: 143
1Muy
7Muy
6Bastante
5Algo
4Medio
3Algo
2Bastant
eInsatisfecho Satisfecho(igual satisfacción
que insatisfacción)

207Cuestionario Sevilla de calidad
de vida (CSCV)
Modelo conceptual: valoración subjetiva de la enfermedad, su impacto y el impacto del tratamiento
Dimensiones:— Favorable: satisfacción vital, armonía,
autoestima— Desfavorable: falta de aprehensión cognitiva,
pérdida de energía, falta de control interno, dificultad de expresión emocional y cognitiva, extrañamiento, miedo a la pérdida de control, hostilidad contenida, automatismo
Administración: autoadministrado N.o de ítems: 59

208
Cuestionario de salud SF-36
Modelo conceptual: valoración subjetiva del estado de salud bidimensional (física y mental)
Dimensiones:— Funcionamiento físico, rol físico, dolor, salud
general, vitalidad, funcionamiento social, rol emocional, salud mental
Administración: autoadministrado N.o de ítems: 36 Se ha demostrado su fiabilidad y validez de
aplicación en pacientes con esquizofrenia y con depresión (Pukrop y cols., 2003)
Continúa

209
Cuestionario de salud SF-36 (cont.)
Salud
física
Salud menta
l
Vitalidad
Función social
Rol emocionalSalud mental
Función física
Rol físico
Dolor
Salud general

210
WHOQOL-100
Modelo conceptual: calidad de vida como percepción subjetiva de la discrepancia entre la situación actual y los objetivos y expectativas
Modelo métrico: tres niveles jerárquicos: ítems, facetas (agregación de ítems) y dominios (agregación de facetas)
Se ha demostrado su fiabilidad al ser aplicado a pacientes con esquizofrenia (Orsel y cols., 2004)
Continúa

211
WHOQOL-100 (cont.)
100 ítems
24 facetas
Calidad de vida y salud general global
6 dominios:- Físico- Psicológico- Independencia- Social- Entorno- Espiritual

212
Monitorización somática
Medidas antropométricas— Peso— Talla— Índice de masa corporal (IMC): kg/m2
— Perímetro abdominal Constantes vitales
— Presión arterial• En sedestación
ECG

213
Monitorización somática: análisis
Bioquímica de sangre: en ayunas de al menos 8 h— Glucosa— Ácido úrico— Colesterol— HDL-colesterol— LDL-colesterol— Triglicéridos— Función hepática— Creatinfosfocinasa— Iones
Hematimetría Hormonas
— TSH— Prolactina

214
Evaluación neurofisiológica e iconográfica
Evaluación neurofisiológica .......................... 215-218
Exploraciones iconográficas.......................... 219-230

215
Evaluación neurofisiológica
EEG para diagnóstico diferencial con la epilepsia (principalmente del lóbulo temporal)
Reducción en amplitud, en potencial evocado P300
Dificultad para inhibir estímulos irrelevantes medido con el potencial evocado P50
Utilización del P50 como marcador de rasgo endofenotípico para la esquizofenia

216
Potencial evocado P50
El cociente entre la respuesta al segundo estímulo y el primer estímulo en los primeros 80 milisegundos (mayor capacidad de inhibir la respuesta a estímulos repetidos cuanto menor sea el cociente) está alterado en pacientes con esquizofrenia y familiares no afectados
Se normaliza con nicotina y clozapina, pero no con otros antipsicóticos
Continúa

217
Potencial evocado P50 (cont.)5,74
4,60
3,46
2,32
1,18
0,03
-1,11
-2,25
-3,39
-4,53
-5,67
-83 -50 -17 16 49 82 115 148 181 214 247
mseg
Am
plit
ud d
e o
nda (
µV
)
P50 Click 2
P50 Click 1
ControlesPacientes

218
Potencial evocado P300A
mp
litud
de o
nd
a (
µV
)
Tiempo (mseg)
ControlesPacientes
F7 FPZ F8
FT7
T7
FT7
TP7
P7
FZ
CZ T8
PZ TP8
OZ P8
200 800400 6000 200 800400 6000 200 800400 6000
0µV
±10

219
Exploraciones iconográficas
Permiten el estudio in vivo de:— Aspectos estructurales y funcionales del
sistema nervioso central— Estructuras corticales y subcorticales
Ninguna técnica tiene sensibilidad o especificidad suficiente para ser utilizada de forma sistemática en el diagnóstico de la esquizofrenia
Importancia principal en el diagnóstico diferencial y la investigación
Continúa

220
Exploraciones iconográficas (cont.)
Estudian la estructura:— TC (tomografía computarizada)— RM (resonancia magnética)
Estudian la función:— PET (tomografía por emisión de positrones)— SPECT (tomografía computarizada por
emisión de fotón único)— RMf (resonancia magnética funcional)— RM por espectroscopia (estudio bioquímico)— MEG (magnetoencefalografía)

221
Exploraciones iconográficas: TC
Tratamiento computarizado de rayos X Imágenes de estructuras corticales y
subcorticales Indicada en todos los casos en que se sospecha
organicidad (diagnóstico diferencial) En esquizofrenia
— ventrículos laterales— ventrículo medio— surcos corticales— tamaño del vermis cerebeloso
Mayor frecuencia en sintomatología negativa

222
Exploraciones iconográficas: RM
Cerebro sometido a campo magnético emisión electromagnética imagen
Resolución superior a la TC Permite distinguir la sustancia gris y la
sustancia blanca No irradia al paciente Obtención de todo tipo de planos.
Reconstrucción tridimensional No se producen artefactos óseos
Continúa

223
Exploraciones iconográficas: RM (cont.)
Principales hallazgos en la esquizofrenia:— Aumento del volumen de los ventrículos
laterales y del tercer ventrículo— Aumento del LCR— Menor volumen del hipocampo— Menor volumen de la circunvolución
temporal superior (correlación con síntomas positivos)
— Falta de la lateralidad normal de los hemisferios cerebrales
— Aumento de los caudados con antipsicóticos convencionales (reversible con tratamiento con clozapina)

224
Exploraciones iconográficas: PET
Inyección de una sustancia marcada con una sustancia emisora de positrones
Imagen que informa del consumo de la sustancia en un momento determinado y las modificaciones que se producen al realizar una tarea o tras un estímulo
Permite visualizar aspectos como:— Metabolismo cerebral de la glucosa— Utilización del oxígeno por el cerebro (flujo)— Mecanismo de acción de psicofármacos— Densidad de receptores
Continúa

225
Exploraciones iconográficas: PET (cont.)
Principales hallazgos en la esquizofrenia:— Hipofunción prefrontal durante la
activación cognitiva— Aumento de flujo en el lóbulo temporal
izquierdo en pacientes con alucinaciones— Correlatos neurofuncionales para cada una
de las tres dimensiones sintomáticas principales de la esquizofrenia: positiva, negativa, desorganizada (Liddle y cols., 1992)

226
Exploraciones iconográficas: RMf
La RMf de perfusión permite trazar un mapa de perfusión cerebral en reposo o ante estímulos; se utiliza sobre todo para estudios vasculares
La difusión o DTI (diffusion tensor imaging) se emplea para estudiar cambios en las fibras de sustancia blanca
La contraste-BOLD (blood oxygen level dependent) detecta cambios regionales en la hemoglobina (oxigenada frente a desoxigenada) que acompañan a las variaciones de flujo. Es la exploración más utilizada en investigación
Continúa

227
Exploraciones iconográficas: RMf (cont.)
Principales hallazgos con la RMf:— Mayor flujo sanguíneo cerebral en las
regiones posteriores del cerebro— Tendencia a la lateralización patológica
(ipsilateral) — Incremento de la actividad en la corteza
auditiva primaria asociado a la presencia de alucinaciones auditivas

228
Exploraciones iconográficas:RM espectroscópica
Utilización de la RM para la función neuroquímica
Utilización sólo en investigación Principales hallazgos en la esquizofrenia:
— Disminución del N-acetilaspartato (marcador de integridad neuronal)
— Hipoactividad glutamatérgica y aumento de fosfodiésteres

229
Exploraciones iconográficas: SPECT
Tomografía computarizada por emisión de fotón único
Utiliza radionúclidos que emiten radiación gamma (fotones)
Visualiza el sistema nervioso central en tres dimensiones
Para los trastornos psiquiátricos clásicos no existen suficientes pruebas de que posea la sensibilidad o especificidad necesarias para el desarrollo de nuevas técnicas diagnósticas o pronósticas

230SPECT y PET de receptores.Respuesta terapéutica
y ocupacional de receptores
Técnicas cada vez más utilizadas para el desarrollo y la evaluación de nuevos antipsicóticos
La ocupación de entre el 53 y el 74% de los receptores D2 se acompaña de respuesta terapéutica, excepto en esquizofrenias resistentes (Kapur y cols., 1996)
La ocupación superior al 85% genera sintomatología extrapiramidal (Farde y cols., 1992)

231
Retos en el manejo y tratamiento ...................................... 232
Tendencias en cuidados ............................................. 233-234
Epidemiología.................................................................... 235
Factores de riesgo: cardiovasculares y metabólicos.......236-266
Estudio CATIE.............................................................267-277
Estudio CLAMORS.......................................................278-296
Guías de consenso......................................................297-328
Cuándo tratar y con qué..............................................329-347
8. Estado de salud general en pacientes esquizofrénicos.
Sobremorbilidad y sobremortalidad

232
Retos
Tratamiento— Personalizado— Integral

233
Conferencia Interministerial y OMS
Compromiso institucional de promoción y prevención en salud mental
Helsinki, 2005

234Tendencia en cuidados y tratamiento de la
esquizofrenia
Interés creciente por la mortalidad y morbilidad somática
Necesidad de evaluaciones globales de los pacientes esquizofrénicos (Mayer y Nasrallah, 2003)
La esquizofrenia como una enfermedad física— Brian Kirkpatrick. Barcelona, noviembre
2005

235
Epidemiolgía
Detección del síndrome metabólico— OMS (1998)— NECP (2001)
Síndrome metabólico: 2-4 veces más frecuente en esquizofrénicos
3 veces más depósitos de grasa intraabdominal Tasas elevadas de diabetes tipo 2
Thakore, Br J Psychiatry 2005

236
Síndrome metabólico y esquizofrenia: causalidad
¿Asociación genética entre esquizofrenia y diabetes?
Hiperactividad del eje hipotálamo-hipófiso-suprarrenal
Estilo de vida Tratamientos antipsicóticos e incremento de
peso
Thakore, Br J Psychiatry 2005

237
Efectos metabólicosde los antipsicóticos
Medline, 1975-2006 El tratamiento con diferentes antispicóticos se asocia con
efectos variables sobre el peso corporal, desde aumentos discretos (<2 kg) con amisulprida, ziprasidona y aripiprazol a incrementos importantes con olanzapina y clozapina (4-10 kg)
Los aumentos de la adiposidad se asocian con disminuciones de la sensibilidad a la insulina en las personas que sufren enfermedad mental y en las que no
Los efectos del aumento de la adiposidad y otros pueden contribuir al aumento de glucosa y lípidos en plasma observado durante el tratamiento con algunos antipsicóticos
El tratamiento con ciertos antipsicóticos se asocia con efectos metabólicos indeseables que pueden aumentar el riesgo de síndrome metabólico y de afecciones como prediabetes, diabetes no insulinodependiente y enfermedad cardiovascular
Newcomer y Haupt. Can J Psychiatry 2006; 51: 480-491

238Síndrome metabólico y enfermedad cardiovascular
Reaven, Drugs 1999; 58 (Suppl 1); NCEP III, Circulation 2002; 106
Tamaño corporal IMC
Adiposidad central
Resistencia a la insulina
Metabolismode la glucosa
Metabolismodel ácido úrico
Nuevos factoresde riesgo
± Intoleranciaa la glucosa
Ácido úrico Aclaramiento urinario de ácido úrico
Triglicéridos Lipemia PP HDL
4 PHLA5) LDL denso, pequeño
Actividad del SNS Retención de Na3) Hipertensión
PCR PAI-1 Fibrinógeno
Cardiopatía coronaria
PAI-1: inhibidor del activador del plasminógeno-1; PHLA: actividad lipolítica postheparina; PP: posprandial
Hiperinsulinemia
Dislipidemia Hemodinámica

239
Otros efectos Anticolinérgico Prolactina Prolongación QTc
Riesgo de hiperglucemia/diabet
es
DisforiaDiscinesia tardía
Sedación
Suicidabilidad
Síntomas negativo
s
Síntomas cognitivo
s
Síntomas
positivos
Factores inducidos por fármacos
Factores de la enfermedad
Relación entre factores de enfermedady factores adversos inducidos por
fármacos en la carga de la esquizofrenia
Síntomas diversos de la esquizofrenia
Efectos adversos de los antipsicóticos
Síntomas extrapiramidales Gananci
a de peso
Depresión/ ansiedad

240
Consideraciones clave
Alteraciones metabólicas como parte inherente de la esquizofrenia
Estilo de vida como factor contribuyente a la patología metabólica en los pacientes esquizofrénicos
Esquizofrenia como factor de riesgo independiente para el desarrollo de algunos trastornos metabólicos (intolerancia a la glucosa, diabetes, etc.)
Tratamiento antipsicótico como factor de riesgo añadido a la situación clínica global

241
Principales factores de riesgo para la cardiopatía coronaria
Fumar cigarrillos Hipertensión (140/90 mmHg) Bajo HDL-colesterol (<40 mg/dl) Historia de cardiopatía coronaria prematura en
parientes de primer grado (<56 años en hombres y <64 años en mujeres)
Edad (>44 años en hombres y >54 años en mujeres)
NCEP, 2001

242Predictores de cardiopatía coronaria y criterios de
síndrome metabólico Estudio de Framingham de 10 años
— Género— Edad— Fumador— LDL-colesterol o colesterol total— HDL-colesterol— Presión sanguínea
Wilson y cols., Circulation 1998

243
Mortalidad y esquizofrenia Menor esperanza de vida (Malzberg, 1934; Odegard,
1936; Alstrom, 1942; Black y Fisher, 1992; Mortensen, 2003)— La esperanza de vida a los 30 años de un varón es
de 8 años menos y la de una mujer es de 10 años menos (Hannerz y cols., 2001)
— La esperanza de vida es un 20% menor que en la población general (Newman y Bland, 1991)
Mayor mortalidad atribuible a (Brown, 1997; Brown y cols., 2000):— 60% a enfermedades físicas (cardiovasculares y
síndrome metabólico)— <28% a suicidio— 12% a accidentes
Ryan y Thakore, Life Sci 2002; Saari y cols., J Clin Psychiatry 2005

244Mortalidad comparada en la esquizofrenia y en población
general
Osby U, Correia N, Brandt L, Ekbom A, Sparen P. Mortality and causes of death in schizophrenia in Stockholm county, Sweden. Schizophr Res 2000; 45: 21-28
Causa de muerte Hombres Mujeres
Infecciosa 3,4 1,9
Respiratoria 3,2 2,7
Endocrina 2,7 2,0
Gastrointestinal 2,5 2,1
Cardiovascular 2,3 2,1
Urogenital 2,3 2,3

245Riesgo relativo de diabetes tipo 2
y antipsicóticos
Antipsicóticos atípicos: OR 4,7
Antipsicóticos de baja potencia: OR 3,3
Antipsicóticos de alta potencia: OR 2,6
Suvisaari J y cols., Schizophrenia Res 2006; 81 (Suppl): 24

246
Riesgos de salud con antipsicóticos
American Diabetes Association; American Psychiatric Association; American Association of Clinical Endocrinologists; North American Association for the Study of Obesity. Consensus Development Conference on Antipsychotic Drugs and Obesity and Diabetes. Diabetes Care 2004; 27: 596-601De Nayer A, De Hert M, Scheer A, Van Gaal L, Peuskens J. Belgian Consensus on metabolic problems associated with atypical antipsychotics. Int J Psychiatr Clin Pract 2005; 9: 130-137
Antipsicótico peso DiabetesEmpeoramiento
del perfil lipídico
Clozapina +++ + +
Olanzapina +++ + +
Risperidona ++ ? ?
Quetiapina ++ ? ?
Aripiprazol +/- - -
Ziprasidona +/- - -
Amisulprida +/- - -

247
Medidas: variable principal Riesgo de presentar enfermedad cardiovascular mortal en 10 años según SCORE*:
*Conroy RM y cols., Eur Heart J 2003; 24: 987-1003
Paso 1.
S0(edad) = exp -(exp())(edad-20)p S0(edad+10) = exp -exp()) (edad-10)p *Valores de los coeficientes y p según tabla A adjunta * El modelo de Weibull es tradicionalmente expresado en términos de = exp()
Paso 2. w = colesterol (colesterol –6) + PAS (PAS-120) + fumador (fumador actual)
Valores de los coeficientes colesterol, PAS y fumador según tabla B adjunta Colesterol en mmol/l y PAS en mmHg. Ser fumador se codifica como 1 si es fumador actual y 0 si es no fumador
Paso 3.
S(edad) = S0(edad)exp(w)
S(edad +10) = S0(edad+10)exp(w)
Paso 4. S10(edad) = S(edad +10)/S(edad)
Paso 5. Riesgo10 = 1-S10(edad)
Paso 6. Riesgo cardiovascular10 (edad) = [ECC_Riesgo (edad)]+[No-ECC_Riesgo (edad)]
Continúa

248
Medidas: variable principal (cont.) Riesgo de presentar enfermedad cardiovascular en 10 años según el estudio de Framingham*:
*Wilson PW y cols., Circulation 1998; 97: 1837-1847
Presión arterial PAS PAD
Presión óptima < 120 mmHg < 80 mmHg
Presión normal 120-129 mmHg 80-84 mmHg
Presión alta 130-139 mmHg 85-89 mmHg
Hipertensión de tipo I 140-159 mmHg 90-99 mmHg
Hipertensión de tipo II ≥160 mmHg ≥100 mmHg
Cuando la PAS y la PAD clasifican a un pacientes en dos tramos, se tomará el tramo con una clasificación más alta
Ecuación 1 (para hombres):L-Cholmen = (0,04826*edad) –0,65945 (si colesterol <160) + 0,17692 (si colesterol = 200-239) + 0,50539 (si colesterol = 240-279) + 0,65713 (si colesterol ≥280) + 0,49744 (si HDL <35) + 0,24310 (si HDL = 35-44) –0,05107 (si HDL = 50-59) –0,48660 (si HDL ≥60) –0,00226 (si presión óptima) + 0,28320 (si presión alta) + 0,52168 (si hipertensión de tipo I) + 0,61859 (si hipertensión de tipo II) + 0,42839 (si diabético) + 0,52337 (si fumador) –3,0975
Ecuación 1 (para mujeres):
L-Cholwomen = (0,33766*edad) – (0,00268*edad2) – 0,26138 (si colesterol <160) + 0,20771 (si colesterol = 200-239) + 0,24385 (si colesterol = 240-279) + 0,53513 (si colesterol ≥280) + 0,84312 (si HDL < 35) + 0,37796 (si HDL = 35-44) + 0,19785 (si HDL = 45-49) – 0,42951 (si HDL ≥60) – 0,53363 (si presión óptima) – 0,06773 (si presión alta) + 0,26288 (si hipertensión de tipo II) + 0,59626 (si diabética) + 0,29246 (si fumadora) – 9,92545
Ecuación 2:
B = eEcuación 1
Ecuación 3:Prob. = 1-[s(t)]B
s(t) (para hombres) = 0,90015s(t) (para mujeres) = 0,96246

249Riesgo a 10 años de cardiopatíacoronaria con antipsicóticos
de 2.a generación
Correll y cols., J Clin Psychiatry 2006
Paci
ente
s co
n c
ard
iopatí
a c
oro
nari
a (
%)
RR = 3,56(IC del 95% = 3,20 a 3,92)
N = 169 N = 198 N = 97 N = 66 N = 73 N = 78 N = 30 N = 23
2,30,5
3,4
8,48,3
2
11,5
20,1Mujeres
Hombres
25
0
5
10
15
20
Total 20-39 años 40-59 años 60-79 años
Sexo y grupo de edad

250
Factores de riesgo cardiovascular
Factores de riesgoPrevalencia estimada y riesgo relativo (RR)
Esquizofrenia Trastorno bipolar
Obesidad 111 45-55%, x1,5-2 RR1 26%5
Tabaquismo 1150-80%, x2-3 RR2 55%6
Diabetes 10-14%, x2 RR3 10%7
Hipertensión ≥18%4 15%5
Dislipidemia 111111111x>5 RR8
1Davidson y cols., Aust NZ J Psychiatry 2001; 2Allison y cols., J Clin Psychiatry 1999; 3Dixon y cols., J Nerv Ment Dis 1999; 4Herran y cols., Schizophr Res 2000; 5McElroy y cols., J Clin Psychiatry 2002; 6Ucok y cols., Psychiatry Clin Neurosci 2004; 7Cassidy y cols., Am J Psychiatry 1999; 8Alleveck, Schizophr Bull 1999

251
Criterios diagnósticos para el síndrome metabólico (NCEP)
Factor de riesgo Medida definida
Obesidad abdominal
Hombre 102 cm
Mujer 88 cm
Triglicéridos ≥ 150 mg/dl
HDL
Hombre <40 mg/dl
Mujer <50 mg/dl
Presión arterial ≥130/85 mmHg o en tratamiento
Glucosa≥110 a ≥ 100 mg/dl o en
tratamiento
Derivados del NCEP (National Cholesterol Education Program), ATP III, 2001.≥3 criterios para establecer el diagnóstico

252
Criterios diagnósticos para el síndrome metabólico (OMS)
Presencia de:— Diabetes mellitus tipo 2 — Intolerancia a la glucosa, o — Tolerancia a la glucosa normal con
resistencia a la insulina 2 o más de los siguientes factores:
— Hipertensión arterial ≥140/90 mmHg— Obesidad abdominal y/o IMC >30— HDL-colesterol <35 mg/dl — Hipertrigliceridemia ≥150 mg/dl— Microalbuminuria ≥30 mg/día
Alberti y Zimmet, Diabet Med 1998

253
Síndrome metabólico. Definición NCEP
Glucosa plasmática ≥110 mg/dl Obesidad abdominal
— Perímetro abdominal • Varones >102 cm • Mujeres >88 cm
— Índice de masa corporal >28,8 kg/m2 Triglicéridos ≥150 mg/dl HDL-colesterol
— Varones <40 mg/dl— Mujeres <50 mg/dl
Presión arterial ≥130/85 mmHg
NCEP (ATP III), JAMA 2001

254
Síndrome metabólico.Definición IDF
Obesidad abdominal (>94 cm o >80 cm) Factores de riesgo (≥2)
— Triglicéridos (>150 mg/dl)— HDL-colesterol (<40/<50 mg/dl)— Presión arterial (>130/85 mmHg)— Glucosa en plasma (>100 mg/dl) o diabetes
tipo 2
Consensus IDF, 2005

255
Síndrome metabólico
Patogénesis compleja Componentes múltiples Factores causales más reconocidos
— Obesidad abdominal• Fácilmente mensurable mediante el
perímetro abdominal— Resistencia a la insulina
Consensus IDF, 2005

256Síndrome metabólico: criterios adicionales para la
investigación
Distribución anómala de la grasa corporal Dislipidemia aterogénica ( triglicéridos, HDL) Disglucemia Resistencia a la insulina (otra que
hiperglucemia) Disregulación vascular (otra que hipertensión
arterial) Estado proinflamatorio Estado protrombótico Factores hormonales
Consensus IDF, 2005

257
Síndrome metabólico: componentes
Ford y cols., JAMA 2002
0
20
40
60
80
100
1+ 2+ 3+ 4+ 5
NHANES III CLAMORS
%

258
Esquizofrenia, antipsicóticos y riesgo cardiovascular
Intervalo QTc prolongado Efectos metabólicos: incremento de peso,
diabetes mellitus, incremento de triglicéridos Efectos en la presión sanguínea: hipotensión
ortostática Miocarditis y miocardiopatía
Glassman, J Clin Psychiatry 2005

259Síndrome metabólico y mortalidad cardiovascular en
Europa (DECODE)
Metaanálisis: 11 estudios prospectivos europeos
N: 6.156 hombres y 5.356 mujeres Seguimiento medio: 8,8 años Definición: ≥ 2 (obesidad, hipertensión arterial,
glucemia) Prevalencia en no diabéticos: 15%
— Hombres: 15,7%— Mujeres: 14,2%
Hu y cols., Arch Intern Med 2004

260Síndrome metabólico y riesgo de mortalidad cardiovascular
(Kuopio)
1.209 hombres finlandeses Rango de edad: 24-60 años RR de muerte por infarto
— 2,9-3,3 (criterios OMS)— 2,9-4,2 (criterios NECP)— 2,3 mortalidad global
Lakka y cols., JAMA 2002

261
Prevalencia del síndrome metabólico (OMS)
PaísPrevalencia (%)
Hombres Mujeres
España 19,3
Inglaterra 45 35
Holanda 18 8
India 37 47

262Prevalencia del síndrome metabólico en población
europea
Dellios G, Diabetes News 2005
EdadHombres (diámetro de cintura, 94 cm)
Mujeres (diámetro de cintura, 80 cm)
30-39 13,2% 10,3%
40-49 29,7% 20,2%
50-59 40,1% 35,6%
60-69 42,7% 45,9%
70-74 44,5% 54,2%
75-89 39,4% 58,4%

263
Prevalencia del síndrome metabólico (NHANES III)
Prevalencia ajustada por edad: 23,7%
8.814 adultos en Estados Unidos. NHANES, 1988-1994
Ford y cols., JAMA 2002; 287: 3
Edad
HombresMujeres
50
Pre
vale
nci
a (
%)
45
40
0
5
10
15
20
25
30
45
20-29 ≥7060-6950-5940-4930-39

264
Prevalencia del síndrome metabólico en la esquizofrenia
Autores, año, país Pacientes Criterios %
Heiskanen y cols., 2003 Finlandia
N = 35, ingresados, 44,5±9,86 años ATP-III 37
Kato y cols., 2003 EE.UU.
N = 48, ambulatorios, 40,2±12,01 años ATP-III 63 (hombres 54,1;
mujeres 70,8)
Littrell y cols., 2003 EE.UU.-Taiwán
N = 127, ingresados y ambulatorios ATP-III 22 ingresados,
51 ambulatorios
Basu y cols., 2004 EE.UU.
N = 33, ambulatorios, 44,5±7,8 años ATP-III 42,4
Cohn y cols., 2004 Canadá
N = 240, ingresados y ambulatorios,
43,3±11 añosATP-III 44,7
Saari y cols., 2005 Finlandia
N = 31, ambulatorios, 31 años ATP-III 19,4
McEvoy y cols., 2005 EE.UU.
N = 689, ambulatorios, 40,7±11 años ATP-III, AHA
40,9 (hombres 36; mujeres 51,6)
42,7 (AHA)
Meyer y cols., 2005 EE.UU.
N = 1.231, ambulatorios,
406±11,2 añosATP-III 35,8
Continúa

265Prevalencia del síndrome metabólico en la esquizofrenia
(cont.)
Autores, año, país
Pacientes Criterios %
Hägg y cols., 2006 Suecia
N = 269, ambulatorios, 46±13
añosATP-III 34,6
Meyer y cols., 2006 EE.UU.
N = 80, ambulatorios, 49
añosATP-III 51,2
De Hert y cols., 2006 Bélgica
N = 240, ingresados y ambulatorios, 36,5±11,8 años
ATP-III, AHA, IDF
28,4% (ATPIII)32,3% (AHA)
36% (IDF)
Correll y cols., 2006 EE.UU.
N = 367, ingresados, 42,9±15,3 años
ATP-III, IDF37,3 (ATPIII)
47,4 (IDF)
Bobes y cols., 2007 España
N = 1.452, ambulatorios,
39,3±11,6 añosATP-III
24,6 (hombres 23,6; mujeres
27,2)

266Factores de riesgo cardiovascular en población
española
Metaanálisis de estudios transversales— 48 estudios— N = 130.945— Frecuencia de factores de riesgo
• Hipertensión arterial en ancianos (66,7%)
• Sobrepeso/obesidad en mujeres adultas (48,3%)
• Tabaquismo en hombres (41,1%)• Colesterol total elevado (23%)• Diabetes (8%)
Medrano y cols., Med Clin (Barc) 2005

267
Resultados CATIE: primera fase
Riesgo a 10 años (esquizofrénicos frente a controles)— Hombres: 9,4% frente a 7,0%— Mujeres: 6,3% frente a 4,2%
Tasas de fumadores: 68% frente a 35% Diabetes: 13% frente a 3% Hipertensión: 27% frente a 17% HDL-colesterol: 43,7% frente a 49,3%
Goff y cols., Schizophr Res 2005 Continúa

268
Resultados CATIE: primera fase (cont.)
Riesgo de cardiopatía coronaria a 10 años
Goff y cols., Schizophr Res 2005
0
10
20
30
40
50
60
70
80
Hombres Mujeres Fumadores Diabetes Hipertensiónarterial
HDL-colesterol
CATIE NHANES
%

269
Conclusiones CATIE: primera fase
Incremento de la mortalidad cardíaca en pacientes esquizofrénicos
El impacto del consumo de cigarrillos es claro Deben clarificarse las contribuciones al riesgo
cardíaco de:— Antipsicóticos— Dieta— Ejercicio— Calidad de cuidados médicos
Goff y cols., Schizophr Res 2005

270Efectos metabólicos de los antipsicóticos
(CATIE)
Aumento medio de glucosa (mg/ dl)
0
5
10
15
OLZ QUE RISP PERF ZIPRA
Cambio medio del colesterol desde la situación inicial
-10-505
10
Lieberman y cols., N Engl J Med 2005
OLZ ZIPRAQUE RISP PERF
OLZ ZIPRAQUE RISP PERF
OLZ, olanzapinaQUE, quetiapinaRISP, risperidonaPERF, perfenazinaZIPRA, ziprasidona
p<0,001
Cambio medio de triglicéridos (mg/ dl)
-20
-10
0
10
20
30
40
50
Serie1
p<0,001

271Efectos neuroendocrinos de los antipsicóticos
(CATIE)
Lieberman y cols., N Engl J Med 2005
No hubo diferencias entre los grupos de tratamiento en el alargamiento del QTc
El uso de una dosis baja de perfenazina podría haber sido causa de que no apareciera diferencia en los porcentajes de efectos extrapiramidales
Cambio en los valores de prolactina
-10-505
101520
OLZ
ZIPRAQUE RISP PERF
p <0,001

272
Abandonos por efectos adversos (CATIE)
Abandono por aumento de peso o efecto metabólico
02
46
810
OLZ QUE RISP PERF ZIPRA
Abandono por efectos adversos
0
5
10
15
20
OLZ QUE RISP PERF ZIPRA
Lieberman y cols., N Engl J Med 2005
p <0,001
p = 0,002
Abandono por efectos extrapiramidales
012345678
OLZ QUE RISP PERF ZIPRA
Serie1

273
Resultados CATIE: primera fase
Análisis de 689 sujetos Prevalencia de síndrome metabólico
— 49% según criterios NCEP (National Cholesterol Education Program)
— 42% con criterios AHA (glucemia 100 mg/dl)• Mujeres: 51,6% (NCEP) frente a 54,2%
(AHA)• Hombres: 36% (NCEP) frente a 36,6%
(AHA)
McEvoy y cols., Schizophr Res 2005 Continúa

274
Resultados CATIE: primera fase (cont.)
Modelo de regresión logística (edad, raza y etnia)— Hombres: 138% CATIE > NHANES de
síndrome metabólico— Mujeres: 251% CATIE > NHANES de
síndrome metabólico Índice de masa corporal
— Hombres: 85% CATIE > NHANES de síndrome metabólico
— Mujeres: 137% CATIE > NHANES de síndrome metabólico
McEvoy y cols., Schizophr Res 2005

275
Conclusiones CATIE: primera fase
El síndrome metabólico es muy prevalente en pacientes esquizofrénicos en Estados Unidos
El síndrome metabólico representa una enorme fuente de riesgo cardiovascular, especialmente en mujeres
La atención clínica debe dirigirse a monitorizar el síndrome metabólico y minimizar el riesgo metabólico asociado con el tratamiento antipsicótico
McEvoy y cols., Schizophr Res 2005

276
Resultados CATIE: primera fase
1.231 sujetos con síndrome metabólico— 35,8% con criterios NCEP
Ajustados por edad, género, raza, etnia y lugar— SF-12: peor salud física (p<0,001)— PANSS: mayor preocupación somática
(p=0,03) Sin diferencias significativas en:
— Gravedad de síntomas, depresión, calidad de vida, neurocognición, salud mental autoevaluada
Meyer y cols., Schizophr Res 2005

277
Conclusiones CATIE: primera fase
El síndrome metabólico se asocia a: — Peor salud física— Incremento de preocupación somática
Necesidad de tomar un papel activo en la monitorización de la salud de estos pacientes con esquizofrenia por parte de los clínicos para minimizar el impacto de:— Comorbilidad médica— Mortalidad a largo plazo— Funcionamiento diario
Meyer y cols., Schizophr Res 2005

278
CLAMORS. Sexo y edad media
Bobes y cols., Schizophr Res 2007
Hombres (n=863) Mujeres (n=555) Total (n=1.452)p3
n1 % n1 % n1 %
Sexo - - - - 1.418 100,0 -
Hombre - - - - 863 60,9 -
Mujer - - - - 555 39,1 -
Edad 859 100,0 554 100,0 1.437 100,0 <0,001
<25 años 67 7,8 37 6,7 105 7,3
25-34 años 265 30,8 130 23,5 402 28,0
35-44 años 271 31,5 162 29,2 436 30,3
45-54 años 154 17,9 121 21,8 280 19,5
55-64 años 80 9,3 73 13,2 160 11,1
≥ 65 años 22 2,6 31 5,6 54 3,8
m1 DE m1 DE m1 DE p4
Edad (años) 39,3 11,6 42,5 12,6 40,7 12,2 <0,0011Algunos pacientes fallaron al facilitar información. 2Debido al trastorno psicótico. 3Test de chi cuadrado (p<0,05). 4Test de U de Mann-Whitney (p<0,05).

279
CLAMORS. Estado civil y ocupación
Bobes y cols., Schizophr Res 2007
Hombres (n=863) Mujeres (n=555) Total (n=1.452)p3
n1 % n1 % n1 %
Estado civil 856 100,0 550 100,0 1.431 100,0 <0,001
Soltero 653 76,3 288 52,4 958 66,9
Casado 145 16,9 172 31,3 324 22,6
Divorciado/separado 49 5,7 61 11,1 111 7,8
Viudo 9 1,1 29 5,3 38 2,7
Ocupación 845 100,0 534 100,0 1.403 100,0 <0,001
Activo 176 20,8 99 18,5 278 19,8
Desempleado 155 18,3 79 14,8 238 17,0
Baja por enfermedad 62 7,3 23 4,3 86 6,1
Pensión de incapacidad
411 48,6 243 45,5 666 47,5
Otros 41 4,9 90 16,9 135 9,61Algunos pacientes fallaron al facilitar información. 2Debido al trastorno psicótico. 3Test de chi cuadrado (p<0,05). 4Test de U de Mann-Whitney (p<0,05).

280CLAMORS. IMC, cintura, años de enfermedad y hospitalizaciones
1Algunos pacientes fallaron al facilitar información. 2Debido al trastorno psicótico. 3Test de chi cuadrado (p<0,05). 4Test de U de Mann-Whitney (p<0,05).
Bobes y cols., Schizophr Res 2007
Hombres (n=863)
Mujeres (n=555) Total (n=1.452)p3
n1 % n1 % n1 %
IMC 855 100,0 551 100,0 1.432 100,0 0,001
Normal (<25) 221 25,8 176 31,9 402 28,1
Sobrepeso (≥25-<30) 385 45,0 195 35,4 589 41,1
Obeso (≥30) 249 29,1 180 32,7 441 30,8
m1 DE m1 DE m1 DE p4
Perímetro de cintura (cm)
98,3 16,4 90,9 18,2 95,4 17,4 <0,001
Duración de la enfermedad (años)
14,7 10,4 16,6 11,3 15,5 10,8 0,002
N.o hospitalizaciones2 2,6 2,9 2,8 3,1 2,6 3,0 0,335

281
CLAMORS. Hábitos de vida saludables
Bobes y cols., Schizophr Res 2007
Hombres (n=863)
Mujeres (n=555)
Total (n=1.452)p3
n1 % n1 % n1 %
Pacientes que siguen dieta 100 11,6 135 24,3 238 16,5 <0,001
Control del consumo de calorías
122 14,3 176 31,9 302 21,1 <0,001
Control del consumo de sal 90 10,5 111 20,1 204 14,3 <0,001
Evitación del consumo de grasas saturadas/colesterol
157 18,4 181 32,8 341 23,8 <0,001
Consumo habitual de dieta rica en fibras
177 20,7 193 35,1 374 26,2 <0,001
1Algunos pacientes fallaron al facilitar información. 2Debido al trastorno psicótico. 3Test de chi cuadrado (p<0,05). 4Test de U de Mann-Whitney (p<0,05).

282CLAMORS. Prevalencia individual de riesgos
cardiovasculares
1Prevalencia calculada del total de pacientes evaluables o media (desviación estándar) con intervalo de confianza del 95%. 2Principales factores de riesgo según la SEA 2003. 5Test de chi cuadrado y test de U de Mann-Whitney.
Bobes y cols., Schizophr Res 2007
Total (n=1.452) Hombres (n=863) Mujeres (n=555)p5
%1 IC 95% %1 IC 95% %1 IC 95%
Edad ≥ 40 (♂) o ≥ 45 (♀) años2 42,9 40,3-45,5 44,4 41,0-47,7 40,6 36,5-44,7 0,165
Fumador2 53,7 51,1-56,2 62,3 59,1-65,6 40,4 36,3-44,4<0,00
1
Diabetes (tipos I, II y glucosa ≥126 mg/dl)
16,3 5,0-7,5 15,8 4,2-7,4 16,8 4,7-8,9 0,422
Hiperglucemia 17,9 6,5-9,3 17,5 5,8-9,3 18,5 6,2-10,8 0,523
Colesterol total ≥200 mg/dl2 50,9 48,2-53,6 49,3 45,8-52,8 52,6 48,2-57,0 0,249
HDL-colesterol <45 (♂) o <50 (♀) mg/dl2
43,7 40,9-46,6 43,9 40,2-47,6 46,1 41,4-50,8 0,472
PAS ≥140 o ≥130 mmHg (enfermedad cardiovascular, renal o diabetes previa)2
28,5 26,1-30,8 30,9 27,8-34,0 24,8 21,1-28,4 0,013
PAD ≥90 o ≥80 mmHg (enfermedad cardiovascular, renal o diabetes previa)2
22,0 19,9-24,2 22,0 19,2-24,8 21,1 17,6-24,5 0,690

283
CLAMORS. Prevalencia de riesgos cardiovasculares
3Calculado con la función SCORE (Conroy y cols., 2003). 4Calculado con la función Framingham (Wilson y cols., 1998), considerando como pacientes diabéticos aquellos con diabetes tipo I o II y/o glucosa ≥126 mg/dl. 5Test de chi cuadrado y test de U de Mann-Whitney.
Bobes y cols., Schizophr Res 2007
Total (n=1.452)
Hombres (n=863)
Mujeres (n=555) p5
% IC 95% % IC 95% % IC 95%
Riesgo de mortalidad cardiovascular (SCORE)3 en 10 años
0,9 0,8-1,0 1,1 0,9-1,2 0,5 0,4-0,6 <0,001
p5
Riesgo de cardiopatía coronaria en 10 años (Framingham)4
6,8 6,5-7,3 8,3 7,9-9,0 4,5 4,1-5,0 <0,001

284CLAMORS. Prevalencia totaly de componentes
del síndrome metabólico
1Porcentajes calculados del total de pacientes evaluables. 2Calculado según criterios NCEP-ATP III (2001). 3También incluye pacientes con diagnóstico de diabetes o que reciben tratamiento antidiabético. 4Test de chi cuadrado (p<0,05).
Bobes y cols., Schizophr Res 2007
Total (n=1.452)Hombres (n=863)
Mujeres (n=555) p4
%1 IC 95% %1 IC 95% %1 IC 95%
Pacientes (%) con síndrome metabólico2 24,6 22,4-26,8 23,6 20,8-26,5 27,2 23,5-30,9 0,130
Componentes del síndrome metabólico2
Obesidad abdominal (perímetro de cintura >102 (♂) o >88 cm (♀)
42,4 39,7-45,1 34,3 31,0-37,7 54,5 50,2-58,9<0,00
1
Hipertrigliceridemia (triglicéridos ≥ 150 mg/dl)
37,3 34,7-40,0 40,7 37,2-44,2 32,4 28,3-36,5 0,003
HDL-colesterol <40 (♂) o <50 (♀) mg/dl
35,4 32,6-38,2 28,5 25,1-31,9 46,1 41,4-50,8<0,00
1
Hipertensión (presión arterial ≥130/85 mmHg)
54,1 51,5-56,7 59,0 55,7-62,3 46,0 41,8-50,2<0,00
1
Hiperglucemia (glucosa ≥ 110 y 126 mg/dl y/o según el CRF) o diabetes (tipo I o II) o glucosa ≥ 126 mg/dl3
14,2 12,4-16,0 13,3 11,1-15,6 15,3 12,3-18,3 0,293

285CLAMORS. Valores mediosde los componentes
del síndrome metabólico
5Test de U de Mann-Whitney (p<0,05).
Bobes y cols., Schizophr Res 2007
Total (n=1.452)
Hombres (n=863)
Mujeres (n=555) p5
m DE m DE m DE
Índice de masa corporal (IMC) (kg/m2)
27,9 4,9 27,8 4,3 28,0 5,6 0,725
Perímetro de cintura (cm)
95,4 17,4 98,3 16,4 90,9 18,2<0,00
1
Triglicéridos 145,9 89,5 154,1 93,4134,
383,9 <0,001
HDL-colesterol 49,9 15,9 48,0 15,4 52,7 16,4 <0,001
Presión sistólica (mmHg) 127,1 15,8 128,8 15,0124,
416,7 <0,001
Presión diastólica (mmHg)
77,4 10,2 78,3 9,4 75,8 11,2 <0,001

286
CLAMORS. Riesgo cardiovascular (SCORE)
1Prevalencia calculada con respecto al global de pacientes evaluables con intervalo de confianza del 95%. 3Test de chi cuadrado entre hombres y mujeres.
Bobes y cols., Schizophr Res 2007
Porcentaje de pacientes con riesgo alto/muy alto de muerte a 10 años por cardiopatía coronaria (fatal y no fatal)
EdadTotal (n = 1.452) Hombres (n = 863) Mujeres (n = 555)
p3
%1 IC 95% %1 IC 95% %1 IC 95%
<25 años 10,0 0,0-3,6 10,0 0,0-6,2 10,0 0,0-10,7 NP
25-34 años 10,0 0,0-1,0 10,0 0,0-1,6 10,0 0,0-3,1 NP
35-44 años 10,3 0,2-1,3 10,4 0,1-2,3 10,0 0,0-2,6 1,000
45-54 años 15,8 2,5-7,7 10,6 5,4-15,9 10,0 0,0-3,3 <0,001
55-64 años 35,1 23,4-38,0 58,6 47,0- 70,1 19,4 2,2-16,5 <0,001
>65 años 81,6 63,9-87,1 95,2 77,3-99,2 71,4 54,7-88,2 0,059
Global 18,0 6,5-9,5 19,9 7,8-12,0 15,2 3,3-7,2 0,003

287
CLAMORS. Riesgo cardiovascular (Framingham)
1Prevalencia calculada con respecto al global de pacientes evaluables con intervalo de confianza del 95%. 3Test de chi cuadrado entre hombres y mujeres.
Bobes y cols., Schizophr Res 2007
Porcentaje de pacientes con riesgo alto/muy alto de desarrollar a 10 años cardiopatía coronaria (fatal y no fatal)
EdadTotal (n = 1.452) Hombres (n = 863) Mujeres (n = 555)
p3
%1 IC 95% %1 IC 95% %1 IC 95%
<25 años 0,0 0,0-3,6 0,0 0,0-5,4 0,0 0,0-9,4 NP
25-34 años 1,8 0,5-3,1 2,6 0,7-4,6 0,0 0,0-2,9 0,101
35-44 años 14,1 10,8-17,4 21,0 16,2-25,9 2,5 0,1-4,9 <0,001
45-54 años 36,0 30,3-41,7 50,0 42,1-57,9 18,2 11,3-25,1 <0,001
55-64 años 63,4 55,8-71,0 86,3 78,7-93,8 38,4 27,2-49,5 <0,001
>65 años 56,6 43,3-69,9 86,4 66,7-95,3 35,5 18,6-52,3 <0,001
Global 20,7 18,6-22,8 26,5 23,6-29,5 11,7 9,0-14,4 <0,001

288CLAMORS. Síndrome metabólico global y por
grupos de edad
1Prevalencia calculada con respecto al global de pacientes evaluables con intervalo de confianza del 95%. 3Test de chi cuadrado entre hombres y mujeres.
Bobes y cols., Schizophr Res 2007
Calculado según criterios NCEP-ATP III (2001)
EdadTotal (n = 1.452) Hombres (n = 863) Mujeres (n = 555)
p3
%1 IC 95% %1 IC 95% %1 IC 95%
<25 años 12,4 16,1-18,7 13,4 15,3-21,6 10,8 10,8-20,8 0,768
25-34 años 16,7 13,0-20,3 15,5 11,1-19,8 20,0 13,1-26,9 0,260
35-44 años 26,6 22,5-30,8 26,2 21,0-31,4 27,8 20,9-34,7 0,720
45-54 años 32,9 27,4-38,4 32,5 25,1-39,9 33,9 25,5-42,3 0,804
55-64 años 30,6 23,5-37,8 33,8 23,4-44,1 28,8 18,4-39,2 0,507
>65 años 35,2 22,4-47,9 22,7 15,2-40,2 45,2 27,6-62,7 0,093
Global 24,6 22,4-26,8 23,6 20,8-26,5 27,2 23,5-30,9 0,130

289Prevalencia del síndromemetabólico en pacientes
esquizofrénicos españoles
ND, no disponible.
Estudio País Pacientes n
Edad media (años) (DE)
Todos
Hombres (%)
Mujeres (%)
CLAMORS (Bobes y cols., 2007)
EspañaAmbulatori
os1.45
240,7
(12,2)24,6
%23,6 27,2
RICAVA (Cañas y cols., en prensa)
EspañaUnidad de
Agudos733
38,0 (11,3)
19% ND ND

290Prevalencia del síndrome metabólico en población general
española
ND, no disponible. 1Prevalencia de síndrome metabólico calculado con criterios NCEP modificados (IMC ≥ 28,8 kg/m2 como criterio para obesidad abdominal en sustitución de perímetro de cintura). 2Prevalencia de síndrome metabólico ajustada por la edad.
Bobes y cols., Schizophr Res 2007
Estudio (autor y año) Población n
Edad media (años) o
rango (DE) TodosHombre
s (%)Mujeres (%)
MESYAS (Alegría y cols., 2005)1 Laboral 7.256 45,4 (9,8) 10,2% ND ND
Oviedo (Álvarez-Cosmea y cols., 2005)
Pacientes de atención primaria
358 56,5 (10,4) 23,5% ND ND
Madrid (Coca Díaz y cols., 2005)
Pacientes de atención primaria
259 54,8 (18,1) 28,6% ND ND
Segovia (Martínez-Larrad y cols., 2005)
General 809 54,0 (11,5) 18,9% 16,8% 20,7%
DESIRE (Ascaso y cols., 2004)Pacientes de
atención primaria
4,232 >45 22,6% ND ND
ENCA (Álvarez León y cols., 2003)
General 578 >45 24,4% 24,5% 24,3%
VIVA (Lorenzo y cols., 2003) General 2.947 49,3 (13,1) 25,9% 20,8% 30,9%

291
Prevalencia del síndrome metabólico. Resumen
La prevalencia de factores de riesgo cardiovascular y de componentes del síndrome metabólico es elevada en pacientes con esquizofrenia, trastorno esquizofreniforme o trastorno esquizoafectivo
Esta prevalencia resulta especialmente elevada considerando la edad media de los pacientes analizados (40,7 ± 12,2 años, media ± DE)
El 8,2% de los pacientes muestran riesgo alto o muy alto (≥3%) de mortalidad cardiovascular en 10 años
El 22,1% de los pacientes muestran riesgo alto o muy alto (≥10%) de desarrollar enfermedad cardiovascular en 10 años
Continúa

292
Prevalencia del síndrome metabólico. Resumen (cont.)
La prevalencia de:— diabetes fue del 14,2% (6% en población
general)— síndrome metabólico fue del 24,6% (en
población general de la misma edad es del 18-19%)
— obesidad (IMC ≥30) fue del 30,8% (en población general es del 14-17%)
— obesidad abdominal fue del 42,4% (este valor es esperable en población general de 55-60 años)
— hipertensión superó el 50% (en la población general esta prevalencia es la esperable en pacientes de 55-60 años)

293
Síndrome metabólico y esquizofrenia
0
20
40
60
80
100
EE.UU.(NHANES III)
Finlandia Canadá España(CLAMORS)
EE.UU.
%
(CATIE)

294
Síndrome metabólico en España
Criterios OMS: modificados, no microalbuminuria
0
20
40
60
80
100
DESIRE ENCA VIVA VIVA(OMS)
VIVA(EGIR)
CLAMORS Segovia
Hombres Mujeres
(esquizofrenia)
(> 40 años) (Canarias)
%
Continúa

295
Síndrome metabólico en España (cont.)
0
20
40
60
80
100
Población general(OMS)
CLYDIA ENCA CLAMORS
%

296
Obesidad visceral comparada
0
20
40
60
80
100
Total Mujeres Hombres
NHANES III CLAMORS
%

297Frecuencia recomendada de detección y seguimiento
metabólico en pacientes bajo tratamiento antipsicótico
American Diabetes Association; American Psychiatric Association; American Association of Clinical Endocrinologists; North American Association for the Study of Obesity. Consensus Development Conference on Antipsychotic Drugs and Obesity and Diabetes. Diabetes Care 2004; 27: 596-601
Medida Inicio4
semanas
8 semana
s
12 semana
sTrimestr
al AnualCada 5 años
Historia personal/familiar
X X
Peso (IMC) X X X X X
Perímetro abdominal
X X
Presión arterial X X X
Glucemia X X X
Perfil lipídico X X X

298Manejo de la comorbilidad médica. Programa de pautas guía
MGH
V: visita. * Más frecuentes en circunstancias especiales (p. ej., tras el inicio de tratamiento antipsicótico).
Goff y cols., J Clin Psychiatry 2005
Inicial V V V V6
meses
V V V V V12
meses
Historia médica completa y revisión de sistemas X
Pruebas de laboratorio y ECG recientes X
Preguntar sobre el tabaquismo y evaluar la receptividad para dejarlo
X X X X X X X X X X X X
Peso, talla, IMC* X X X
Presión arterial y pulso X X X
Comunicar con el médico de atención primaria X X X
Evaluar el nivel de conocimiento: factores de riesgo y proporcionar materiales educativos
X X X
Revisión de nuevos síntomas somáticos X X X X X X X X X X X
Preguntar sobre cambios de medicación X X X X X X X X X X X
Glucosa en ayunas* X X
Test de screening (p. ej., Papanicolaou, mamografía, colonoscopia realizados en el último año)
X X
Revisar el estado de inmunización (purified protein derivate, hepatitis B, neumococos y tétanos)
X X
Revisar la seguridad de la residencia (detectores de humo, eliminar armas de fuego)
X X
Revisar hábitos saludables (p. ej., ejercicio, cinturón de seguridad)
X X

299
Síndrome metabólico: implicaciones clínicas
Necesidad de atención y manejo de los aspectos metabólicos de estos pacientes
Necesidad de reducir los riesgos relativos de pérdida de salud
Necesidad de reducir los riesgos relativos de pérdida de vida
Necesidad de promocionar actividades y estilos de vida saludables

300
Componentes de la visitaantes de la prescripciónde antipsicóticos de 2.a
generación
Historia médica, centrada en problemas metabólicos y en la historia familiar:— Síntomas, resultados de pruebas de laboratorio y exploraciones
especiales, si alguno está relacionado con el diagnóstico de diabetes
— Registrar glucemia en ayunas, test de tolerancia oral a la glucosa o HbA1c (hemoglobina glucosilada) previos
— Historia familiar de diabetes o sobrepeso/obesidad— Patrones de comidas, estado nutricional, historia del peso— Historia de ejercicio— Otras medicaciones que puedan afectar a los niveles de
glucemia (valproato, litio, etc.)— Factores de riesgo de aterosclerosis: fumar, hipertensión,
obesidad, dislipidemia e historia familiar— Educación sobre nutrición, actitudes y creencias de salud
previas— Tabaco, abuso de alcohol y/o uso controlado de sustancias
De Nayer A, De Hert M, Schee A, Van Gaal L, Peuskens J. Belgian Consensus on metabolic problems associated with atypical antipsychotics. Int J Psychiatr Clin Pract 2005; 9: 130-137 Continúa

301
Componentes de la visitaantes de la prescripción
de antipsicóticos de 2.a generación (cont.)
Exploración física— Medidas de talla y peso, calculando el índice de masa
corporal (IMC)— Perímetro de la cintura (medida entre la cresta ilíaca y el
cartílago costal inferior)— Examen físico en profundidad— Presión sanguínea
Pruebas de laboratorio— Glucemia en ayunas— Perfil lipídico en ayunas (colesterol total, LDL, HDL y
triglicéridos) Orientación
— En el riesgo asociado de diabetes con la enfermedad subyacente y con antipsicóticos de 2.a generación
— En signos de cetoacidosis y otras complicaciones diabéticas— En cuestiones de estilo de vida (dejar de fumar, nutrición,
automonitorización del peso)De Nayer A, De Hert M, Schee A, Van Gaal L, Peuskens J. Belgian Consensus on metabolic problems associated with atypical antipsychotics. Int J Psychiatr Clin Pract 2005; 9: 130-137 Continúa

302
Consenso belga: puntos clave Se prefieren los antipsicóticos con el perfil de menor riesgo
(amisulprida, aripiprazol, ziprasidona) Deben identificarse tempranamente, antes del inicio del
tratamiento con antipsicóticos de 2.a generación, los pacientes que tengan factores de riesgo de presentar complicaciones metabólicas
La frecuencia de monitorización debe adaptarse al estado metabólico del paciente y al perfil de riesgo para la elección del antipsicótico de 2.a generación
Los trastornos metabólicos emergentes por el tratamiento justifican el cambio del antipsicótico de 2.a generación a uno con perfil de menor riesgo de complicaciones en colaboración con el médico de atención primaria/endocrinólogo
Los pacientes deberían ser informados sobre el manejo de su enfermedad mental y el riesgo metabólico asociado a los antipsicóticos de 2.a generación De Nayer A, De Hert M, Schee A, Van Gaal L, Peuskens J. Belgian Consensus
on metabolic problems associated with atypical antipsychotics. Int J Psychiatr Clin Pract 2005; 9: 130-137

303Mantenimiento de la salud metabólica
y cardiovascular en pacientes conesquizofrenia: perspectivas a largo
plazo
Para identificar inequívocamente el origen de los efectos adversos, se deben intentar ensayos seriados en monoterapia antes de un tratamiento combinado
Un tratamiento farmacológico solamente tras un ensayo de duración adecuada y a dosis apropiadas
Los pacientes deberían ser monitorizados y educados continuamente para prevenir resultados adversos y controlar los que puedan aparecer
Gelenberg, Levy, Manoukian, 2004

304
Síndrome metabólico: conclusiones CLAMORS
La prevalencia de factores de riesgo cardiovascular y componentes del síndrome metabólico fue elevada entre pacientes con esquizofrenia, trastorno esquizofreniforme o trastorno esquizoafectivo (40,7 ±12,2 años, media ± DE)
La prevalencia de factores de riesgo y síndrome metabólico aumenta con la impresión clínica de gravedad (ICG-G) y con el insuficiente control de los síntomas esquizofrénicos
Los valores de prevalencia encontrados son equivalentes a los de la población general con 15-20 años más de edad
Una prevención deseable implica mejorar la calidad de los cuidados y atención de los pacientes esquizofrénicos, tanto en asistencia primaria como en especializada

305
Síndrome metabólico: guías clínicas publicadas
Physical Health Monitoring of Patients with Schizophrenia. Am J Psychiatry 2004; 161: 1334-1349
Consensus Development Conference on Antipsychotic Drugs and Obesity and Diabetes. Diabetes Care 2004; 27: 596-601
Medical Morbidity and Mortality in Schizophrenia: Guidelines for Psychiatrists. J Clin Psychiatry 2005; 66: 183-194
Consenso español de salud física del paciente con esquizofrenia. Congreso de la Asociación Europea de Psiquiatría, Madrid, marzo 2007

306
Monitorización de la salud física en la esquizofrenia
Objetivo: recomendaciones para mejorar la monitorización de la salud física en pacientes con esquizofrenia— Paciente adulto, ambulatorio, tratado con
antipsicóticos atípicos— Se revisan las patologías más negativamente
afectadas por la medicación antipsicótica— Se excluye la evaluación de tabaquismo,
abuso de drogas y alcoholismo — Sólo intervenciones susceptibles de ser
incorporadas en la práctica habitual del psiquiatra
Marder, 2004 Continúa

307
Monitorización de la salud físicaen la esquizofrenia (cont.)
Marder, 2004 Continúa
DIABETES
Monitorización a los 4 meses tras el inicio
del tratamientoy posteriormente anual
Referencia a medicina interna o atención primaria
Si hay diagnóstico de diabetes
Glucosa (ayunas)/hemoglobina A1c(todos los pacientes al inicio del tratamiento)
Monitorización periódica de síntomas
Si hay síntomasde diabetes
Si hay factores de riesgo para diabetes
Test de glucosa;Si es positivo

308
Monitorización de la salud físicaen la esquizofrenia (cont.)
Esquizofrénicos: grupo de alto riesgoSeguimiento de recomendaciones
NCEPMarder, 2004 Continúa
Referencia a atención primaria
HIPERLIPIDEMIA
Al menos 1 vez cada2 años
Referencia a medicina interna o atención primariaCambio de dieta
Inicio de antihipercolesterolémico
Si LDL >130 mg/dl
Perfil lipídico(todos lo pacientes al inicio del tratamiento)
Monitorización para síndrome metabólico
1 vez cada 6 meses
Si los niveles de LDL son normales

309
Monitorización de la salud físicaen la esquizofrenia (cont.)
PROLONGACIÓN DEL INTERVALO QT
Ziprasidona puede ser prescrita sin necesidad de monitorización
No ziprasidon
a
Si ziprasidona, ECG basalantes de iniciar tratamiento(+ ECG de seguimiento si haysíntomas de prolongación delintervalo QT)
ECG
Sin factores de riesgo
cardiovascular
Marder, 2004 Continúa
Con factores de riesgo
cardiovascular

310
Monitorización de la salud físicaen la esquizofrenia (cont.)
ELEVACIÓN DE LOS NIVELES DE PROLACTINA Y DISFUNCIÓN SEXUAL
Niveles de
prolactina
Preguntas de screeningen cada visita tras el inicio o hasta la estabilización de las dosis. Después, anualmente
Si se toman antipsicóticos que elevan los niveles de prolactina + respuesta
positiva a preguntas
Niveles de prolactina + causalidad+ considerar cambio de antipsicótico
Marder, 2004 Continúa
Si con antipsicóticos que elevan los niveles
de prolactina
Preguntas de screening(todos los pacientes al inicio del tratamiento y posteriormente de
forma anual)
Si indicios clínicos

311
Monitorización de la salud físicaen la esquizofrenia (cont.)
EFECTOS ADVERSOS EXTRAPIRAMIDALES, ACATISIA Y DISCINESIA TARDÍA
Monitorización semanal hasta la
estabilización de las dosis; hasta 2
semanas tras el inicio del
tratamiento/aumento significativo de
dosis
Si se toman antipsicóticos típicos:
monitorización de discinesia tardía cada
6 meses; si se toman antipsicóticos
atípicos, cada 12 meses
Si pacientes de alto riesgo (anciano, acatisia, etc.):
monitorización cada 3 meses si se toman
antipsicóticos típicos; cada 6 meses si se
toman antipsicóticos atípicos
Alteraciones del movimiento(todos los pacientes antes de iniciar el
tratamiento)
Marder, 2004 Continúa

312
Monitorización de la salud físicaen la esquizofrenia (cont.)
CATARATAS
Si mayor de 40 años: revisión ocular anual
Si menor de 40 años:revisión ocular cada 2
años
Anualmente, monitorización (preguntas al paciente) de alteraciones visuales
MIOCARDITIS EN PACIENTES CON CLOZAPINA
Recuento sanguíneo de leucocitos Niveles plasmáticos de troponina
Retirada de clozapina y referencia a atención primaria
Si sospecha de miocarditis Si diagnóstico de miocarditis
Especial atención a síntomas de miocarditis (fatiga, disnea, fiebre, palpitaciones)
Marder, 2004

313Conferencia de Consensoen fármacos antipsicóticos,
obesidad y diabetes
Conclusiones principales:— Consideración de los factores de riesgo
metabólicos al iniciar tratamiento con antipsicóticos de 2.a generación
— Actitud educacional en paciente, familia y cuidadores
— Monitorización inicial y seguimiento periódico
— Referencia de los pacientes a servicios especializados cuando sea oportuno
ADA, 2004

314Morbilidad y mortalidad médicaen esquizofrenia: pautas guía
para psiquiatras
Objetivo: conocer los factores de riesgo modificables presentes en la población esquizofrénica y definir recomendaciones para su diagnóstico y tratamiento— Factores de riesgo cardiovascular
• Tabaquismo, obesidad, diabetes mellitus, alteraciones lipídicas, hipertensión arterial
— Enfermedad infecciosa• VIH, hepatitis B y C
— Enfermedad pulmonar• Tuberculosis
Goff, 2005 Continúa

315Morbilidad y mortalidad médicaen esquizofrenia: pautas guía
para psiquiatras (cont.)
Resultados (presencia del factor de riesgo en población esquizofrénica):— Factores de riesgo cardiovascular:
• Tabaquismo: 85% frente a 23% en población general• Obesidad
IMC superior en mujeres esquizofrénicas. Similar en hombres
Uso de antipsicóticos atípicos, potencial causa de aumento de obesidad
• Diabetes mellitus (DM): Tasas superiores de DM tipo II en pacientes
esquizofrénicos Potencial relación con medicación antipsicótica
• Alteraciones lipídicas: asociación de antipsicóticos (cloazapina, olanzapina) e hipertrigliceridemia
• Hipertensión: sin conclusiones en población esquizofrénica
Goff, 2005 Continúa

316Morbilidad y mortalidad médicaen esquizofrenia: pautas guía
para psiquiatras (cont.)
Resultados (presencia del factor de riesgo en población esquizofrénica): — Enfermedad infecciosa:
• VIH: prevalencia 8 veces superior (enfermos mentales) • Hepatitis B y C: tasas 5 y 11 veces superiores (enfermos
mentales)— Enfemedad pulmonar:
Prevalencia de tuberculosis sin determinar en enfermos mentales
No obstante, el riesgo aumenta en centros de larga estancia e indigentes
Goff, 2005 Continúa

317Morbilidad y mortalidad médicaen esquizofrenia: pautas guía
para psiquiatras (cont.) Resultados (recomendaciones):
— Factores de riesgo cardiovascular:• Tabaquismo
Sólo tras mejora de los síntomas psíquicos y si no existe depresión mayor
Terapia conductual + 8-12 semanas de tratamiento con bupropión o nortriptilina
Estrecho seguimiento de síntomas clínicos durante el proceso (efectos adversos de la medicación)
• Obesidad Intervención recomendada si IMC ≥30 o ≥20+2 factores
de riesgo cardiovascular Cambio de antipsicótico si aumento de peso >5%, IMC >1
unidad, o perímetro abdominal >35 (mujeres) o >40 (hombres)
La eficacia de programas psicoeducacionales en esta población requiere un mayor análisis
• Diabetes mellitus: referencia al Consenso ADA • Alteraciones lipídicas: evaluación anual de parámetros lipídicos
Goff, 2005 Continúa

318Morbilidad y mortalidad médicaen esquizofrenia: pautas guía
para psiquiatras (cont.)
Resultados (recomendaciones): — Enfermedad infecciosa: VIH, hepatitis
• Programas de educación conductual• Pruebas de diagnóstico
Acceso a servicios de salud— Desenlace clínico peor en pacientes esquizofrénicos que en la
población general— Los psiquiatras han de asumir un rol principal ante estos pacientes
Goff, 2005

319
Resumen de las guías clínicas (EE.UU.)
Marder, 2004 ADA, 2004 Goff, 2005
Objetivo
Mejorar la detección y
seguimiento de la morbilidad física
Mejorar la detección y seguimiento de los
factores de riesgo cardiovascular
Mejorar la detección y
seguimiento de factores de riesgo modificables para morbilidad física
Población Ambulatoria, tratada con AP
Tratada con antipsicóticos de 2.a
generación
Población esquizofrénica
Metodología
Literatura x x x
Reunión Consenso x x Discusión
Formato del documento final
Artículo + tabla Recomendaciones
por factor de riesgo/ patología
Artículo Artículo + tabla
Recomendaciones por visita
Continúa

320
Resumen de las guías clínicas (EE.UU.) (cont.)
Marder, 2004 ADA Goff, 2005
Criterio
Morbilidad/factor de riesgo derivada del
tratamiento antipsicótico
Factores de riesgo cardiovasculares
derivados del tratamiento con
antipsicóticos de 2.a generación
Factores de riesgo modificables
Factor de riesgo/enfermedad
Obesidad x x
Diabetes x x x
Hiperlipidemia x x x
Intervalo QTc x
Miocarditis x
Aumento de prolactina x
Efectos extrapiramidales x
Cataratas x x
Hipertensión arterial x
Tabaquismo x
Enfermedades infecciosas (VIH, hepatitis)
x
Enfermedad pulmonar (tuberculosis) x
Acceso a servicios de salud x

321
Consenso Español de Salud Física del Paciente con Esquizofrenia
1. La Sociedad Española de Psiquiatría y la Sociedad Española de Psiquiatría Biológica consideran que el nivel de discapacidad y un menor estado de salud física de los pacientes con esquizofrenia pueden llegar a ser muy importantes debido a factores inherentes a la propia enfermedad, a malos hábitos de vida y a los tratamientos antipsicóticos
2. La Estrategia Europea de Salud Mental y la OMS invitan a mejorar el estado de salud física de los pacientes con enfermedades mentales y al empleo de medidas preventivas y de promoción de la salud
3. Los pacientes con esquizofrenia en general, y en nuestro país en particular, presentan mayor incidencia de patología cardiovascular, respiratoria, metabólica e infecciosa (sobremorbilidad) y un mayor riesgo de mortalidad global, tanto por causas naturales como específicas (respiratorias, cardiovasculares y neoplásicas)
4. El estado de salud física de los pacientes con esquizofrenia puede y debe mejorarse con un mayor grado de intervención sobre los factores de salud modificables y con la realización de formación continuada de los psiquiatras clínicos al respecto
5. Las características de los pacientes con esquizofrenia y la necesidad de utilización de tratamientos farmacológicos antipsicóticos que pueden tener impacto sobre la salud física hacen necesaria una mayor toma en consideración del estado de salud física de los pacientes por parte de los psiquiatras
Sociedad Española de Psiquiatría y Sociedad Española de Psiquiatría Biológica, 2007 Continúa

322Consenso Español de Salud Física del Paciente con Esquizofrenia
(cont.) 6. Las recomendaciones internacionales y nacionales formuladas
recientemente precisan adaptación al contexto español de la asistencia a la salud mental
7. Para conseguir los objetivos generales y específicos de mejora de la salud física del paciente con esquizofrenia se recomiendan actuaciones dirigidas a la prevención, diagnóstico, manejo y monitorización de las diferentes patologías concomitantes, factores y comportamientos de riesgo
8. La Sociedad Española de Psiquiatría y la Sociedad Española de Psiquiatría Biológica consideran necesario mejorar el acceso de los pacientes con esquizofrenia a los recursos asistenciales y/o de salud, así como el grado de coordinación entre la asistencia especializada y/o la asistencia primaria para el mejor manejo de la salud física de estos pacientes
9. Se considera necesario desarrollar y aplicar programas psicoeducativos incorporando los aspectos de salud física usualmente deteriorados en estos pacientes
10. Al objeto de mejorar el estado de salud física de los pacientes con esquizofrenia, se considera imprescindible contar con un historial clínico completo y alternativas terapéuticas integradas que incorporen particularmente la atención a los aspectos de salud física del paciente
Sociedad Española de Psiquiatría y Sociedad Española de Psiquiatría Biológica, 2007 Continúa

323Consenso Español de Salud Física del Paciente con
Esquizofrenia (cont.) Para el desarrollo de este decálogo se consideran imprescindibles las siguientes medidas de evaluación,
monitorización e intervención en el paciente con esquizofrenia
Sociedad Española de Psiquiatría y Sociedad Española de Psiquiatría Biológica, 2007
Protocolo de monitorización en el paciente con esquizofrenia
Parámetros que monitorizar Basal 3 m 6 m 12 m 18 m 24 m Observaciones
Historia clínica y antecedentes familiares
Valoración de deseo de deshabituación y seguimiento de las fases de cambio
Hábitos tóxicos Basal y seguimiento si factores de riesgo cardiovascular
ECG
Presión arterial y frecuencia cardíaca basal
Peso (IMC) y perímetro abdominal
Hemograma (perfil básico)
Bioquímica: perfil lipídico, glucemia, función hepática, VIH, sífilis
1 vez al año o si > 125 mg/dl repetir en la siguiente visita o a las 10 semanas y a los 6 meses de un cambio de tratamiento antipsicótico o tras un incremento de peso > 5%
Determinación de prolactina y valoración clínica de galactorrea
1 vez al año
Análisis sistemático de orina y creatinina basal
En caso de adicción a drogas repetir cada 3 meses
Determinación de papilomavirus (en pacientes mujeres de alto riesgo)
1 vez al inicio. Repetir si hay prácticas de riesgo
Valoración clínica de patología respiratoria
Al inicio
Valoración clínica de alteraciones visuales
Revisión según protocolo de la Sociedad de Oftalmología
Valoración clínica del estado dental Revisión según protocolo de la Sociedad de Estomatología
Revisión de la medicación antipsicótica

324Tasas de mortalidadpor enfermedades médicas
en enfermos mentales
Incremento del riesgo de muerte por causas médicas en la esquizofrenia y 20% vida más corta
Los trastornos afectivos unipolar y bipolar también se asocian con tasas mayores por causas médicas— 1,9 hombres/2,1 mujeres en el trastorno
bipolar— 1,5 hombres/1,6 mujeres en el trastorno
unipolar La mortalidad cardiovascular en la esquizofrenia
se incrementó en 1976-1995, con un mayor incremento en hombres desde 1991-1995
Manu, APA 2006

325
Elevación de triglicéridos y disminución de HDL-colesterol
Obesidad Inactividad física Fumar cigarrillos Consumo excesivo de alcohol Dieta elevada en carbohidratos (>60% de la energía
consumida) Enfermedades (diabetes mellitus tipo II, insuficiencia
renal crónica, síndrome nefrótico) Fármacos (corticosteroides, estrógenos, retinoides,
esteroides anabolizantes, dosis altas de -bloqueantes) Dislipidemias genéticas (presentaciones familiares de
hipertrigliceridemia, combinación de hiperlipidemia y disbetaliproteinemia)
NCEP, 2001

326
Niveles de triglicéridos
Normal: <150 mg/dl Límite alto: 150-190 mg/dl Alto: 200-499 mg/dl Muy alto: >500 mg/dl

327
No HDL-colesterol
La NCEP ATP utiliza la terminología no HDL-colesterol para indicar triglicéridos ricos de restos de liproproteínas como VLDL e IDL
No HDL-colesterol: — Colesterol total – HDL-colesterol— LDL + VLDL
NCEP, 2001

328Triglicéridos elevados como factor de riesgo independiente
La NCEP ATP III ha determinado que la elevación de los niveles de triglicéridos es un factor de riesgo independiente para la enfermedad cardiovascular aterogénica, basada en los datos que muestran que los triglicéridos ricos en lipoproteínas, especialmente VLDL, IDL y apolipoproteína B (restos de lipoproteínas), se correlacionan directamente con la progresión de la aterosclerosis
NCEP, 2001

329
Tratamiento: pautas guía
Identificar no HDL-colesterol como un objetivo terapéutico secundario tras las LDL-colesterol en pacientes con triglicéridos >200 mg/dl
Los niveles de HDL-colesterol son 30 mg/dl superiores al objetivo de LDL-colesterol para pacientes en categorías de riesgo (niveles normales de VLDL son ≤ 30 mg/dl)
El paso más importante en el tratamiento con triglicéridos elevados es situar el LDL-colesterol en los niveles del objetivo o por debajo
NCEP, 2001

330
Cuándo iniciar el tratamiento
Manu, APA 2006
Riesgo
LDL-colesterol
(mg/dl)
Iniciar cambios
terapéuticos de estilo de vida (mg/dl)
Farmacoterapia (mg/dl)
Alto: cardiopatía coronaria o riesgo equivalente (riesgo 10 años >20%)
<100 (opcional <70)
≥100
≥100 (<100
considerar farmacoterapia
)
Moderadamente alto: ≥2 factores de riesgo (riesgo 10 años 10-20%)
<130 ≥130 ≥130
Moderado: ≥2 factores de riesgo (riesgo 10 años <10%)
<130 ≥130 ≥160
Bajo: 0-1 factores de riesgo <160 ≥160 ≥190

331
Inhibidores de la HMG-CoA reductasa (estatinas)
Efectos secundarios habituales— Dolor abdominal, diarrea, flatulencia
Reacciones graves— Miopatía (rabdomiólisis manifestada por dolor,
incremento de la CPK, <1% de pacientes), pancreatitis
Contraindicaciones— Situaciones: enfermedad hepática activa, embarazo— Interacciones farmacológicas: fibratos (menor riesgo
con fenofibrato en comparación con gemfibrozilo), ácido nicotínico, ciclosporina, antibióticos macrólidos, antidepresivos
Manu, APA 2006

332Interacciones entre antidepresivosy estatinas: riesgo de rabdomiólisis
y trananimitis
Las interacciones son producidas por la inhibición del citocromo P450 isoenzima 3A4, que incrementa el nivel en plasma de estatinas metabolizadas por la misma isoenzima— Atorvastatina: nefazodona, trazodona— Lovastatina: escitalopram, citalopram,
fluvoxamina— Simvastatina: venlafaxina, mirtazapina
Una combinación segura podría incluir rosuvastatina (no metabolizada por el P450) y fluoxetina, paroxetina y sertralina
Karnik y Maldonado, 2005

333Dosis de estatinas para reducir el 30-40% los niveles
de LDL
Manu, APA 2006
Fármaco Dosis (mg/dl) LDL (%)
Atorvastatina 10 40
Lovastatina 40 30
Pravastatina 40 35
Simvastatina 20-40 35-40
Fluvastatina 40-80 25-35
Rosuvastatina 05-10 40-45

334
Diabetes: consideraciones estratégicas
El síndrome metabólico incrementa sustancialmente el riesgo de diabetes mellitus tipo 2
La diabetes mellitus tipo 2 es un trastorno heterogéneo, caracterizado por disminuir la sensibilidad a la insulina (resistencia a la insulina) en hígado, músculo y tejido adiposo y deteriorar el funcionamiento de las células beta
Las intervenciones farmacológicas son obligatorias en pacientes con diabetes mellitus establecida
Manu, APA 2006

335Cuándo iniciar tratamiento farmacológico para la
diabetes
HbA1c ≥7% Glucosa en ayunas >126 mg/dl Fracaso en la modificación del estilo de vida Otras pruebas (niveles de insulina en ayunas,
HOMA para glucosa e insulina en ayunas, test de tolerancia oral a la glucosa, muestreo frecuente de tolerancia intravenosa a la glucosa, pinza hiperinsulinémica euglucémica) no se consideran necesarias en la práctica clínica habitual
Manu, APA 2006
HOMA, Homeostasis Model Assessment

336Hipoglucemiantes orales en el síndrome
metabólico
Agentes adyuvantes de la insulina— Biguanida (metformina)— Tiazolidindionas (soriglitazona, pioglitazona,
troglitazona)— Inhibidores de la -glucosidasa (acarbosa)
Agentes que aumentan la insulina— Sulfonilureas— Meglitinidas
Manu, APA 2006

337
Trastornos psiquiátricos y diabetes
EsquizofreniaTrastorno esquizoafectivo
Antipsicóticos
atípicos
Estilo de vida no
saludable
Síndrome metabólico(común)
Cetoacidosis(excepcional)
DiabetesGlucosa en ayunas afectada/tolerancia a la glucosa afectada
Resistencia ala insulina
Secreción de insulinadefectuosa
Efectos independientes en peso
Efectos relacionados
en peso
Efectos independiente
s en peso
Efectos relacionados en peso
Scheen AJ, De Hert MA. Diabetes and Metabolism 2007

338
Trastornos psiquiátricos y diabetes
Anomalías de la glucosa en relación con el tratamiento antipsicótico en un estudio transversal de 415 pacientes con esquizofrenia o trastorno esquizoafectivo, reclutados durante 2 años
Scheen AJ, De Hert MA. Diabetes and Metabolism 2007
Diabetes (N = 26) Prediabetes (N = 97)
1.a generación (N = 87) 113,5% (3) 1125,5% (22)*
Amisulprida (N = 32) 0% (0) 16,3% (2)
Aripiprazol (N = 4) 0% (0) 0% (0)
Clozapina (N = 74) 119,6% (7) 1140,5% (30)
Risperidona (N = 98) 115,1% (5) 1121,4% (21)
Quetiapina (N = 53) 119,4% (5) 111,3% (6)
Olanzapina (N = 139) 115,8% (8) 1123,7% (33)
*12 pacientes combinaban antipsicóticos de 1.a generación con uno de 2.a generación.

339
Presión arterial
Manu, APA 2006
Categoría PAS (mmHg) PAD (mmHg)
Óptima <120 Y <80
Normal <130 Y <85
Normal-alta 130-139 O 85-89
Hipertensión
Fase 1 140-159 O 90-99
Fase 2 160-179 O 100-109
Fase 3 180 O 110

340Farmacoterapia para la hipertensión no
emergente
CVD Guidelines, 2006
Clasificación de la presión arterial
Farmacoterapia inicial sin indicaciones imperiosas
Fase 1 Diurético tipo tiazida para la mayoría
Fase 2Combinación de 2 fármacos (diurético tipo tiazida
y ECA/BRA/betabloqueante/antagonista del calcio)
ECA: enzima convertidora de la angiotensina; BRA: bloqueador del receptor de aldosterona.

341
Obesidad: opciones
Sibutramina* Fentermina* Dietilpropión* Orlistat* Fluoxetina Bupropión Topiramato
Sertralina Zonisamida Metformina Fendimetrazina Metilfenidato Dexanfetamina Lamotrigina
* Aprobadas por la FDA para la disminución del peso

342Consenso para la salud física del paciente
esquizofrénico Tratamiento antipsicótico como factor de riesgo
para la salud física— Aumento de peso y obesidad— Diabetes— Hiperlipidemia— Prolongación del intervalo QT— Hiperprolactinemia: irregularidades
menstruales, osteoporosis y disfunción sexual— Efectos extrapiramidales, acatisia y discinesia— Cataratas— Miocarditis— Sedación
Goff y cols., Schizophr Res 2005 Continúa

343Consenso para la salud física del paciente esquizofrénico
(cont.)
Diferencias entre los tratamientos
Aumento de peso Hiperlipidemia
Enfermedad cardiovascular
Resistencia a lainsulina
QTc
Trastornos sexuales
Discinesia
Efectosextrapiramidales
Segunda generación
Primera generación
Diabetes
Aumentode glucosa

344Efectos colateralesde los antipsicóticos atípicos:
cambio en la percepción del riesgo
Interés previo de seguridad
QTc
SEP
Efectos colateralesneurológicos:
Interés actual de seguridad
Síntomas extrapiramidal
es (SEP) + discinesia
tardía
QTcHiperlipidemia
Ganancia de peso
Resistencia a la
insulina
Resistencia a la
insulina
Ganancia de peso
ECVHiper-
glucemia
Hiper-glucemi
a
Diabetes
Enfermedad cardiovascular
(ECV)
Dislipidemia

345Determinantes de la efectividad del fármaco: adherencia al
tratamiento
Adherencia
Eficacia
Percepción del clínico
Percepción del paciente
Tolerabilidad

346Consenso ADA en antipsicóticos, obesidad y
diabetes
Diabetes Care 2004; 27: 596-601
FármacoGanancia de
pesoRiesgo de diabetes
Dislipidemia
Clozapina +++ + +
Olanzapina +++ + +
Risperidona ++ D D
Quetiapina ++ D D
Aripiprazol* +/- - -
Ziprasidona* +/- - -+: efecto aumentado; -: sin efecto, D: resultados discrepantes.*Fármacos más nuevos con datos limitados a largo plazo.

347
Comparación de pautas guía en esquizofrenia
Adaptado de Milner y Valenstein, 2002
Año
APA IPAP PORT TMAP ExCG
2004 2004 2003 2003 1999
Localización
www.psych.org/ psych_pract/treatg/pg/SchizP G-Complete-Feb04.pdf
www.ipap.org Lehman y cols., Schizophrenia Bulletin 30: 193-217
www.dshs.state. tx.us/mhprograms/timasczman.pdf
www.psychguides.com/scgl.pdf
Alcance de las recomendaciones
Psicofarmacología en psicosis agudas
Psicofarmacología de mantenimiento
Dosis recomendadas
Mejora cognitiva
Terapias psicosociales
Como complemento
Manejo de la comorbilidad médica
Como complemento
APA: American Psychiatric Association Practice Guideline for the Treatment of Patients with Schizophrenia – Second Edition;IPAP: International Psychopharmacology Algorithm Project – Schizophrenia Algorithm;PORT: The Schizophrenia Patient Outcomes Research Team Updated Treatment Recommendations;TMAP: Texas Medication Algorithm Project – Schizophrenia Algorithm;ECG: Expert Consensus Guidelines on the Treatment of Schizophrenia.

348
9. Evolución y pronóstico
Curso y pronóstico ...................................... 349-352
Factores que influyen en el pronóstico .......... 353-359
Principales estudios a largo plazo........................ 360
Evolución de la esquizofrenia....................... 361-362
Adherencia al tratamiento ............................ 363-364
Motivos de ingreso............................................. 365

349
Curso clínico en la esquizofrenia
La esquizofrenia es una enfermedad que cursa en forma de múltiples brotes (90%)
La repetición de los brotes agudos induce una pérdida progresiva de capacidades cognitivas, sociolaborales y funcionales, más acusada en los primeros 5 años
Los objetivos básicos son el tratamiento eficaz de los brotes, la rehabilitación funcional y la prevención de recaídas
Continúa

350
Curso clínico en la esquizofrenia (cont.)
Signos prodrómicos
Deterioro progresivo
Funcionamientopremórbido
Déficit
Brotes Funcionamiento normal
Estabilización

351
Curso y pronóstico
La esquizofrenia es una enfermedad de evolución crónica y discapacitante
Kraepelin revisa a la baja su porcentaje del 13% de recuperaciones al 4% después de separar las esquizofrenias de las «psicosis funcionales» y los trastornos bipolares
La vida media de los pacientes se acorta en 10 años con respecto a la población general
Estudios en pacientes con síntomas psicóticos un año antes del primer ingreso hospitalario muestran recaídas en los primeros 2 años en un 82%
Continúa

352
Curso y pronóstico (cont.)
En el conjunto de pacientes ingresados por un primer episodio psicótico en un hospital, un tercio no recaen en los primeros 2 años
Hasta un 20% evoluciona con síntomas crónicos y gran discapacidad
La sintomatología es más acusada los primeros 5 años de enfermedad
En el estudio piloto de esquizofrenia de la OMS los pacientes presentaron mejor evolución en países en desarrollo (India y Nigeria) que en países desarrollados

353Factores que afectan el curso delas esquizofrenias: el círculo
vicioso de la falta de tratamiento
Retraso en el tratamiento del primer episodio
Recuperación y abandono
del tratamiento
Recaída
Progresión y cronicidad de la enfermedad/resistencia
al tratamiento

354
Factores que contribuyen a la efectividad a largo plazo
Apoyo social/familiar
Eficacia del tratamiento en el mayor número de síntomas
Aceptación y
adherencia
Tolerabilidad del tratamiento
Efectividad
clínica

355
Factores que influyen en el pronóstico de la esquizofrenia
No Historia familiar de esquizofrenia
Sí NoComienzo brusco
con factor estresante
MayorEdad de inicio
Menor
Sexo*Mujeres Varones
Tiempo hasta elinicio del tratamiento
ProlongadoBreve
Impacto positivo
en el pronóstic
o
Impacto negativo
en el pronóstico
*El comienzo es más tardío y por lo general menos grave en mujeres. La comorbilidad con consumo de drogas en la esquizofrenia es mayor en varones.
Sí

356
Factores de buen pronóstico
Estrés psicosocial elevado asociado al inicio del brote psicótico
Pertenencia a una minoría étnica Antecedentes familiares de trastornos afectivos Predominio de síntomas positivos presentes
durante corto tiempo
Continúa

357
Factores de buen pronóstico (cont.)
Buen ajuste premórbido Inicio agudo de los síntomas Menor número de episodios psicóticos y menor
duración de éstos Adhesión al tratamiento farmacológico Ser mujer Estar casado (en varones) Baja emoción expresada en la familia Menor duración de los síntomas antes de
recibir tratamiento

358
Remisión sintomáticaen la esquizofrenia
«Remisión» se definió como un bajo nivel de síntomas que «no influyen en el comportamiento de los individuos»
Andreasen NC, Carpenter WT Jr, Kane JM, Lasser RA, Marder SR, Weinberger DR. Remission in schizophrenia: proposed criteria and rationale for consensus. Am J Psychiatry 2005; 162: 441-449

359
Remisión pragmáticaen la esquizofrenia
Cognitivamente afectados, socialmente aislados, desempleados y marginados
Remington G, Kapuer S. Letter to the Editor. Am J Psychiatry 162: 12

360
Principales estudios a largo plazo
Manfred Bleuler (1972, Suiza): 208 pacientes, 23 años de seguimiento; 66% recuperación o importante mejoría
Ciompi y Muller (1976, Suiza): 289 pacientes, 37 años de seguimiento; 27% recuperación, 22% ligeramente enfermos
Proyecto Vermont (1987, EE.UU.): 269 pacientes, entre 22 y 59 años de seguimiento; 34% recuperación, 34% importante mejoría

361
Evolución de las esquizofrenias
Años
Etapas de la enfermedad
SanoSignos y síntomas
Gestación/nacimiento
10 20 30 40 50
PremórbidoProdrómico Inicio/deterioro
Residual/estable
Pubertad
Lieberman y cols., 2001

362Tasa de respuestaal tratamiento según el período
de la psicosis sin tratar
Porcentaje acumulado de respuesta al tratamiento
Semanas en tratamiento
10090
8070
6050
403020
10
00 4 8 12 16 20 24 28 32 36 40 44 48 52 56 60
10 semanas 24 semanas 1 año 2 años
Lieberman y cols., 1996

363
Estudio CATIE El 74% de los pacientes interrumpieron o cambiaron su
tratamiento antes de los 18 meses, sobre todo por falta de eficacia, efectos secundarios y propia decisión del paciente
Olanzapina tuvo el porcentaje de abandono más bajo (64%) en comparación con quetiapina, risperidona, ziprasidona y perfenazina
El tiempo hasta el abandono del tratamiento debido a efectos secundarios fue similar en los distintos grupos; sin embargo:— La olanzapina se asoció a más abandonos debido a aumento
de peso y problemas relacionados con el metabolismo lipídico y aumento de glucemias
— La perfenazina se asoció a más abandonos relacionados con sintomatología extrapiramidal
El tratamiento de elección depende del equilibrio entre riesgos y beneficios en cada paciente concreto
Lieberman y cols., 2005

364
¿Por qué abandonan los pacientes el tratamiento?
Fleischhacker y cols., 2003
Factores que influyen en la adherencia
Factores relacionados
con el tratamiento:
Efectos secundarios
Vía de administraciónPeriodicidad en
las tomasDuración del tratamiento
CostePolifarmacia
Factores relacionados con
el ambiente:Apoyo social
Apoyo económicoActitud hacia el
tratamientoSupervisión del
tratamientoEstatus social
Recursos asistenciales disponibles
Factores relacionados con el paciente:
Insight Sintomatología
Problemas cognitivos Edad
Comorbilidad Sexo

365
Motivos de ingreso
Motivos de
ingreso
Síntomaspositivos
Problemasfamiliares
Riesgo de
suicidio
Violencia
DepresiónConsum
o de drogas
Diagnósticodiferencial
Problemassociales

366
10. Terapéuticas biológicas y psicológicas
Terapéuticas biológicas................................ 367-471
Terapéuticas psicológicas ............................. 472-505
Algoritmo de tratamiento ............................. 506-510

367
Terapéuticas biológicas
Tratamientos biológicos.....................................
368 Perfil de los antipsicóticos............................
369-383 Perfil de eficacia y tolerabilidad....................
384-424 Incumplimiento..........................................
425-429 Efectos secundarios....................................
430-450 Manejo......................................................
451-454 Metaanálisis de antipsicóticos......................
455-462 Medidas cautelares para el uso
de antipsicóticos en España................................
463 Antipsicóticos en ancianos...........................
464-465 Antipsicóticos en niños y adolescentes..........
466-471

368
Tratamientos biológicos
Históricos:— Choques de insulina (cura de Sakel)— Psicocirugía— Fármacos: reserpina, opiáceos, etc.
Actuales:— Fármacos: neurolépticos y nuevos
antipsicóticos— Otros (terapia electroconvulsiva,
estimulación magnética transcraneal, etc.)

369
Características de los antipsicóticos
Clásicos Nuevos (atípicos)
Bloqueo del receptor D2
Eficacia ante síntomas positivos
Efectos secundarios de tipo extrapiramidal (SEP)
Riesgo de discinesia tardía
Hiperprolactinemia
Bloqueo D2 y 5-HT2
Modulación del receptor D2
Eficacia ante síntomas positivos, negativos, cognitivos
y afectivos
Bajo perfil de efectos extrapiramidales (SEP)
Bajo riesgo de discinesia tardía
Ausencia de hiperprolactinemia

370
Antipsicóticos clásicos
Incisivos— Haloperidol— Zuclopentixol— Trifluoperazina— Perfenazina— Pimozida
Atípicos— Sulpirida— Loxapina
Sedativos— Clorpromazina— Levomepromazin
a— Clotiapina— Tioridazina
Depot— Flufenazina— Zuclopentixol— Pipotiazina

371
Nuevos antipsicóticos (atípicos)
Bloqueo D2 y 5-HT2
— Clozapina— Olanzapina— Quetiapina— Risperidona— Ziprasidona
Modulación dopaminérgica— Amisulprida— Aripiprazol
Depot— Risperidona

372
Perfil del antipsicótico ideal
Detección precoz Control de síntomas Prevención de recaídas
Rehabilitación
Eficacia en todo tipo de síntomas Prevención de recaídas y suicidio Buena tolerancia. Sin toxicidad Facilidad de administración (i.m., depot, etc.) Facilita la rehabilitación funcional Bien aceptado por el paciente

373
Amisulprida
Aripiprazol
Clozapina Olanzapina QuetiapinaRisperidon
aSertindol
Ziprasidona
Eficacia frente a síntomas negativos
Alta ? Alta Media Media Media Media/alta Media
Eficacia frente a síntomas cognitivos
? Memoria verbal 2.a
Ejecución motora;
aprendizaje verbal
Velocidad de proceso/ atención; ejecución general,
organización perceptiva
Atención, memoria, ejecución motora, función
ejecutiva
Aprendizaje verbal
declarativo, habilidades de memoria visuomotor
a
Tiempo de reacción
Atención, memoria, ejecución motora, función
ejecutiva (?)
Riesgo de suicidio
? ? Reducido Reducido ? ? Reducido ?
Síntomas extrapiramidales
Relacionado con dosis
Sin indicios
Sin indicios Casi sin indicios con
dosis
Sin indicios
Sedación Leve Leve Fuerte Moderada Moderada Leve Sin efecto Leve
Peso Poco Poco/sin* Fuerte Fuerte Alguno Alguno Alguno Poco/sin
Efectos metabólicos
? ? Riesgo de diabetes
Riesgo de diabetes
Riesgo de diabetes
Riesgo de diabetes
Sin evidencia clínica*
Sin evidencia clínica*
Otros efectos colaterales
? - Actividad anticolinérgic
a agranulocitosis, salivación
Actividad anticolinérgi
ca media
Actividad anticolinérgi
ca leve
Prolactina Prolonga QTc,
volumen eyaculator
io
Prolonga QTc, prolactina
(?)
*Datos limitados.
Comparación de perfilesde seguridad y eficacia
de antipsicóticos atípicos

374
Perfil de eficacia de antipsicóticos atípicos
Amisulprida
Clozapina Olanzapina
QuetiapinaRisperidon
a <6 mg/día
Sertindol Ziprasidona
Zotepina
Signos positivos
+++ +++ +++ +++ +++ +++ +++ +++
Signos secundarios negativos
+++ +++ ++ ++ ++ ++ ++ ++
Signos primarios negativos o déficit
++ +
Ansiedad ND ++ + ++ +
Depresión ++ ++ ++ + +
Blin, 1999

375
Fármaco SEPAntimuscarínic
os PLT
PesoConvulsione
sSedació
nHipotensión postural
Prolonga QTc
Dislipidemia
Tioridazina + +++ ++ ++ + + ++ +++ ++
Haloperidol+++
++++
+ + + + + +
Amisulprida
+ -+++
+ + + + + ?
Aripiprazol + - - + - + + -
Clozapina - +++ - +++ +++ +++ +++ + +++
Olanzapina + + + +++ + ++ + + +++
Quetiapina - + - ++ + ++ ++ + ++
Risperidona
++ -+++
++ + + ++ + -
Ziprasidona
+ - + - + + + ++ -
Zotepina + - ++ ++ ++ ++ + + ?
SEP: síntomas extrapiramidales. riesgo: - mínimo, + pequeño, ++ moderado, +++ alto, ? no claro.
Riesgo comparativo de efectos adversos de los antipsicóticos
Haddad y Sharma. CNS Drugs 2007; 21: 911-936
Comparadores: haloperidol y tioridazina

376
Perfil de efectos secundarios de antipsicóticos atípicos
Efectos secundarios extrapiramidales Efectos
secundarios vegetativosDosis bajas Dosis elevadas
Amisulprida — + ++
Clozapina + + +++
Olanzapina + + +++
Quetiapina + + ++
Risperidona + ++ ++
Sertindol — — ++
Ziprasidona + + ++
Zotepina + ++ ++

377
Afinidad a subtipos receptoriales
Constantes de afinidad de varios antipsicóticos para receptores de los sistemas de neurotransmisión clásicosFármaco D1 D2 D3 1 2 H1 5-HT2 1C 5-HT2 M1
Quetiapina
Olanzapina
Clozapina
Risperidona
Remoxeprida
Amisulprida
Haloperidol
1.243
31 ± 0,7
85 ± 0,7
75 ± 8
>10.000
>1.000
25 ± 7
329
11 ± 2
126 ± 20
3 ± 0,1
274 ± 179
2,8
1 ± 0,04
89
3,2
2,3
90
19 ± 1
7 ± 4
2 ± 0,1
27.870
46 ± 6
270
228 ± 40
8 ± 3
3 ± 0,7
2.904
360 ± 98
30
7 ± 0,3
7 ± 0,3
155 ± 35
>10.000
3.630
23 ± 3
23 ± 3
60
>10.000
148
5 ± 0,7
5 ± 0,7
0,6 ± 0,4
>10.000
>10.000
1,9 ± 0,2
1,9 ± 0,2
>3.000
>3.000
1.475
Moorey y cols., 1993; Schoemaker y cols., 1996

378
Perfil de unión a receptores de los antipsicóticos
Receptor Amisulprida
Aripiprazol
Clozapina Haloperidol
Olanzapina
Risperidona
Ziprasidona
Familia D1D1
— + + ++ —
D5 — + + ND ND
Familia D2D2
++ + +++ ++ +++
D3 +++ + ++ ND ++
D4 — ++ ++ ++ ++
5-HT1A — — — — +
5-HT1D — — — — ++
5-HT2A — +++ ++ +++ +++
5-HT2C — ++ — ++ +++
5-HT3 — + — + —
5-HT4 — — — ND ND
1 — +++ +++ ++ +++
2 — ++ — — +++
H1 — +++ — +++ +++
Muscarínico — ++ — ++ —
Sigma — — +++ ND +

379Afinidad de los antipsicóticos
por el receptor D2
100
10
1
0,1
Quetiapina
Clozapina
OlanzapinaZiprasidonaAmisulpridaRisperidonaClorpromazinaHaloperidol
Dopamina K (1,5 nM)

380
Disociación del receptor D2
QuetiapinaClozapinaRemoxipridaAmisulprida
Olanzapina Haloperidol
Antipsicóticos atípicos Antipsicóticos clásicos
RÁPIDA MEDIA LENTA
Sertindol Racloprida Clorpromazina
01 2 4 6 8 10
20
30
Minutos para la liberación del 50% del antipsicótico del D2

381
Perfil de afinidad receptorial de los antipsicóticos
D1D25-HT2A
5-HT1A
1
2
H1
Quetiapina
D1 D2
5-HT2A
5-HT1A
2
H1
M
Clozapina
1
D1 D2
5-HT2A
1
H1
M
Olanzapina
D2
5-HT2A
1
2H1
Risperidona D1
D2/D3
Amisulprida
D1
D2
5-HT1A
A1
HaloperidolH1
Golletein, 1999

382
Bases racionales del tratamiento
Locus niger
Área tegmental ventral
Estriado: caudado, putamen y globus pallidus
Corteza frontal
Núcleo accumbens

383
Vías dopaminérgicas y efectos clínicos de su bloqueo
Mesolímbica (A-10): su bloqueo disminuye los síntomas positivos y la hiperdopaminergia del núcleo accumbens
Mesocortical: existe una hipodopaminergia que puede mejorar con algunos de los nuevos antipsicóticos; está asociada al déficit cognitivo
Nigroestriada: el bloqueo produce síntomas extrapiramidales, acatisia y parkinsonismo
Tuberoinfundibular: el bloqueo libera la secreción de prolactina

384Efecto de los nuevos antipsicóticos
y perfil de eficacia-tolerabilidad Selectividad mesolímbica (A-10)
— Menor nivel de efectos extrapiramidales/discinesia tardía
Bloqueo de antagonistas NMDA— Mejoría de la psicosis, la cognición y los
síntomas negativos Bloqueo del receptor 5-HT2
— Mejora la tolerancia del bloqueo D2
— Mejora la función cognitiva Incremento de la expresión c-fos en la corteza
prefrontal— Mejoría de la cognición y los síntomas
afectivosMaguire, APA 2002

385
La ocupación de receptores D2 predice la respuesta clínica
Kapur y cols., Am J Psychiatry 2000
Porcentaje de ocupación de receptores D2
p = 0,07 en síntomas positivos del PANNS
Porc
en
taje
de r
esp
on
dedore
s IC
G (
p <
0,0
01
)
Respuesta Ausencia de respuesta
010203040
60708090
100
< 65 > 65
50

386
La ocupación de receptores D2
del estriado predice acatisia/SEP
Kapur y cols., Am J Psychiatry 2000
0
10
20
30
40
50
60
70
80
90
Sujetos individuales
78%
Sujetos con acatisia/SEP
%
SEP: síntomas extrapiramidales

387Risperidona: ocupación
de receptores D2
0102030405060708090
100
0 2 4 6 8 10 12
Dosis (mg/día)
Respuesta clínica
SEP-acatisia
%
Kapur y cols., Am J Psychiatry 1999
Ocupación de receptores D2

388Olanzapina: ocupación
de receptores D2
Kapur y cols., Am J Psychiatry 1999
0102030405060708090
0 5 10 15 20 25 30 35 40
Respuesta clínica
SEP-acatisia
%
Dosis (mg/día)
Ocupación de receptores D2

389
0
10
20
30
40
50
60
70
0 100 200 300 400 500 600 700 800
Clozapina: ocupación de receptores D2
Respuesta clínica
SEP-acatisia
%
Dosis (mg/día)
Nunca cruza el límite de los SEP
Kapur y cols., Am J Psychiatry 1999
Ocupación de receptores D2

390
0
5
10
15
20
25
0 150 300 450 600 750
Quetiapina: ocupación de receptores D2. Estriado: sin
SEP
Respuesta clínica
%
Dosis (mg/día)
Nunca cruza el límite de los SEP
Kapur y cols., Am J Psychiatry 1999
Ocupación de receptores D2

391Quetiapina: ocupación de receptores D2 en el sistema
límbico (accumbens)
20
57
0
10
20
30
40
50
60
3 h 9 h
%
400 mg 450 mg
2 h
24 h
0
6470
10
20
60
30
40
50
0

392Características de algunos antipsicóticos: selectividad
límbica
Reversión del efecto anfetamínico a dosis más bajas en la vía A-10 que en la A-9
Tras dosis crónicas, selectividad en la inhibición de la vía dopaminérgica A-10
Incremento selectivo en la expresión c-fos en áreas límbicas, pero no motoras
Ausencia de SEP
Goldstein y cols., 1993; Vahid-Ansari y cols., 1996

393Características de algunosnuevos antipsicóticos:
modulación dopaminérgica
La amisulprida a dosis bajas tiene un efecto prodopaminérgico en la corteza frontal, lo que la hace también eficaz en síntomas negativos y en alteraciones cognitivas
El aripiprazol tiene efectos sobre el receptor D2, como agonista parcial competitivo: en situaciones hipodopaminérgicas es activador (corteza frontal) y en situaciones de hiperdopaminergia es inhibidor (sistema límbico)

394
Características de algunos nuevos antipsicóticos: dosis
Con amisulprida, dado su mecanismo de acción y su escasa incidencia de SEP a las diferentes dosis recomendadas, se recomienda iniciar el tratamiento a dosis plena. En fase aguda debe iniciarse el tratamiento con 800 mg/día, pudiendo incrementarse hasta un máximo de 1.200 mg/día. En fase de mantenimiento, debe ajustarse la dosis en función de la sintomatología predominante, recomendándose un rango de 600 a 400 mg/día en pacientes con predominio de sintomatología positiva y un rango de 300 a 100 mg/día en aquellos con predominio de sintomatología negativa
Continúa

395
Características de algunos nuevos antipsicóticos: dosis (cont.)
Con olanzapina, en cuanto a dosis, «más es más»; la buena tolerancia permite dosis de hasta 20-30 mg/día y se obtiene una eficacia mayor con escaso riesgo de SEP
Con quetiapina, dada la ausencia de SEP, tiene sentido aumentar la dosis por encima de las habituales (400-800 mg/día) para un bloqueo D2 suficiente
Con risperidona «menos es más», y ofrece su mejor perfil a dosis en torno a los 4 mg

396
Dosis ideal y perfil de ocupación
El margen de dosis ideal permite un bloqueo D2 superior al 65% (asociado con eficacia clínica) e inferior al 78% (asociado con efectos extrapiramidales)
Algunos nuevos antipsicóticos no alcanzan la cifra del 65% salvo transitoriamente por una constante de disociación (k-off ) rápida (quetiapina, clozapina)

397
Hipótesis dopaminérgica de la esquizofrenia
Psicosis aguda:
Síntomas +agitación
Agudo Crónico
Efectos antipsicóticos clásicos: • SEP-acatisia • Discinesia tardía
Up-regulation
Recaída por
up-regulation
• Aumento de dosis
• Más SEP, etc.

398
Efectos de los nuevos antipsicóticos
Psicosis aguda:
Control de síntomas +agitación
Efecto crónico:
• Sin up-regulation
• Sin SEP-acatisia
• Sin discinesia tardía
Nuevos antipsicóticos: activan la liberación dopaminérgica por efecto bloqueante 5-HT2A: eficacia en síntomas negativos y cognitivos
Déficit dopaminérgico en la corteza frontal:síntomas negativos

399
Constante de disociación (K-off )
0
20
40
60
80
100
120
0 15 30 45 60 75 90
50% de disociación en menos de 90 seg
50% de disociación en más de 80 min
Tiempo (seg)
Kapur y cols., J Psych Neurosci 2000
%

400
Una K-off rápida predice atipicidad
Los diferentes antipsicóticos tienen una K-on similar (igual o superior al 60% Eficacia en síntomas positivos)
Las diferencias en clínica vienen dadas por sus diferencias en K-off: Eficacia en síntomas negativos— Antipsicóticos más «pegajosos»: clásicos— Antipsicóticos más «volátiles»: atípicos
Los atípicos tienen una disociación más rápida y menor afinidad que los clásicos:clozapina-quetiapina-amisulprida >> olanzapina > risperidona > haloperidol

401
Afinidad por el receptor D2
K p
ara
D2 (
nM
)
Alta para D2
Clorpromazina
Flufenazina
Perfenazina
Tiotixeno-cis
A0,01
0,1
1
10
100
Melperona
Perlapina
Quetiapina
RemoxipridaClozapina
Amoxapina
Sulpirida
Loxapina
Iloperidona
MolindonaOlanzapina
ZiprasidonaSertindolAmisulprida
Moperona, raclopridatrifluoperazina, pimozida
Risperidona
Clorprotixeno
HaloperidolFlupentixol-cis
Droperidol
Butaclamol-(+)
Tiotixeno-cis
Butaclamol-(+)
Nemonaprida

402Actividad intrínseca
en los receptores D2
La eficacia intrínseca describe la habilidad de un compuesto para activar los receptores
Plena activación
Sin activación
Activación parcial
Receptor D2
Agonista completo (dopamina)
Antagonista (haloperidol, risperidona, etc.)
Antagonista intermitente:(quetiapina, olanzapina, clozapina, amisulprida a dosis elevadas, etc.)
Agonista parcial (amisulprida a dosis bajas, aripiprazol)
Bloqueo parcial

403Afinidad relativa por los receptores D2 y 5-HT2*
Baja Intermedia Alta
Baja
AltaClozapinaQuetiapina
OlanzapinaRisperidona
SertindolZiprasidona
HaloperidolAmisulpridaFlupentixol
Risperidona(dosis elevadas)
5-HT2A
*En relación con las dosis clínicas habituales
Kasper y cols., 1999
D2

404
Amisulprida: perfil farmacológico
Perfil farmacológico Consecuencia clínica
Selectivo para receptores D2 y D3 Eficacia en síntomas positivos, negativos, cognitivos y afectivosSin efectos vegetativos, anticolinérgicos o vascularesMenor incremento de peso
Selectividad límbica Buena tolerancia sin acción en el nigroestriado (menor incidencia de SEP)
Antagonista D2 postsináptico Eficacia en síntomas positivos y (400 a 1.200 mg) negativos (incluidos primarios)
Antagonista D2/D3 presináptico Eficacia en síntomas negativos en el sistema mesocortical (incluidos primarios)(100 a 300 mg)

405
Amisulprida: resumen sobre eficacia
Episodio agudo
Amisulprida = haloperidolAmisulprida = risperidonaAmisulprida = olanzapina
Amisulprida > haloperidolAmisulprida = risperidonaAmisulprida = olanzapina
Amisulprida > haloperidolAmisulprida = risperidona
PANSS positivo PANSS negativo BPRSICG
6 meses
Amisulprida = risperidona Amisulprida > risperidona
PANSS positivo-PANSS negativo-BPRS-SANS
SOFAS-Respuesta subjetiva positiva
12 meses
Amisulprida > haloperidol
PANSS negativo-BPRS-QSL-GAF
Síntomas negativos primarios
Amisulprida > placebo
SANS
Amisulprida = olanzapina

406
Amisulprida: resumen sobre tolerabilidad
Síntomas extrapiramidales
Simpson-Angus SAS
Efectos endocrinos
Amisulprida = haloperidol
Incremento de peso
Amisulprida < haloperidol < risperidona < quetiapina < clorpromazina < olanzapina < clozapina
Amisulprida = risperidona
Amisulprida = olanzapina
Amisulprida > haloperidol
Haloperidol < risperidona

407Amisulprida: eficacia en episodios agudos frente a
risperidona
Peuskens y cols., 1999
PANSS positivo
5248
0
10
20
30
40
50
60
Amisulprida800 mg
(n = 115)
Risperidona8 mg
(n = 113)
Red
ucci
ón e
n la
su
besc
ala
PA
NS
S (
%)
PANSS negativo
39
31
0
10
20
30
40
Amisulprida800 mg
(n = 115)
Risperidona8 mg
(n = 113)
Red
ucci
ón e
n la
su
besc
ala
PA
NS
S (
%)
p = 0,09

408Amisulprida: eficacia en episodios agudos frente a
olanzapina
Martin y cols., 2002
Amisulprida Olanzapina
Subescala BPRS
6,9
3,43
6,1
1,5
3,6
6,2
3,12,9
5,6
1,4
3,5
0
2
4
6
8
Ansie
dad,
depr
esión
Anerg
i
aTr
asto
rno
del
pens
amie
nt
oAct
ivac
ión
Hostil
idad
Psicos
is
Cam
bio
medio
D0
-D2
mese
s

409Amisulprida: eficaciaen episodios agudos.
Mejora de síntomas depresivos
Peuskens y cols., 2002
Estas diferencias significativas (p = 0,01) a favor de amisulprida se manifiestan ya a las 2 semanas de
tratamiento
Subescala depresión/ansiedad BPRS
5,6 + 6,14,4 + 5,5
1
2
3
4
5
6
Amisulprida400 a 800 mg
(n = 339)
Haloperidol15 a 20 mg(n = 160)
Reducc
ión m
edia
en la s
ubesc
ala
BPR
S
Risperidona8 mg
(n = 113)
3,7 + 4,7
0

410Amisulprida: seguridad en fase aguda. Síntomas
extrapiramidales
Peuskens y cols., 1999 Martin y cols., 2002
Escala de Simpson-Angus
–0,1
–0,05
0
0,05
0,1
Amisulprida800 mg
(n = 114)
Risperidona6 mg
(n = 113)
NS
0,01–0,01
Cam
bio
med
io D
máx-D
0
–0,1
–0,05
0
0,05
0,1
Amisulprida200-800 mg
(n = 189)
Olanzapina5-20 mg(n = 188)
NS
–0,03 –0,007
Cam
bio
med
io D
máx-
D0

411Amisulprida: seguridad en fase aguda. Efectos
endocrinos
*Una alteración endocrina por lo menos
Coulovrat, 1999
Amisulpridan = 579
Haloperidoln = 214
Risperidonan = 113
0
4%
1%*
5
10Porc
enta
je d
e e
nfe
rmos
NS
6%p < 0,05

412
Control metabólico en pacientes con esquizofrenia
Cambio de medio de peso corporal a lo largo del período de tratamiento de 6 meses. Los dos grupos de tratamiento presentaban una diferencia significativa (p = 0,0004: análisis de covarianza).
Peuskens J y cols. Int Clin Psychopharmacol 2007; 22: 145-152
Visita del estudio (días)
8
6A
um
en
to d
e p
eso
(kg)
14 28 42 56 90 120 150 1800
1
2
3
4
5
Grupo de olanzapina
Grupo de amisulprida

413Cambios tempranos en la lipidemia durante el tratamiento
con antipsicóticos atípicos
Estudio prospectivo, abierto, en 35 pacientes con esquizofrenia (CIE-10) bajo tratamiento con:— Amisulprida (n = 12)— Ziprasidona (n = 6)— Clozapina (n = 8)— Olanzapina (n = 9)
Comparación de peso corporal y lípidos séricos a las 4 semanas
IMC, colesterol total y triglicéridos y HDL en pacientes tratados con clozapina y olanzapina
Amisulprida y ziprasidona: perfil más favorable respecto a la ganancia de peso y la hiperlipidemia
Rettenbacher MA, Ebenbichler C, Hofer A y cols. Early changes of plasma lipids during treatment with atypical antipsychotics. Int Clin Psychopharmacol 2006; 21: 369-372

414Alteraciones del metabolismode glucosa con clozapina
o amisulprida
Estudio prospectivo, abierto, en pacientes con esquizofrenia, en tratamiento con— Amisulprida (n = 12)— Clozapina (n = 10)
Evaluación mensual de peso corporal y resistencia a insulina, durante 12-16 semanas
IMC, niveles séricos de insulina en ayunas y HOMA IR (Homeostasis Model Assessment for Insulin Resistence) en pacientes tratados con clozapina
Ninguno de los parámetros se incrementó significativamente en los pacientes tratados con amisulprida
Rettenbacher MA, Ebenbichler C, Hofer A y cols. Early changes of plasma lipids during treatment with atypical antipsychotics. Int Clin Psychopharmacol 2006; 21: 369-372

415Alteraciones del metabolismode glucosa con clozapina
o amisulprida
Rettenbacher MA, Ebenbichler C, Hofer A y cols. Early changes of plasma lipids during treatment with atypical antipsychotics. Int Clin Psychopharmacol 2006; 21: 369-372
HOMA IR basal
HO
MA
IR
sem
ana 1
2-1
6
Amisulprida
Clozapina
5040
30
20
10
543
2
1
503020105321 404

416
Incremento de peso
Incremento de peso (kg) en 10 semanas:metaanálisis de todos los estudios
0,82
1,08
2,12
2,16
2,58
4,15
4,45
0 0,5 1 1,5 2 2,5 3 3,5 4 4,5
Clozapina
Olanzapina
Clorpromazina
Quetiapina
Risperidona
Haloperidol
Amisulprida
Allison y cols., 1999; Taylor, 2000; Müller-Spahn, 2001

417
Tasa de abandonos
Leutch y cols., 2002
22
30
4346
0
10
20
30
40
50
Amisulprida Risperidona Olanzapina Quetiapina
Paci
ente
s qu
e a
bandonan
el tr
ata
mie
nto
(%
)

418
Amisulprida permite iniciarel tratamiento a dosis plena
Fase aguda
Fase de mantenimiento
Paciente no tratado
Cambio de tratamiento
800 mg/díaen dos tomas
(Hasta 1.200 mg/día)
Con síntomas positivos
Con síntomas negativos
600-400 mg/díaen dos tomas
300-100 mg/díaen una toma
Neuropsychobiology 2001; 44: 41-46

419
Amisulprida no necesita fase de titulación
Retirar el tratamiento previo progresivamente
(1-4 semanas)
Iniciar el tratamiento con amisulprida a
dosis plena(800 mg/día en fase aguda)
+
Tiempo
Inicio de amisulprida Fin del tratamiento previo1 a 4 semanas
Neuropsychobiology 2001; 44: 41-46

420
100 nM dopamina+ haloperidol
100 nM dopamina+ aripiprazol
El aripiprazol es un agonista parcial en los receptores hD2L
Células D2L de ovario de hámster chino expuestas a 10 µM de EEDQ.Datos de Bristol-Myers Squibb Co., y Otsuka Pharmaceutical Co., Ltd.
Fármaco
Porc
enta
je m
áxim
o
de r
esp
uest
a d
opam
inérg
ica
10-10 10-9 10-8 10-7 10-6 10-5
0
50
100
Dopamina
Aripiprazol
Haloperidol

421
Aripiprazol: farmacodinámica Agonista parcial de los receptores D2
— En la esquizofrenia la actividad dopaminérgica varía en diferentes áreas del cerebro: existe hiperactividad en regiones mesolímbicas (síntomas positivos) e hipoactividad en regiones corticofrontales (síntomas negativos y cognitivos)
— El aripiprazol actúa como antagonista funcional en condiciones de hiperdopaminergia y como agonista parcial en zonas hipodopaminérgicas
Agonista parcial de los receptores 5-HT1A
Antagonista de los receptores 5-HT2A
Efecto global de estabilización del sistema dopamina-serotonina

422
Aripiprazol: farmacocinética
Biodisponibilidad = 87% Semivida de eliminación (T1/2) ~ 72 h La dosis proporcional a la Cmáx y el área bajo la
curva (AUC) se sitúa entre 5 y 30 mg/día
Es metabolizado por más de un citocromo del sistema P450, por lo que su potencial de interacciones parece bajo
No requiere ajuste de la dosis en caso de insuficiencia renal o hepática

423Actividad relativade varios antipsicóticosen los receptores 5-HT1A
0
20
40
60
80
100
120
5-HT Ziprasidona Buspirona Aripiprazol Clozapina Risperidona
Máx
imo
efec
to e
stim
ulan
te

424Farmacogenética.
Genes y alelos asociados con respuesta
a antipsicóticos
Gutiérrez y cols., 2000; Collier y cols., 2002
Fármaco Gen PolimorfismoAlelo asociado a mala respuesta
Consecuencias clínicas
Clozapina 5-HT2A
5-HT2c
T102C
His452TyrA-1438G
Cys23Ser
C102
Tyr452G-1438
Cys23
No funcional. En desequilibrio de
ligamiento con A-1438G
?
¿Alteración en la expresión génica?
?
Clorpromazina
D4 VNTR (48bp) Alelo 2 rep ¿Alteración del mecanismo de
unión del fármaco al receptor?

425
El problema del incumplimiento
La necesidad de hospitalización se duplica en los pacientes que no siguen correctamente el tratamiento (Curson, 1985)
El 74% de los pacientes abandonan el tratamiento en 2 años (Weiden, 1991)
El abandono de los antipsicóticos es la mayor causa de recaídas e induce un riesgo seguro de reagudización y un deterioro en el funcionamiento social (Johnson, 1983)

426Consecuencias de la interrupción de los
antipsicóticos
Mayor gravedad clínica (Curson, 1985) Mayor duración del período de recuperación
(Loebel, 1995) Mayor índice de refractariedad (Loebel, 1995) Mayor riesgo de suicidio (Cohen, 1964) Más conductas violentas (Virkunen, 1974;
Tanay, 1987) Peor pronóstico a largo plazo (Wyatt, 1995)

427
Predictores de abandono de antipsicóticos
0 2 4 6 8 10
Función ejecutiva
Depresión
Educación
Enfermedad de Parkinson
Clase social
Robinson, Arch Gen Psychiatry 1999; 56: 241
Hillside Hospital First Episode Study

428
Tasas de recaída por dejar los antipsicóticos
Ayuso Gutiérrez, 1999
Autor n Meses Recaída (%)
Hogarty, 1976
Johnson, 1976
Denker, 1980
Cheung, 1981
Johnson, 1979
Wisted, 1981
Adejide, 1982
41
23
32
30
60
14
70
12
6
24
18
18
12
12
65
53
94
62
80
100
56
Total 270 73

429Los nuevos antipsicóticos mejoran el cumplimiento del
tratamiento
*p = 0,001 frente a risperidona **p = 0,022 frente a haloperidol
*
**
Porcentaje de pacientes según el grado de cumplimiento (6 meses)
Gómez y cols., J Clin Psychiatry 2000
Alto: ≥80% Moderado: 60-79% Bajo: 20-59% Nulo: <20%
84,8 74,2 69,8
11,119,4 27,1
100
0
20
40
60
80
Paci
ente
s (%
)

430
Efectos secundarios posibles
SNC:— Sedación-agitación— Extrapiramidales:
temblor, distonías, acatisia, parkinsonismo
— Discinesia tardía— Convulsiones— Síndrome
neuroléptico maligno Anticolinérgicos:
— Sequedad de mucosas
— Estreñimiento, retención de orina
— Vista borrosa
Cardiovascular:— Hipotensión
ortostática— Alteraciones en el ECG— Aumento del intervalo
QT— Fibrilación ventricular
Endocrino:— Hiperprolactinemia— Amenorrea-impotencia— Galactorrea,
ginecomastia— Aumento de peso— Resistencia a la
insulina
Continúa

431
Efectos secundarios posibles (cont.)
Hematológicos:— Leucopenia— Agranulocitosis
Dermatológicos:— Fotosensibilidad— Alergias
Oftálmicos:— Retinopatía
pigmentaria— ¿Cataratas?
Hepáticos:— Elevación de las
transaminasas— Hepatitis
colestásica Otros:
— Enlentecimiento motor
— Afectación cognitiva
— Alteración de la conciencia
— Disminución de la expresividad emocional

432
Contraindicaciones (relativas)
Enfermedad de Parkinson
Arteriosclerosis Alteración del
intervalo QT Epilepsia Insuficiencia hepática Insuficiencia renal
Hemiplejía Glaucoma de ángulo
agudo Tumor cerebral Hipertrofia
prostática Gestación Alteraciones
hematológicas

433Criterios diagnósticos del síndrome neuroléptico
maligno Tratamiento con neurolépticos en los 7 días
previos Hipertermia (≥ 38 ºC) Rigidez muscular Cinco de los siguientes:
— Alteración de la conciencia
— Taquicardia— Alteración de la presión— Taquipnea-hipoxia — Hipoxia
Exclusión de otras causas
— Sudor o sialorrea — Temblor— Incontinencia— CPK-mioglobinuria— Leucocitosis— Acidosis metabólica
(enfermedades o drogas)

434Bajo riesgo de efectos
secundarios extrapiramidales: ventajas de los antipsicóticos
atípicos
Menos riesgo dediscinesia tardía
Menos efectos motores-estigma
Menos disforia
Mejoría cognitiva
Menos síntomas negativos
secundarios
Mejoradherencia
Jibson y Tandon, 1998
Ventajas de laausencia de SEP

435
Tratamiento de los síntomas extrapiramidales
Hipertonía, rigidez, parkinsonismo:— Anticolinérgicos— Benzodiazepinas.
.. Temblor:
— Anticolinérgicos— -bloqueantes
Discinesia tardía:— Vitamina E,
melatonina— Muy resistente
Acatisia:— -bloqueantes— Benzodiazepinas— Anticolinérgicos— Antidepresivos— Reducir las dosis...
Mejor:— Usar
antipsicóticos con bajo perfil de SEP

436Los síntomas extrapiramidales están relacionados con la
dosisC
am
bio
med
io m
áxim
o
en
el E
SR
S
Risperidona*p < 0,05 frente a 1 o 4 mg/día de risperidona†p < 0,05 frente a 1, 4, 8 o 12 mg/día de risperidona
Owens, 1994; Peuskens, 1995
*
*
††
Dosis crecientes de risperidona
1 mg(n = 229)
4 mg(n = 227)
8 mg(n = 230)
12 mg(n = 226)
16 mg(n = 224)
10 mg(n = 226)
3
2
1
0Haloperidol
Haloperidol

437
Consecuencias potenciales de la elevación de prolactina
Amenorrea
GalactorreaAumento del pecho
Impotencia
Ginecomastia
Disfunciónsexual
Osteoporosis
Elevación deprolactina

438
Efecto de los antipsicóticos en el QTc
Funck-Brentano y Jaillon, 1993Pfizer Study 54, FDA Psychopharmacological Drug Advisory Committee 19th, July 2000
30,1
35,6
30,8
29,6
28,7
28,5
28,1
7,1
4,7
6,8
7,3
7,4
6,1
6,3
5,7
14,5
6,9
4,8
7,5
4,4
3,8
1,7
6,8
2,3
1,1
2,5
1,6
1,2
3,6
9,1
4,3
3,0
3,3
3,7
3,3
15,9
20,3
16,5
15,5
14,9
14,9
14,6
Corrección al inicio
Corrección de Bazett*
Corrección de la FDA
Corrección de Fridericia
Corrección de Hodges
Corrección Framingham
Corrección lineal
Tiorida-zina
Halo-peridol
Quetia-pina
Olanza-pina
Risperi-dona
Ziprasi-dona
Cambio en el QTc desde la línea de base (mseg)
*El método de Bazett se considera poco exacto.

439
Qtc: variación media en un estudio comparativo
Milisegundos entre situación basal y equilibrio
0 5 10 15 20 25 30 35 40
Tioridazina
Ziprasidona
Quetiapina
Risperidona
Olanzapina
Bazett (1) Fridericia (2)
1. Briefing Document for Ziprasidone Capsules, FDA Psychopharmacological Drugs Committee,
19 de julio de 2000 2. Pfizer Inc. Study Report of Ziprasidone Clinical Pharmacology Protocol. Rockville, Md. FDA
Center for Drug Evaluation and Research Division of Cardiorenal Drug Products Consultation, 14 de junio de 2000

440Interacciones de los antipsicóticos. Precauciones
según la ficha técnica Aripiprazol
— Precaución con el uso asociado de:• Inhibidores (CYP2D6): antiarrítmicos Ia, quinidina, paroxetina,
fluoxetina, etc.• Inhibidores (CYP3A4): azoles, macrólidos, inhidores de la
proteasa, antagonistas del calcio, fluoxetina, fluvoxamina• Inductores: fenobarbital, fenitonía, rifampicina, efavirenz,
nevirapina, primidona, etc. Olanzapina
— Precaución con el uso asociado de:• Inductores: carbamazepina• Inhibidores (CYP1A2): tabaco, fluvoxamina, ciprofloxacino
Quetiapina— Evitar el uso asociado de:
• Inhibidores (CYP3A4): azoles, macrólidos, inhidores de la proteasa, antagonistas del calcio, fluoxetina, fluvoxamina
— Precaución (riesgo de ineficacia) con:• Inductores (CYP3A4): carbamazepina, fenitoína, rifampicina
Risperidona— Precaución con el uso asociado de:
• Inhibidores (CYP2D6): antiarrítmicos Ia, quinidina, paroxetina, fluoxetina, fenotiazinas, etc.
• Inductores: fenobarbital, fenitonía, rifampicina

441
Interacciones de los antipsicóticos
Haloperidol
Amisulprida
Aripiprazol
Clozapina
Olanzapina
Quetiapina
Risperidona
Ziprasidona
Antiparkinsonianos
+ + + + + + + +
En la distribución - - - + - - - -
CYP1A2 + - - + + - - -
CYP2D6 + - + + + - + -
CYP3A4 + - + + - ++ + -
Benzodiazepinas - - - + - - - -
Depresores de la médula ósea
- - - ++ - - - -
Depresores del SNC
+ + + + + + + +
Litio + + + + + + + +
Prolongación del QTc
+ + + + + + + +
Antihipertensivos + + + + + + + +
Adrenérgicos + - - + - - + -
Antihistamínicos - - - + + + - -
Anticolinérgicos - - - + + - - -

442
Otros efectos tóxicos y secundarios
Toxicidad hemática: clozapina Incremento de peso: clozapina, olanzapina,
tioridazina Incremento de la prolactina: risperidona,
amisulprida, haloperidol Congestión nasal: tioridazina, sertindol Hipotensión: tioridazina, quetiapina

443El estigma puede ser debido a efectos secundarios
neurolépticos
Los signos más evidentes de la enfermedad pueden deberse a los efectos secundarios de
la medicación neuroléptica
Estigma
Alteración de la funcionalidad

444
Efectos secundarios cognitivos
Disminución de las posibilidades de empleo Disminución del desarrollo social/laboral
Disminución de la capacidad de aprendizaje/estudio
Dificultades para leer y memorizar

445
Función cognitiva y alteraciones extrapiramidales
Función motora y cognición están relacionadas (Alexander, 1986)
Los esquizofrénicos con discinesia tardía tienen mayor disfunción cognitiva (Brown, 1992)
Las disfunciones cognitivas preceden a la discinesia tardía (Wegner, 1986)
El parkinsonismo inducido por neurolépticos genera más déficit en orientación y memoria (Brown, 1991)

446
Disfunción cognitiva por SEP (Krausz 1999)
0 1 2 3 4 5 6
Percepción
Pensamiento
Motilidad
Falta automatización
Cuestionario de quejas de Frankfurt
Muchos SEP Pocos SEP

447
Efectos secundarios y relaciones sociales
Dificultades para establecer relaciones personalesDificultades para participar en actos públicos
(sequedad de boca)Alteraciones de la esfera sexual
AislamientoDisminución de la autoestima

448
Efectos secundarios y habilidades/aspecto físico
Torpeza motoraLentitud
Falta de expresión facial
Rechazo socialIntegración deficiente en la sociedad

449Empleo de nuevos antipsicóticos: importancia
para el paciente
76 77 78 79 80 81 82 83
Mejora de la motivación, ánimo, etc.
Mejor control de síntomas positivos
Menos efectos secundarios
Mejora el pensamiento y la atención
Puede vivir una vida normal
Encuesta a pacientes tras el paso de neurolépticos a nuevos antipsicóticos (Naber, ECNP 2000)
%

450Importancia de los motivosde cambio de un neuroléptico
a un nuevo antipsicótico
0 10 20 30 40 50 60 70
Disfunción cognitiva
Prolactina/disfunción sexual
Síntomas positivos
Síntomas negativos
Discinesia tardía
Recaída
SEP y S (±)
McEvoy, Scheiffer y Frances, 1999
Elección del tratamiento (%)

451
¿Cuál es la dosis ideal?
Escalada progresiva de dosis
Ventajas — Mejor tolerabilidad— Mínima dosis eficaz
Incovenientes— Tardanza de la
eficacia
Dosis de choque
Ventajas— Rapidez de
eficacia
Posibles estrategias:
Incovenientes— ¿Peor tolerabilidad?

452
Dosis idónea de antipsicóticos Eficacia: la que garantice un bloqueo suficiente de
los receptores D2 en el sistema límbico:— Antipsicóticos con K-off rápida: dosis altas— Antipsicóticos con selectividad límbica: dosis
altas— Antipsicóticos con riesgo de SEP: dosis
medias/bajas Tolerancia: la que evite una ocupación excesiva
en el estriado/corteza frontal— Risperidona, haloperidol, etc.: dosis
medias/bajas— Olanzapina, ziprasidona, amisulprida: dosis
medias-altas— Clozapina, quetiapina, aripiprazol: dosis altas

453
Mantenimiento de los antipsicóticos
Antipsicóticos con riesgo elevado de SEP:— Ajustar la dosis a la mínima posible para el
control de los síntomas positivos Antipsicóticos con bajo riesgo de SEP:
— Mantener dosis altas, que garantizan la estabilidad y minimizan las recaídas

454Consenso francés sobre usode antipsicóticos atípicos
en esquizofrenia
Importancia para el clínico Fase aguda Fase crónica
Eficacia +++ +++
Síntomas positivos +++ +
Síntomas negativos + +++
Agitación +++ +
Depresión + ++
Seguridad + +++
Síntomas extrapiramidales ++ +++
Acatisia ++ +++
Sedación + +++
Ganancia de peso + +++
Disfunción sexual + ++
Cumplimiento +++ +++
Experiencia subjetiva de los pacientes +++ +++
Lecrubier y cols., 2001

455 Metaanálisis: antipsicóticos clásicos frente a antipsicóticos
atípicos
Análisis de regresión de 52 ensayos controlados aleatorizados (Medline, EMBASE, PsychLIT, Cochrane)
12.649 pacientes con esquizofrenia o trastornos relacionados
Comparación de antipsicóticos atípicos (amisulprida, clozapina, olanzapina, quetiapina, risperidona, sertindol) con antipsicóticos clásicos (habitualmente haloperidol o clorpromazina) o antipsicóticos atípicos alternativos
Geddes y cols., BMJ 2000; 321: 1371-1376 Continúa

456
Criterios— Reducción de síntomas— Tasas de abandono— Efectos adversos, SEP: poco frecuentes con los
antipsicóticos atípicos La metarregresión sugiere que la dosis de los
antipsicóticos clásicos explica la heterogeneidad de los resultados en la reducción de síntomas y tasas de abandonos— Dosis de antipsicóticos clásicos iguales o inferiores
a 12 mg/día de haloperidol o equivalente igualan la eficacia y tolerabilidad de los atípicos, aunque éstos causan muy pocos síntomas extrapiramidales
Los atípicos no resultan más efectivos o mejor tolerados
Metaanálisis: antipsicóticos clásicos frente a antipsicóticos atípicos (cont.)
Geddes y cols., BMJ 2000; 321: 1371-1376
Resultados heterogéneos

457Metaanálisis de eficacia de antipsicóticos de segunda
generación 142 ensayos controlados, aleatorizados, con datos de
eficacia en:— 124 estudios de antipsicóticos de segunda
generación frente a los de primera generación (18.272 pacientes)
— 18 estudios de comparación entre antipsicóticos de segunda generación (2.748 pacientes)
Eficacia:— Algunos antipsicóticos de segunda generación >
antipsicóticos de primera generación (clozapina, amisulprida, risperidona, olanzapina > haloperidol)
— Los antipsicóticos de segunda generación no son un grupo homogéneo
Davis y cols. Arch Gen Psychiatry 2003; 60: 553-564

458Prevención de recaídas en esquizofrenia con antipsicóticos
de nueva generación
Ensayos controlados, aleatorizados, de 6 meses o más de duración, que compararon antipsicóticos de nueva generación con placebo y/o antipsicóticos clásicos
Análisis y resultados— Efectividad de antipsicóticos de nueva
generación en prevención de recaídas (6 estudios frente a placebo, 983 pacientes): son efectivos
— Recaída/fracaso del tratamiento (11 estudios frente a antipsicóticos clásicos, 2.032 pacientes): es menor con antipsicóticos de nueva generación
— Tolerancia: semejanteLeucht y cols. Am J Psychiatry 2003; 160, 7: 1209-1222 Continúa

459Prevención de recaídas en esquizofrenia con antipsicóticos
de nueva generación (cont.)
Los antipsicóticos de nueva generación tienen potencial para reducir las tasas de recaídas
Futuros ensayos deben ser dirigidos a mejorar aspectos metodológicos— Elección del comparador— Uso de dosis adecuadas— Aplicación de criterios de recaída
clínicamente relevantes— Monitorizar la adherencia al tratamiento— Minimización de abandonos
Leucht y cols. Am J Psychiatry 2003; 160, 7: 1209-1222

460Nueva generación de antipsicóticos frente a antipsicóticos
clásicos de baja potencia
Metaanálisis de todos los ensayos controlados de antipsicóticos de nueva generación (amisulprida, clozapina, olanzapina, quetiapina, remoxiprida, risperidona, sertindol, ziprasidona, zotepina)frente a
Antipsicóticos clásicos de baja potencia (< clorpromazina: clorprotixeno, levomepromazina, melperona, mesoridazina, metotrimeprazina, perazina, pipamperona, prometazina, protipendil, tioridazina)
Leucht y cols. Lancet 2003; 361: 1581-1589 Continúa

461Nueva generación de
antipsicóticos frente a antipsicóticos clásicos
de baja potencia (cont.)
Los estudios incluidos reunían criterios del Cochrane Collaboration Handbook— A: aleatorización adecuada, o— B: habitualmente estudios aleatorizados sin
una explicación precisa del método utilizado
Fueron evaluados con la escala Jadad (valora la calidad de los ensayos clínicos)— 1. ¿Es el estudio aleatorizado?— 2. ¿Es doble ciego? — 3. ¿Hay descripción de abandonos?— 4. ¿Se ha descrito la aleatorización
adecuadamente? — 5. ¿Está descrito adecuadamente el ciego?
Leucht y cols. Lancet 2003; 361: 1581-1589 Continúa

462Nueva generación de
antipsicóticos frente a antipsicóticos clásicos
de baja potencia (cont.)
Incluidos para el análisis: 31 ensayos con 2.320 pacientes en total
Antipsicóticos de nueva generación muestran mayor eficacia que antipsicóticos clásicos de baja potencia
Dosis 600 mg/día de clorpromazina o equivalentes no generan más riesgo de síntomas extrapiramidales que los antipsicóticos de nueva generación
Leucht y cols. Lancet 2003; 361: 1581-1589

463Medidas cautelares para el uso de antipsicóticos en
España
¿Son necesarias? ¿Están justificadas en 2007? ¿Pérdida de oportunidad terapéutica? ¿Dificultan el acceso al tratamiento a largo
plazo? ¿Está justificada la inequidad regional? ¿Es aceptable el agravio comparativo entre
distintas comunidades autónomas? ¿Transgreden la cartera de servicios comunes
del Sistema Nacional de Salud 2006?

464
Antipsicóticos y visado en ancianos (> 75 años)
N = 22.890, mayores de 65 años— Tratados entre 1994 y 2003 con
antipsicóticos típicos o atípicos— ¿Incremento del riesgo de mortalidad?— ¿Son necesarias medidas cautelares?— Conclusión: los antipsicóticos
convencionales no demuestran ser más seguros que los atípicos en población involutiva sin demencia
Wang y cols. N Engl J Med 2005; 353; 22: 2335-2341 Continúa

465
Antipsicóticos y visado en ancianos (> 75 años) (cont.)
N = 19.940 pacientes bajo tratamiento antipsicótico frente a N = 112.078 pacientes sin tratamiento antipsicótico, en residencias geriátricas de 5 estados norteamericanos— La mayor parte de los pacientes recibían
antipsicóticos atípicos— 6 meses de seguimiento (hospitalización por
tromboembolismos en instituciones Medicare)— Tasa de hospitalización por tromboembolismos.
Media: 0,91% personas/año• Risperidona: 1,98%• Olanzapina: 1,87%
Conclusión: complicaciones tromboembólicas escasas, algo superiores en pacientes en tratamiento con antipsicóticos atípicos y no incremento significativo con fenotiazinas
Liperoti y cols. Arch Intern Med 2005; 165: 2677-2682
• Clozapina y quetiapina: 2,68%• Fenotiazinas: 1,03%

466
Antipsicóticos en niños y adolescentes
Aumento de las prescripciones (EE.UU.):—1993: 201.000 menores en
tratamiento con antipsicóticos—2002: 1.224.000 menores en
tratamiento con antipsicóticos (Olfson y cols., 2006)
2000-2002: el 92,3% de las prescripciones de antipsicóticos fueron de antipsicóticos de segunda generación (Olfson y cols., 2006)
Uso cada vez mayor en trastornos no psicóticos Falta de estudios sobre seguridad y tolerancia
600%

467
Tolerabilidad en niños y adolescentes
Gothelf y cols. J Neural Transm 2003 Continúa
Olanzapina Risperidona Haloperidol
SEP (%) 23,6 11,8 57,2
Depresión (%) 11,8 26,3 71,4
Fatiga (%) 11,8 42,1 71,4
Sueño (%) 23,5 47,4 42,9
Sedación (%) 17,6 47,4 42,9
Concentración (%) 11,8 36,8 42,9

468
Tolerabilidad en niños y adolescentes (cont.)
Gothelf y cols. J Neural Transm 2003
Olanzapina Risperidona Haloperidol
Visión borrosa (%) 38 42 93
Sequedad de boca (%) 62 32 80
Estreñimiento (%) 31 32 27
Retención urinaria (%) 6 5 20
Náuseas (%) 50 53 47
Inquietud (%) 53 56 67

469
Aumento de peso en niños y adolescentes
Risperidona Olanzapina Clozapina Haloperidol
Ratzoni y cols., 200212 semanas
+3,9 kgIMC: +1,3
kg/m2
+7,2 kgIMC: +2,5
kg/m2
+1,1 kgIMC: +0,3 kg/m2
Sikich y cols., 20048 semanas
+4,9 kgIMC: +1,6
kg/m2
+7,2 kgIMC: +2,4
kg/m2
+3,6 kgIMC: +1,2 kg/m2
Shaw y cols., 20068 semanas
+3,6 kgIMC: +1,4 kg/m2
+3,8 kgIMC: +1,6
kg/m2

470Parámetros metabólicos y hormonales en niños y
adolescentes
Fedorowitz y Fombonne. J Psychopharm 2005
Risperidona
Olanzapina
ClozapinaHaloperid
olQuetiapin
a
Glucosa - ++ - - -
Colesterol + ++ + + -
Triglicéridos - + - - -
Prolactina ++ + + + -
Hormona tiroidea
- - - -

471Recomendaciones clínicasen el uso de antipsicóticos
en población pediátrica
Valorar los efectos secundarios que pueden interferir con el funcionamiento (p. ej., sueño y aprendizaje escolar)
Monitorizar los efectos secundarios metabólicos y hormonales
Monitorizar el aumento de peso

472
Terapéuticas psicológicas
Evolución histórica......................................
473-475 Generalidades............................................
476-484 Orientaciones cognitivas..............................
485-489 Terapia cognitivo-conductual.......................
490-505

473
Evolución histórica
Etapas— Visión organicista, representada por
Kraepelin: desintegración de la personalidad como consecuencia inevitable del deterioro cognitivo
— Visión del psicoanálisis: «demencia precoz» como neurosis narcisista que impedía la transferencia y el tratamiento analítico
Continúa

474
Evolución histórica (cont.)
Etapas (Slade y Haddock, 1996)— Década de 1960: terapias basadas en los
principios del condicionamiento operante— Década de 1970-1980: introducción de
tratamientos familiares y entrenamiento en habilidades sociales e instrumentales de los pacientes
— Década de 1990: consolidación de las dos modalidades anteriores e introducción y desarrollo de terapias cognitivo-conductuales (TCC) para el tratamiento de síntomas psicóticos residuales
Continúa

475
Evolución histórica (cont.)
— Florecimiento actual de las intervenciones psicológicas que significan un cambio en la atención, desde los procesos de rehabilitación o mejoría de discapacidades secundarias a los síntomas a centrarse en los propios síntomas (Birchwood, 1999)

476
Modalidades de intervención psicológica
Modelo de tratamiento comunitario asertivo de manejo de casos
Procedimientos de empleo protegido para la rehabilitación laboral
Intervenciones familiares Entrenamiento en habilidades Automanejo de la enfermedad Terapia cognitivo-conductual para síntomas
psicóticos Tratamiento integrado para pacientes de
diagnóstico dual

477Tratamientos psicológicos que han demostrado
eficacia
Intervenciones familiares psicoeducativas Entrenamiento en habilidades sociales Tratamientos cognitivo-conductuales, dirigidos
a:— Los síntomas positivos de la enfermedad— Las alteraciones de los procesos cognitivos
básicos subyacentes Paquetes integrados multimodales

478
Enfoque de los tratamientos psicológicos
Centrados en:— Efectos de la adaptación a las experiencias
psicóticas— Reducción de los síntomas psicóticos
residuales— Prevención de recaídas— Cumplimiento del tratamiento— Relaciones interpersonales— Adquisición de habilidades para la vida
independiente— Reducción del estrés— Reducción de la carga familiar

479
Terapias psicológicas:requisitos para su eficacia
Concepción de la esquizofrenia como un trastorno de base biológica que se puede manejar parcialmente por medio del aprendizaje y de la práctica de estrategias de afrontamiento
Utilización del modelo de vulnerabilidad-estrés como apoyo para la explicación de la sintomatología y del curso de la enfermedad
Consideración del establecimiento de una alianza terapéutica como prerrequisito para el adecuado desarrollo del resto de las actividades
Fenton. Schizophr Bull 2000 Continúa

480
Terapias psicológicas:requisitos para su eficacia (cont.)
Énfasis en la comprensión de la experiencia subjetiva del trastorno y el fortalecimiento de los recursos naturales de afrontamiento
Consideración del tratamiento como un proceso flexible y basado en las necesidades y capacidades individuales
Fenton. Schizophr Bull 2000

481
Limitaciones de los tratamientos existentes
La medicación antipsicótica y el apoyo comunitario son sólo efectivos de forma parcial para aproximadamente el 50% de los pacientes — Síntomas positivos persistentes— Episodios agudos recurrentes— Depresión y ansiedad habitual— Prolongada discapacidad social, con
pobreza, desempleo y restricción de vida

482
Fase y modalidad terapéutica
Fase ModalidadAplicació
nMetas terapéuticas
Prepsicótica PsicoeducaciónTerapia cognitivo-conductualTrabajo con la familiaTerapia familiar
IndividualIndividual
FamiliarFamiliar
Reducción de síntomas y de discapacidad
Reducción en el riesgo de psicosisMejora del funcionamiento familiar
Primer episodio de psicosis: fase aguda (0-2 meses aprox.)
Intervención y apoyo en crisisPsicoeducación
Individual y familiar
Reducción de la angustia emocionalMejora del conocimiento y comprensión de la psicosisEstrategias de afrontamiento adaptativasRegreso al funcionamiento normalReducción de estrategias de afrontamiento desadaptativasMcGorry, 2000 Continúa

483
Fase y modalidad terapéutica (cont.)
Fase Modalidad Aplicación Metas terapéuticas
Recuperación temprana (2-6 meses aprox.)
Manejo de casos basado en las necesidades
PsicoeducaciónTrabajo con familias, con
educación y apoyoIntervenciones de grupo,
basadas en necesidadesIntervenciones cognitivo-
conductuales para la recuperación
Psicoterapia de orientación cognitiva para las psicosis (COPE)
Prevención del suicidio
Reducción del consumo de cannabis (cognitivo-educativo-motivacional)
Individual
IndividualFamiliar
Grupal
Grupal
Individual
Adaptación óptima al inicio de la psicosis y a sus implicaciones
Reducción de la angustia emocional
Ajuste familiar óptimo y reducción de la angustia emocional
Reintegración, relaciones interpersonales, conocimiento y ocio
Rehabilitación laboral. Habilidades interpersonales
Buen conocimiento de aspectos relacionados con la enfermedad
Correcta adaptación y manejo de la enfermedad
Reducción de la comorbilidadFuncionamiento psicosocial
óptimoReducción de la ideación,
conducta y riesgo de suicidioReducción del uso de cannabis
McGorry, 2000 Continúa

484
Fase y modalidad terapéutica (cont.)
Fase Modalidad Aplicación Metas terapéuticas
Recuperación posterior (6-24 meses o más)
COPE
Prevención de recaída (+ psicoeducación + terapia de cumplimiento)
Tratamiento sistemático de síntomas positivos persistentes (STOPP)
Apoyo intensivo y educación para familias con pacientes con recaídas frecuentes y escasa respuesta al tratamiento
Intervenciones laborales, interpersonales y psicoterapéuticas
Individual
Individual
Individual
Familiar
Grupal
Adaptación óptima y funcionamiento con el mínimo malestar emocional
Buen conocimiento (un modelo explicativo de trabajo)
Tasa de recaídas mínimamente razonable
Buena adherencia a la medicaciónReducción de síntomas positivos
residualesReducción del malestar emocionalMejora del funcionamiento
psicosocial y de la calidad de vida
Reducción del impacto y de la angustia en la familia
Mejora en las formas de afrontamiento familiar
Crecimiento familiar y mejor calidad de vida
Progreso laboralMejor funcionamiento psicosocial,
mejores relaciones familiares y con los demás
McGorry, 2000

485
Orientaciones cognitivas en el abordaje de la esquizofrenia
Terapia psicológica integrada (TPI)1
Programas de rehabilitación del grupo de UCLA2
Terapia cognitiva de la esquizofrenia (TC)3
1 Brenner y cols., 1980; Roder y cols., 19882 Liberman, 1981, 19863 Perris, 1988

486Aproximaciones cognitivas:continuo de experiencias
psicóticas
Las experiencias psicóticas (p. ej., alucinaciones) son comunes en la población general (van Os y cols., 1999)
Solapamiento considerable en la frecuencia de aparición de ideas delirantes entre poblaciones generales y psicóticas, pero se diferencian en la convicción, preocupación y malestar (Peters, Garety y Joseph, 1999)

487
Aproximaciones cognitivas: percepciones
No son sólo los acontecimientos y experiencias los que conducen directamente al malestar o trastorno, sino el modo en que la persona percibe las experiencias —el significado que les da— lo que es crucial
Beck, 1976

488
Distorsiones cognitivas más frecuentes en la esquizofrenia
Identificación predicativa Atribuciones precipitadas de significado Sobreinclusión egocéntrica Confusión de causas y significados Desimbolización Concretización y perceptualización de
conceptos

489Un modelo cognitivo de los síntomas positivos de la
psicosis
Síntomas positivos
Vulnerabilidadbiopsicosocial
Estrés
Disfunción cognitiva básica
Experiencias anómalas
Cambiosemocionales
Factores de mantenimiento:• Razonamientos• Creencias, emociones y comportamientos• Reconocimiento de psicosis• Entornos adversos
Percepción de
experiencias
Percepción influida por:• Razonamientos• Creencias sobre sí mismo y el mundo• Aislamiento y entornos adversos
Garety y cols., 2001

490
Terapia cognitivo-conductual
La terapia cognitivo-conductual (TCC) fue desarrollada originalmente en la década de 1970 por el Dr. Aaron T. Beck en Philadelphia (EE.UU.) para tratar la depresión y la ansiedad
Enfocada en pensamientos negativos que conducen a emociones negativas: el significado atribuido a los acontecimientos y experiencias es lo que causa malestar
Explorar e indagar creencias sobre sí mismo, el mundo y el futuro: un proceso conjunto de investigación para probar nuevas maneras de pensar y actuar

491
Terapia cognitivo-conductualpara psicosis
Las limitaciones de los tratamientos existentes y la persistencia de síntomas positivos comportan la necesidad de nuevas aproximaciones
La psicosis se experimenta como un trastorno cognitivo, una alteración del pensamiento y la percepción: éstas son materias débiles de la TCC
Desarrollo de TCC para trastornos emocionales principalmente por psicólogos del Reino Unido a principios de la década de 1990
La TCC recurre a los modelos de psicosis por vulnerabilidad al estrés y cognitivos, con las percepciones como clave
Fowler, Garety y Kuipers; Chadwick, Trower y Birchwood; Kingdon y Turkington; Tarrier; Haddock y Bentall; Morrison

492Ámbitos de intervención cognitivo-conductual en las
psicosis Predisposición a la desorganización aguda Distorsiones perceptivas Deterioro de:
— Atención— Memoria— Razonamiento diferencial— Juicio social
Trastornos emocionales Deterioro en la regulación del afecto Incapacidad social Distorsión del sentido del yo y de los demás
Davidson, Lambert y McGlashan, 1998

493Objetivos de la terapia cognitivo-conductual para
psicosis
Reducir el malestar causado por los síntomas psicóticos
Desarrollar un entendimiento de la psicosis y posibilitar un autocuidado mejor
Mejorar la autoestima y reducir la depresión y la ansiedad
Reducir el riesgo de recaídas y la discapacidad social
Fowler, Garety y Kuipers, 1995

494
Terapia cognitivo-conductual para psicosis: puntos clave
Desarrollo participativo del entendimiento de experiencias psicóticas angustiosas
Reevaluación de las apreciaciones de las experiencias
Trabajo en factores de mantenimiento (p. ej., estilo de razonamiento, autoconcepto, aislamiento social, percepciones de psicosis, procesos emocionales)

495Métodos de terapia cognitivo-conductual para
psicosis
Combinada con medicación y servicios Sesiones ambulatorias semanales o
quincenales Sesiones que duren una media de 50 min Duración de 9 meses (media de 20 sesiones),
pero variable Terapeutas formados

496Terapia cognitivo-conductualpara psicosis del espectro
de las esquizofrenias
¿Cuál es la prueba de la efectividad?— Durante las décadas pasadas se han
llevado a cabo numerosos ensayos controlados, aleatorizados
— La mayoría de las personas incluidas tenían diagnóstico de esquizofrenia y síntomas positivos persistentes, con escasa respuesta a la medicación
— Las medidas de resultados principales fueron evaluaciones estandarizadas de síntomas psiquiátricos, pero también se evaluaron otros resultados

497
Puntuaciones de síntomas psiquiátricos (BPRS)
15
17
19
21
23
25
27
29
Inicio 9 meses 18 meses
Grupo de TCC Grupo sólo con tratamiento estándar
TCC n = 27Estándar n = 26
Kuipers, Garety, Fowler y cols., 1998

498
Cambio en los delirios
00,20,40,60,8
11,21,41,61,8
2
Convicción Preocupación
Grupo de TCC Grupo con tratamiento estándar
p = 0,1
p = 0,002
p = 0,06
Malestar
Kuipers y cols., 1998
Convicción Preocupación

499
Cambio en las alucinaciones
0
0,2
0,4
0,6
0,8
1
1,2
1,4
1,6
Frecuencia Intensidad Malestar
Grupo de TCC Grupo con tratamiento estándar
p = 0,17
p = 0,27p = 0,01
Kuipers y cols., 1998
Frecuencia
Intensidad Malestar

500La prueba actual: metaanálisis sobre ensayos de terapia
cognitivo-conductual
Selección sólo de ensayos clínicos aleatorizados de «alta calidad» (p. ej., asignación encubierta; información de inclusión y exclusión; terapia y control claramente definidos)
Uso de datos publicados y datos adicionales Resultados extraídos que reúnen el criterio de
inclusión, p. ej., medias y DE disponibles, excluyendo resultados con más del 50% de abandonos/perdidos
Puesta en común de datos comparativos
Pilling y cols., 2002; NICE Schizophrenia Guideline 2002

501
Metaanálisis sobre terapia cognitivo-conductual
Sólo diagnósticos del espectro de la esquizofrenia
13 ensayos y 1.293 pacientes Los estudios difieren en el estadio:
precoz/agudo (2); agudo mixto (2); síntomas persistentes (6); comunidad (2); día (1)
Países: Reino Unido (10); EE.UU. (2); Israel (1)
Pilling y cols., 2002; NICE Schizophrenia Guideline 2002

502Metaanálisis sobre terapia cognitivo-conductual:
conclusiones
1. Hay pruebas convincentes de que la TCC reduce los síntomas persistentes y el malestar que se mantiene durante más de un año postratamiento
2. Hay pruebas de que la TCC reduce los síntomas y mejora el insight al final del tratamiento
3. Hay pruebas más limitadas de mejoría en humor, recaídas, funcionamiento social y autoestima, y de que las mejorías duren hasta 5 años
Continúa

503Metaanálisis sobre terapia cognitivo-conductual: conclusiones
(cont.)
4. El tamaño del efecto —20-40% de reducciones— es similar al efecto de la mejor medicación antipsicótica para síntomas persistentes
5. La prueba sugiere que es más eficaz si es más larga: más de 6 meses y/o más de diez sesiones planeadas. En la práctica, son habituales 20 sesiones/9 meses
6. Las pruebas de salud económica sugieren que la TCC no es costosa y tiene un «buen precio»

504Terapia cognitivo-conductual: metaanálisis sobre resumen
de las pruebas
Los ensayos clínicos aleatorizados de TCC han demostrado ventajas para algunos pacientes
El tamaño del efecto o número necesario a tratar (NNT) sugieren que este tratamiento clínicamente merece la pena

505
Conclusiones
La TCC para la esquizofrenia está entrando ahora como tratamiento predominante en los servicios del Reino Unido
Ofrece mejoría de resultados Es concordante con los modelos
biopsicosociales de vulnerabilidad al estrés La TCC requiere un mayor refinamiento e
investigación, incluyendo cómo puede combinarse mejor con los tratamientos farmacológicos y sociales

506
Algoritmo de tratamiento de la esquizofrenia
IPAP, 2006 (OMS-CINP)— Nueva jerarquía de criterios:
• Tolerabilidad• Eficacia• Coste-efectividad
IPAP: International Psychopharmacology Algorithm ProjectOMS: Organización Mundial de la SaludCINP: Collegium Internationale Neuro-Psychopharmacologicum Continúa

507
Algoritmo de tratamiento de la esquizofrenia (cont.)
2. Considerar aspectos críticos iniciales o emergentes que afecten al manejo o elección de fármacos (aquí y
en cada nodo de tratamiento subsecuente)
1. Diagnóstico de esquizofrenia o trastorno esquizoafectivo
MONOTERAPIA3. Prueba de un antipsicótico atípico durante 4-6 semanas (amisulprida, aripiprazol, olantapina, quetiapina,
risperidona o ziprasidona) o, si no está disponible, prueba de haloperidol,
clorpromazina u antipsicótico típico
CONSIDERAR EN CADA ETAPAA. Riesgo de suicidioB. Aspectos metabólicos
(peso/olanzapina) y efectos secundarios inducidos por el tratamiento
C. Agitación grave o violenciaD. No cumplimientoE. Depresión o síntomas del humorF. Abuso de sustanciasG. Pródromos o primer episodioH. Catatonía o síndrome
neuroléptico maligno
4. ¿Prueba de dosisadecuada, duración,
no intolerancia?
NoSí
IPAP, 2006 Continúa
Sí

508
Algoritmo de tratamiento de la esquizofrenia (cont.)
5. ¿Persiste la psicosis tras el ajuste de dosis?
MONOTERAPIA6. 2.a prueba de un segundo antipsicótico
atípico durante 4-6 semanas, si está disponible o, si no, segundo antipsicótico
típico
7. ¿Prueba adecuada? (ver 4)
8. ¿Psicosis odiscinesia tardía grave o distonía tardía
tras ajuste de dosis?
Sí
9. Prueba de 6 meses con clozapinaSuperior a 900 mg/día
10. ¿Persistenlos síntomas?
12. Entra en fase de mantenimiento
11. Optimizar clozapina y/o aumentar con TEC o
medicación adyuvante, alternar estrategias
No
No
Sí
No
Sí

509
IPAP, junio 2005
Efectos secundarios de los antipsicóticos
Continúa
TípicosClozapin
aRisperidona
Olanzapina
Quetiapina
Ziprasidona
Aripiprazol
Amisulprida
Efectos extrapiramidales
Alguno - +++
0+ - < (si <4 mg)
0 - + (si <10
mg)0 0 - + 0 - + +
Discinesia tardía++ - ++
+0 - raro Raro Raro Raro Raro Raro Raro
Ataques 0,1-0,3% 2-6 % ~0,3% ~0,9% ~0,8% ~0,4% ~0,1% Raro
SedaciónAlguno -
++++++ + ++ ++ 0 - ++ 0 - + +
OrtostasisAlguno -
++++++ ++ + ++ + - ++ + - ++ +
Cardíacos, incluido QTc
+ - +++ + - ++ + 0 - + + - ++ ++ 0 - + 0 - +
Pruebas de función hepática
Alguno - ++
++ 0 - + ++ ++ 0 - + 0 - + 0 - +
Efectos anticolinérgicos
Alguno - +++
+++ + +++ ++ 0 0 0La estimación asume las dosis completas de antipsicóticos. Estimados por Osser y Meltzer, de la literatura y prospectos.

510
IPAP, junio 2005
Efectos secundarios de los antipsicóticos (cont.)
TípicosClozapin
aRisperido
naOlanzapin
aQuetiapin
aZiprasidon
aAripipraz
olAmisulprid
a
Agranulocitosis~1 en 50.000
6 en 1.000
<1 en 50.000
<1 en 50.000
<1 en 50.000
<1 en 50.000
<1 en 50.000
<1 en 50.000
Mayor Prolactina++ - +
++Pasajero +++
+ si >20mg
0 0 - + 0 +++
Ganancia de pesoalguno -
++
Media 5,44 kg/ 10 sem
Media 1,81 kg/6
sem
Media 5,44 kg/12 sem
Media 2,72 kg/6
sem0
Media 0,68 kg/6
sem
Media 0,9 kg/6 sem
Cataratas focales ¿0? ¿0? ¿0? ¿0?Algún riesgo
¿0? ¿0? ¿0?
Metabolizados por CYP P450
Varios1A2,
2D6, 3A42D6 1A2, 2D6 3A4 3A4 2D6, 3A4 No
Exacerbación de diabetes
+ - ++ +++ + +++ ++ 0 + ? 0
Hipertrigliceridemia
+ - ++ +++ + +++ ++ 0 0 0

511
11. Prevención de recaídas y comportamientos suicidas
Recaídas— Importancia de las recaídas..........................
512— Causas de las recaídas...........................
513-515 Estrategias de prevención
de recaídas ................................................ 516-524
Comportamientos suicidas y estrategias de prevención ........................
525-529

512
Importancia de las recaídas
El 50% recaen durante el primer año (Gaebel y Pietzcker, 1985)
El número de recaídas se correlaciona negativamente con el funcionamiento social (Curson, 1985)
La repetición de episodios hace que sean más difíciles de tratar y que requieran más tiempo para recuperarse (Loebel, 1995)
El coste de una recaída es igual que 100 años de tratamiento farmacológico (Wisted, 1991)
La mayoría de las recaídas se deben al abandono del tratamiento

513
Causas de las recaídas
Por enfermedad Exacerbación
idiopática— Evolución natural de
la enfermedad Falta de insight:
— Negación de la enfermedad
— Falta de adhesión
Psicosociales Falta de apoyo:
— Familiar (alta emoción expresada)
— Social (demandante)— Laboral
(competencia)— Ambiente estresante
Sistema de atención sanitario deficiente: — Tan sólo un 50% de
los pacientes mantienen su primera cita ambulatoriaMaguire, APA 2002 Continúa

514
Causas de las recaídas (cont.)Farmacológicas
Fijación elevada
Up-regulation de receptores
Mayor potencial de recaída
Continúa
Posible relación con la afinidad por el receptor
D2:

515
Causas de las recaídas (cont.)
Falta de eficacia:— Función cognitiva-
insight— Síntomas negativos:
abandonismo
— Síntomas afectivos: apatía
— Sintomas positivos: alteración de la conducta
Retirada por toxicidad Agranulocitosis, QTc
Efectos secundarios:— SEP, acatisia— Discinesia tardía— Hiperprolactinemia— Disfunción sexual— Obesidad— Sedación, bloqueo
Dificultad de toma:— Solución: velotab,
gotas, depot, etc.
Farmacológicas

516Riesgo de recaída por up-regulation de los
receptores D2
Los antipsicóticos con elevada afinidad (K-on) y elevada fijación (baja K-off ) por los receptores D2 inducen una up-regulation (sensibilización de los receptores)
Esta up-regulation está relacionada con la aparición de discinesia tardía
El abandono del antipsicótico, aunque sea de forma transitoria, en pacientes con up-regulation precipita recaídas, que también pueden producirse espontáneamente

517
Intervención familiar Elementos comunes de programas de actuación
— Educación sobre la esquizofrenia— Técnicas comportamentales— Mejorar la comunicación, especialmente
técnicas de escucha— Métodos para reducir las críticas y la
sobreimplicación— Reducción del contacto social entre el
paciente y sus familiares— Extensión de redes sociales de pacientes— Disminución de las expectativas familiares a
un nivel realista
Leff, 1995 Continúa

518
Intervención familiar (cont.)
Obstáculos al trabajo con familias en clínica— Convertir en un abordaje sofisticado lo que
puede ser aprendido por médicos no especialistas
— Ausencia de bases nacionales para enseñar técnicas de trabajo clínico con familias
— Costes económicos elevados para adquirir entrenamiento en servicios clínicos
Leff, 1995

519
¿Por qué psicoeducación?
Los pacientes y sus familiares tienen gran necesidad de información y el derecho a que les sea facilitada
Esta necesidad no se alcanza de forma satisfactoria en las condiciones clínicas habituales
Puede conseguirse mediante grupos psicoeducacionales

520
Psicoeducación
Incrementa el cumplimiento del tratamiento Reduce los índices de recidivas y de
readmisiones Mejora la calidad de vida Reduce el coste de la esquizofrenia

521
Objetivos de la psicoeducación
Informar a los pacientes y a sus familiares sobre la esquizofrenia
Eliminar prejuicios Mejorar el cumplimiento del tratamiento Reducir el riesgo de recidivas

522
Factores que afectan al cumplimiento-adherencia
Gravedad de la enfermedad Inducción de síntomas colaterales,
especialmente extrapiramidales Estigmatización temprana Primer contacto adecuado Recuperación cognitiva Contacto familiar Contacto con la comunidad Momento de reintegración Opinión de la población Factores profesionales Causas estructurales

523
Intervención psicosocial
Algunos psiquiatras creen que las intervenciones psicosociales son esenciales para la mejoría del nivel global de funcionamiento y la calidad de vida de los pacientes
El modelo más efectivo es la combinación de tratamiento positivo comunitario, grupos multifamiliares y psicoeducación familiar, todos coordinados por el equipo terapéutico
McFarlane

524
¿Cuál debe ser la duración del tratamiento preventivo?
Recomendaciones sobre la duración de la prevención de recidivas con tratamiento antipsicótico— Pacientes con primer episodio, al menos
1 o 2 años— Pacientes con múltiples episodios, al
menos 5 años— Pacientes que fueron peligrosos para sí
mismos o para otros, de forma indefinida en cualquier episodio

525
Esquizofrenia y suicidio: aspectos epidemiológicos
Más del 10% de los pacientes esquizofrénicos se suicida La mayoría lo hace durante los primeros años de la
enfermedad Más del 50% ha realizado tentativas previas Los síntomas depresivos y el alcoholismo están
estrechamente relacionados con esta conducta Se correlaciona con la presencia de acatisia y
desesperanza Habitualmente los pacientes que se suicidan son
jóvenes, con buen funcionamiento premórbido y grandes expectativas de rendimiento (Drake y cols.)
Más de un tercio de los suicidios se produce durante las primeras semanas que siguen al alta hospitalaria
Otro tercio se produce durante la hospitalizaciónTsuang, 1978; Roy, 2001

526
Factores de riesgo de suicidio en pacientes esquizofrénicos
Sexo masculino Edad inferior a los 30 años Desempleo Evolución crónica con exacerbaciones Consumo de drogas Alta hospitalaria reciente Antecedentes de tentativas previas Presencia de síntomas depresivos Subtipo paranoide Nivel educativo alto
Allebeck y cols., 1987; Fenton y McGlashan, 1991; Roy, 2001

527
Predicción de suicidio en esquizofrenia
Tentativas suicidas previas Depresión durante la hospitalización Ideación suicida durante la hospitalización Antecedentes familiares de trastornos afectivos Ajuste premórbido deficiente Quejas sexuales Agitación psicomotora durante la
hospitalización
Stephens y cols., 1999

528
Prevención de suicidio en esquizofrenia
La FDA ha aprobado el uso preventivo de la clozapina para reducir el riesgo suicida en pacientes esquizofrénicos
Mayor utilidad de nuevos antipsicóticos Tratamiento de comorbilidad
— Depresión: ISRS y antidepresivos tricíclicos— Uso-abuso de drogas
Programas de rehabilitación
Meltzer y cols., 1995; Roy, 2001

529Los nuevos antipsicóticos son más eficaces para prevenir el
suicidio
Intentosde suicidio (100 pacientes/año)
12
10
8
4
2
0Antes del estudio
Durante el estudio
9,3
6
10,6
2,7
6,3
Glazer y cols. J Clin Psychiatry 1998
Olanzapina Haloperidol

530
12. Impacto de la enfermedad
Generalidades.............................................
531-533 Calidad de vida...........................................
534-549 Discapacidad..............................................
550-553 Impacto económico...........................................
554 Estigma en la esquizofrenia..........................
555-556

531
Impacto global de la esquizofrenia
Estimación de la OMS sobre el impacto global de las enfermedades para el año 2000:— La esquizofrenia es la 7.a causa de años
perdidos por discapacidad (YLD) • Representa el 2,8% del total de YLD
— Sin embargo, en el rango de edad de 15 a 44 años asciende hasta el 3.er lugar
Brewin y cols., 1997

532
Impacto de la esquizofrenia
Mayor riesgo de:— Comorbilidad psiquiátrica— Comorbilidad somática— Exceso de mortalidad
Nivel de funcionamiento muy deficiente Un 25-50% intenta suicidarse y un 10-15%
consuma el suicidio Desempleo e índice de pobreza elevado Ausencia de relaciones sociales Sufrimiento para familiares y cuidadores

533
Resultados en la esquizofrenia
Proximales— Síntomas
positivos— Síntomas
negativos— Desorganización — Funciones
relacionales— Efectos
secundarios— Síntomas
residualesLehman, 1999
Distales— Nivel de
funcionamiento— Calidad de vida— Bienestar familiar— Seguridad pública

534
¿Qué es calidad de vida?
«Percepción personal de un individuo de su situación en la vida, dentro del contexto cultural y de valores en que vive, y en relación con sus objetivos, expectativas, valores e intereses» (OMS, 1993)

535
Calidad de vida y esquizofrenia
Relación muy compleja— Factores comunes a otras enfermedades:
cronicidad, falta de un tratamiento totalmente eficaz, efectos adversos de la medicación
— Factores exclusivos de la esquizofrenia: falta de insight, discapacidad notable, estigma social

536
Hitos históricos en calidad de vida y esquizofrenia
1970: desinstitucionalización y desarrollo de programas de salud mental comunitarios
1977: Index Medicus-palabra clave 1980: primeras evaluaciones de programas
comunitarios de salud mental en términos de calidad de vida
1984: Quality of Life Scale (QLS) (Heinrichs y cols.)
1988: Lehman Quality of Life Interview (QOLI) 1989: aprobación del Patient Outcome
Research Act por el Congreso de EE.UU. Comienzo del WHOQOL Group
Continúa

537Hitos históricos en calidad de vida
y esquizofrenia (cont.)
1990: antipsicóticos atípicos 1992: International Journal of QoL Research SF-
36 (Ware y Sherbourne) (ISOQOL) 1994: 7.o Congreso de la AEP (Viena): Calidad
de vida y discapacidad en trastornos mentales 1995: WHOQOL-100 1996: WHOQOL-BREF 1997: CSCV (Giner y cols.) 1999: ERIQA 2002: PETiT (Voruganti y Awad) 2003: S-QoL (Auquier y cols.)

538
Importancia de la calidad de vida en la esquizofrenia
Medida de resultados y de curso evolutivo de pacientes mentales crónicos
NIMH: Caring for Persons with Severe Mental Illness, identifica la calidad de vida como una de las principales áreas de resultados para evaluar
FDA: un requisito esencial para el registro de nuevos antipsicóticos
Medida de resultados en ensayos clínicos con implicación de nuevos antipsicóticos

539¿Por qué ha de evaluarse la calidad de vida de los pacientes
esquizofrénicos?
Determinar la eficacia de las intervenciones Ayudar en la toma de decisiones clínicas Valorar la calidad de los cuidados Estimar las necesidades de la población Comprender las causas y las consecuencias de
las diferencias en salud

540¿Qué sabemos de la calidad de vida de los pacientes
esquizofrénicos?
Peor que la de la población general y que la de otros enfermos mentales y físicos

541Calidad de vida: esquizofrenia frente a otras enfermedades
mentales
0
20
40
60
80
100
Func
ión físic
a
Rol f
ísico
Dolor
Salud
gen
eral
Vitali
dad
Func
ionam
iento so
cial
Rol e
moc
ional
Salud
men
tal
Esquizofrenia TOC Depresión Heroína
Func
ión
física
Rol fí
sico

542Calidad de vida: esquizofrenia frente a otras enfermedades
físicas
0
20
40
60
80
100
Func
ión físic
a
Rol f
ísico
Dolor
Salud
gen
eral
Vitali
dad
Func
ionam
iento so
cial
Rol e
moc
ional
Salud
men
tal
Esquizofrenia Trasplante renal Hemodiálisis Mielodisplasia

543¿Qué sabemos de la calidad de vida de los pacientes
esquizofrénicos? Jóvenes, mujeres, casados y bajo nivel de
educación refieren mejor calidad de vida A mayor duración de la enfermedad, peor
calidad de vida La psicopatología, en especial los síntomas
negativos y afectivos, se correlaciona negativamente con la calidad de vida
Escasos efectos secundarios y el tratamiento combinado (psicofarmacología + psicoterapia) mejoran la calidad de vida
Los pacientes integrados en programas comunitarios muestran mejor calidad de vida que los institucionalizados

544
Nuevos antipsicóticos y calidad de vida
Estos nuevos fármacos, al tener mayor eficacia sobre los síntomas negativos y un perfil de tolerancia más favorable, tienen un mayor efecto positivo sobre la calidad de vida
¿Superioridad de unos sobre otros?— Escasos estudios comparativos entre los
nuevos antipsicóticos— Calidad de las evidencias variada
Continúa

545
Nuevos antipsicóticos y calidad de vida (cont.)
MoléculaPrimer autor,
añoInstrumento Resultados
Amisulprida (AMI)- AMI frente a HAL- AMI frente a HAL- AMI frente a HAL frente a placebo
Colonna, 1998Carrière, 2000Saleem, 2002
QLSQLSQLS
AMI > HALAMI > HAL
AMI > HAL y placebo
Clozapina (CLZ)- CLZ- CLZ frente a NLP- CLZ frente a NLP- CLZ frente a HAL
Meltzer, 1990Naber, 1995Essock, 1996Rosenheck,
1997
QLSSWNQOLIQLS
CLZ > NLPCLZ = NLPCLZ > HAL
HAL: haloperidol; NLP: neurolépticos; QLS: Quality of Life Scale; SWN: Subjective Well-Being under Neuroleptics Scale; QOLI: Quality of Life Interview.
Continúa

546
Nuevos antipsicóticos y calidad de vida (cont.)
MoléculaPrimer autor,
añoInstrumento Resultados
Olanzapina (OLZ)- OLZ frente a HAL- OLZ frente a RISP- OLZ frente a RISP- OLZ frente a RISP
frente a NLP- OLZ frente a RISP
Revicki, 1999Tran, 1997Ho, 1998
Montes, 2003Gureje, 2003
QLS, SF-36QLS
PSYCH-BASE
EuroQoLQLS, SF-36
OLZ > HALOLZ > RISPOLZ = RISP
OLZ y RISP > NLPOLZ > RISP
HAL: haloperidol; RISP: risperidona; NLP: neurolépticos; QLS: Quality of Life Scale; SF-36: Medical Outcomes Study – Short-Form 36; PSYCH-BASE: Psychiatric Status You Currently Have – Baseline version.
Continúa

547
Nuevos antipsicóticos y calidad de vida (cont.)
Molécula Primer autor, año Instrumento Resultados
Risperidona (RISP)- RISP- RISP- RISP frente a NLP- RISP frente a APS- RISP frente a FPX
Barcia, 1996Bobes, 1998Franz, 1997
Mahmoud, 1997Hertling, 2003
QLSSF-36
MM-QoLSF-36, QOLI
EuroQoL
RISP > NLPRISP > APSRISP = FPX
NLP: neurolépticos; APS: antipsicóticos; FPX: flupentixol; QLS: Quality of Life Scale; QOLI: Quality of Life Interview; SF-36; Medical Outcomes Study – Short-Form 36, MM-QOL: Modified Munich QoL Dimension List for Schizophrenic Patients. Continúa

548
Nuevos antipsicóticos y calidad de vida (cont.)
MoléculaPrimer autor,
año Instrumento Resultados
Quetiapina (QUET)- QUET Velligan, 2003 QLS
Ziprasidona (ZIP)- ZIP O’Connor, 2001 QLS
Cambio de NLP a- OLZ, RISP- OLZ, RISP, QUET
Ritchie, 2003Voruganti, 2003
WHOQOL-BQLS
OLZ, RISP >OLZ, RISP, QUET
NLP: neurolépticos; OLZ: olanzapina; RISP: risperidona; QLS: Quality of Life Scale; WHOQOL-B: WHOQOL-BREF.

549Calidad de vida comparada:
1.a frente a 2.a generación de antipsicóticos.
CUtLASS 1
227 pacientes esquizofrénicos, 18-65 años, 14 centros de salud mental
Estudio multicéntrico, aleatorizado, sin soporte de la industria farmacéutica
Evaluaciones a las 12, 26 y 56 semanas Instrumentos: QLS, satisfacción y costes Conclusiones: no se encontraron diferencias en
el QLS, síntomas, costes y preferencias de los pacientes
Jones y cols., Arch Gen Psychiatry 2006; 63: 1079-1097
QLS: Quality of Life Scale

550
Causas líderes de años perdidos por discapacidad (YLD)
Worlwide, Year 2000 Estimate (WHO, 2001)
Rango Enfermedad
1 Depresión unipolar
2 Trastornos por uso de alcohol
3 Esquizofrenia
4 Anemia ferropénica
5 Trastorno bipolar
6 Pérdida de audición de inicio en la edad adulta
7 VIH/SIDA
8 Enfermedad pulmonar obstructiva crónica
9 Osteoartritis
10 Accidentes de tráfico
Edad: 15-44 años

551
Carga global de la esquizofrenia (GBD), años 1990 y 2000
Ayuso-Mateos. Draft 15-08-06. WHO
YLD: años perdidos por discapacidad; YLL: años perdidos por muerte prematura; DALY: años de vida en función de la discapacidad.
Hombres Mujeres Total
YLD- GBD 1990- GBD 2000
6.3977.873
5.7867.554
12.18315.427
YLL- GBD 1999- GBD
384144
230119
615263
DALY- GBD 1990- GBD 2000
6.7818.017
6.0177.672
12.79815.690

552Discapacidad en el paciente esquizofrénico: variables
influyentes
Síntomas positivos:— Breier, 1991— O’Connor y Herman,
1993— Montero, 1998
Síntomas negativos:— WHO, 1979— Möller, 1982— Kay, 1987— Carpenter, 1988— Goodman, 1989— Breier, 1991— Hwu, 1995— Shankar, 1995— Bailer, 1996

553
Funcionalidad y esquizofrenia
Hegarty y cols., 1994
El deterioro en el funcionamiento en la esquizofrenia es relativamente resistente a las distintas estrategias terapéuticas
0
20
40
60
80
100
Aire fresco Metrazol TEC Lobotomía Clorpromazina Decanoato deflufenazina
Paci
ente
s vi
vien
do in
depe
ndie
ntes
(%
)

554
Impacto económico
ProblemasPorcentaje de pérdidas-DALY-1990
Enfermedades infecciosas y parasitarias
Lesiones no intencionadas
Problemas mentalesa
Enfermedades cardiovasculares
Infecciones respiratorias
Condiciones perinatales
Neoplasias malignas
22,9
11,0
10,5
9,7
8,5
6,7
5,1
aIncluye: trastornos afectivos unipolares y bipolares, psicosis, epilepsia, demencia, enfermedad de Parkinson, esclerosis múltiple, dependencia de alcohol y drogas, TEPT, TOC, trastorno de angustia, otros trastornos neuropsiquiátricos.

555
Consecuencias del estigma en la esquizofrenia
Escasez de recursos para la ampliación de los servicios de psiquiatría comparado con otras patologías— Resolución 119/1992 de las Naciones
Unidas Problemas de vivienda Menores oportunidades de empleo
— En EE.UU. está empleado menos del 15% Aislamiento social Efectos negativos en la evolución de la
enfermedad mental Efectos negativos en las familias de las
personas con esquizofrenia

556
Estrategias para reducir la estigmatización (WPA, 2000)
Aumentar el desarrollo y el uso de fármacos que controlen los síntomas y reduzcan al mínimo los efectos secundarios estigmatizantes
Iniciar actividades educativas en la comunidad dirigidas a cambiar actitudes
Incluir la educación antiestigma en los profesores y profesionales sanitarios
Mejorar la psicoeducación de los pacientes y sus familiares sobre las formas de vivir con la enfermedad
Implicar a los pacientes y a sus familiares en la identificación de las prácticas discriminatorias
Promover acciones legales y sociales para reducir la discriminación

557
13. Aspectos médico-legales
Conductas violentas.................................... 558-561
Aspectos psiquiátrico-legales........................ 562-568

558
Conductas violentas
Autoagresivas: mutilaciones, ... suicidio Heteroagresivas: agresión física, ... homicidio Heteroagresivas + autoagresivas: gas,
ahogamiento, envenenamiento, incineración ...

559
Potencial de agresividad
0
1
2
3
4
Agresividad
Esquizofrenia Población general

560Factores de riesgo de conductas violentas en pacientes
esquizofrénicos
Sexo masculino Ser joven Bajo nivel socioeconómico Consumo de drogas Antecedentes de conducta violenta Reagudización reciente con presencia de
delirios y alucinaciones Alteraciones de la afectividad (disforia,
angustia, miedo) Agresividad verbal manifiesta o latente
Taylor, 1995; Junginger, 1996

561
Riesgo de conductas violentas
No todos los esquizofrénicos presentan riesgo elevado de este tipo de conductas
El riesgo se multiplica con el uso/abuso de alcohol y otras drogas
Estas conductas suelen ser de gran violencia, irracionales, absurdas e incomprensibles

562
Aspectos piquiátrico-legales. Inimputabilidad
Exento de responsabilidad criminal quien al tiempo de cometer la infracción penal, a causa de cualquier anomalía o alteración psíquica, no pueda:— Comprender la ilicitud del hecho: déficit
cognitivo— Actuar conforme a esa comprensión:
trastorno de la volición
Código Penal. Art. 20.1º, 1996

563
Valoración de la imputabilidad
La primera consecuencia penal será, sin duda, a efectos de la incidencia en la modificación de la responsabilidad criminal
Y posteriormente en relación con el pronóstico y la aplicación de medidas de seguridad
Como paso inicial es preciso llegar al diagnóstico, tanto de la variedad clínica como de la fase evolutiva en la que se encontraba el individuo en el momento de los hechos
Continúa

564
Valoración de la imputabilidad (cont.)
Posteriormente, determinar la existencia, en esas circunstancias, de síntomas activos, negativos o ausencia de éstos, siempre en relación con las exigencias explicitadas en el Art. 20 del Código Penal, desde los criterios mixtos, biológico-psicológicos de la inimputabilidad
Casi todos los fenómenos psicopatológicos que surgen tienen naturaleza e intensidad suficiente como para alterar de forma profunda el mundo cognitivo y condicionar la voluntad
Continúa

565
Valoración de la imputabilidad (cont.)
Son alteraciones que impiden a la persona que las padece conocer la realidad; el pensamiento desorganizado, el error de los sentidos, el delirio, la alucinación, la alteración de la afectividad, etc. suponen la percepción equivocada de la realidad y, por consiguiente, llevan a conductas conformes a esa percepción distorsionada de la realidad
La incidencia en esas cualidades básicas del comportamiento libre y voluntario puede ser total, disminuyendo notablemente o anulándolas
En esos casos, la psicopatología que presentan es base suficiente para plantearse una modificación sustancial de la responsabilidad criminal, en el sentido de disminución y, con mucha frecuencia, anulación

566
Imputabilidad del esquizofrénico y responsabilidad criminal
Se trata de una verdadera psicosis endógena que se caracteriza por:— Distorsiones fundamentales y
características del pensamiento y de la sensopercepción• Eco, inserción, robo o difusión del
pensamiento• Percepciones o ideas delirantes, voces
alucinatorias— Afectos embotados o inapropiados— Con el paso del tiempo pueden presentarse
déficit cognoscitivosContinúa

567
Imputabilidad del esquizofrénico y responsabilidad criminal (cont.)
Si el hecho se ha producido bajo los efectos del brote esquizofrénico, habrá de aplicarse la eximente completa del Art. 20.1 del Código Penal
Si no se obró bajo dicho brote, pero las circunstancias concretas del hecho revelan un comportamiento anómalo del individuo que puede atribuirse a dicha enfermedad, habrá de aplicarse una eximente incompleta del Art. 21.1 del Código Penal
Continúa

568
Imputabilidad del esquizofrénico y responsabilidad criminal (cont.)
Si no hubo brote y tampoco ese comportamiento anómalo del individuo en el supuesto concreto, nos encontraremos ante una atenuante analógica del Art. 21.6 del Código Penal, como consecuencia del residuo patológico, llamado defecto esquizofrénico, que conserva quien padece tal enfermedad; es necesario para aplicar la atenuante analógica del Art. 21.6 que el tribunal considere que los hechos están en relación causal psíquica con la afectación psiquiátrica que presenta